Необходимость рассмотрения плода как пациента связана с возможностью коррекции тяжелых патологических состояний, включая некоторые аномалии развития, фето-фетальный трансфузионный синдром (ФФТС) при монохориальном многоплодии, тяжелые формы гемолитической болезни плода.
Спектр болезней плода, подлежащих внутриутробной коррекции, с каждым годом расширяется, разрабатываются и совершенствуются новые технологии [1]. Сейчас в практику Уральского НИИ ОММ внедрены 11 фетальных методик, требующих импортных расходных материалов, которые в настоящее время Россией не закупаются. Мы готовы участвовать в разработке инструментария с нашими отечественными производителями, но для этого требуются значительные инвестиции.
Внутриутробная хирургия объединяет врачей различных специальностей — акушеров-гинекологов, неонатальных хирургов, анестезиологов-реаниматологов, специалистов биофизической и лучевой диагностики, трансфузиологов. В настоящее время в Уральском НИИ ОММ проводят внутриутробные операции совместно с детскими нейрохирургами, сосудистыми хирургами, урологами. Наши анестезиологи владеют методами обезболивания не только беременной женщины, но и плода.
Проблемами внутриутробной хирургии занимается международное сообщество «Плод как пациент» — междисциплинарная группа врачей, которая работает над совершенствованием методов диагностики и лечения плода. Российская Федерация — не исключение. В ноябре 2017 г. в Санкт-Петербурге пройдет уже второй съезд Российской ассоциации специалистов медицины плода. Молодых исследователей этой области медицины стремится поддерживать Общество фетальных хирургов. На многочисленных форумах и съездах дискутируются не только профессиональные, но и этические проблемы.
Внедрение методов фетальной хирургии в Уральском НИИ ОММ начато с апреля 2009 г. Опыт, накопленный с этого момента, позволяет нам в большинстве случаев не только точно диагностировать патологию плода, но и создавать протоколы внутриутробных операций.
На сегодняшний день институт ставит перед собой задачу освоения внутриутробной коррекции спинномозговой грыжи. В содружестве со специалистами тюменского Федерального нейрохирургического центра прошел I этап эксперимента по отработке этой операции (рис. 1).
Рис. 1. I этап эксперимента по коррекции спинномозговой грыжи. Здесь и далее в статье фото авторов
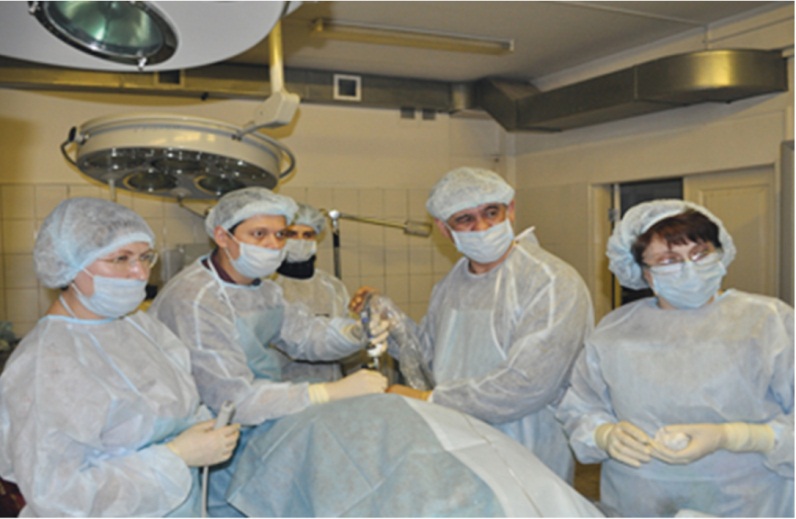
В статье представлен опыт нашего института по коррекции патологии плода методами внутриутробной хирургии. Все внутриутробные манипуляции прошли клиническую апробацию в экспериментах на животных и утверждены Этическим комитетом.
КРЕСТЦОВО-КОПЧИКОВАЯ ТЕРАТОМА
Крестцово-копчиковая тератома (ККТ) является наиболее распространенной опухолью, встречается примерно в 1 наблюдении на 40 000 живорождений [2]. ККТ представлены тремя видами зародышевых клеток (эктодермы, мезодермы и энтодермы) и эмбриологически происходят от узла Хенсена [2]. Большинство ККТ возникают спорадически, но были описаны несколько семей с аутосомно-доминантным типом наследования [2]. Ультразвуковая пренатальная диагностика позволяет диагностировать опухоль еще в начале II триместра. На фоне небольших ККТ обычно не возникают перинатальные проблемы. При ККТ значительного размера перинатальная смертность связана с декомпенсацией сердечно-сосудистой системы, артериовенозным шунтированием в пределах крупной сосудистой сети опухоли с развитием водянки плода [2].
Для плодов с плохим прогнозом было предложено несколько типов внутриутробного вмешательства. Несмотря на то что первая успешная открытая хирургическая резекция ККТ была выполнена N. S. Adzick и соавт. в 1997 г. [2], открытая хирургия зачастую связана с угрозой преждевременных родов, хориоамнионита, внутриутробной гибели плода, высоким риском осложнений со стороны матери [2]. Были также предприняты попытки использвать минимально инвазивные методы, такие как радиочастотная аблация или шунтирование кист опухоли [2]. Однако критерии необходимости пренатальных вмешательств при ККТ остаются неясными [3].
В практике Уральского НИИ ОММ мы провели 4 операции для чрескожного мини-инвазивного лечения ККТ. Показания к оперативному лечению формировали при ультразвуковой и МРТ оценке состояния плода и опухоли.
При УЗИ определяли выраженность кистозного и эхогенного компонентов (> 50%) и темп роста тератомы (быстрым считали рост опухоли на 1 см и более в 2 недели), при Doppler-исследовании — составляющие сосудистой сети опухоли. Регистрировали доплерометрические изменения кровотока в нижней полой вене, венозном протоке, вене пуповины, трикуспидальную регургитацию. Подтверждали экзофитный рост опухоли с помощью УЗИ и МРТ.
Объем опухоли рассчитывали с использованием трехмерной ультразвуковой системы VOCAL.
Тип ККТ определяли при МРТ, применяли классификацию Американской академии детской хирургии.
Тип I: развивается только за пределами плода (может иметь небольшую сакральную составляющую); встречается в большинстве случаев (47%).
Тип II: с внутритазовой и сакральной составляющими.
Тип III: экстраэмбриональная составляющая с брюшно-тазовой локализацией.
Тип IV: опухоль полностью развивается в тазу плода.
Показаниями к внутриутробному лечению послужили:
- быстрый рост опухоли;
- преимущественно экзофитный рост;
- преимущественно эхогенный компонент опухоли (> 50%);
- отношение объема опухоли к предполагаемой массе плода выше 0,12 см3/г;
- срок беременности до 28 недель.
Операции по коагуляции сосудистой ножки ККТ производили в сроке от 21 до 26 недель беременности. Средний срок проведения манипуляции составил 25,3 недели, средний возраст пациенток — 28,3 года. Три пациентки были первобеременными, одна — повторнобеременной повторнородящей. Соматический и акушерский анамнез у всех женщин не был отягощен. Все опухоли относились к I–II типу. Водянка у плода была зарегистрирована в одном наблюдении.
Эффективность операции составила 50%. У первой беременной после коагуляции сосудистой ножки тератомы плода с неиммунной водянкой (НИВП) произошли преждевременные роды в сроке беременности 28 недель. Во втором наблюдении увеличились внутритазовая и сакральная составляющие опухоли, что вызвало появление двустороннего гидронефроза у плода, и беременность была прервана по медицинским показаниям. Оставшиеся две пациентки беременность доносили в срок. Окончательно опухоль удаляли после рождения детей (рис. 2).
Рис. 2. Крестцово-копчиковая тератома у новорожденного после коагуляции сосудистой ножки тератомы в сроке 22 недели беременности
ОБСТРУКЦИЯ МОЧЕВЫВОДЯЩИХ ПУТЕЙ У ПЛОДА
Благодаря современным методам инструментальной диагностики выявляют широкий спектр патологии мочевыводящей системы плода (от агенезии до транзиторной пиелоэктазии). Внутриутробные вмешательства в пренатальном периоде могут оказаться эффективными только при некоторых аномалиях [4, 5]. Наилучшие показатели выживаемости, на основании данных Международного общества терапии и хирургии плода, регистрируются у плодов с синдромом заднего уретрального клапана [6, 7].
Нами проведены 27 шунтирующих операций почек плода при обструктивных поражениях мочевыделительного тракта у 19 пациенток с положительным эффектом. Показаниями для оперативной коррекции патологии мочевыводящих путей плода стали синдром задних уретральных клапанов, двусторонние/односторонние гидронефрозы III–IV степени. Шунтирующие операции на мочевом пузыре нами применяются редко и на более поздних сроках беременности, т. к. почечная паренхима фиксирует стент лучше. Целью операции является создание оттока мочи из почки плода в амниотическую полость. Первое стентирование во всех случаях проводили в сроке беременности 22–28 недель. Повторные шунтирования осуществляли при ультразвуковых признаках выпадения стента из почки.
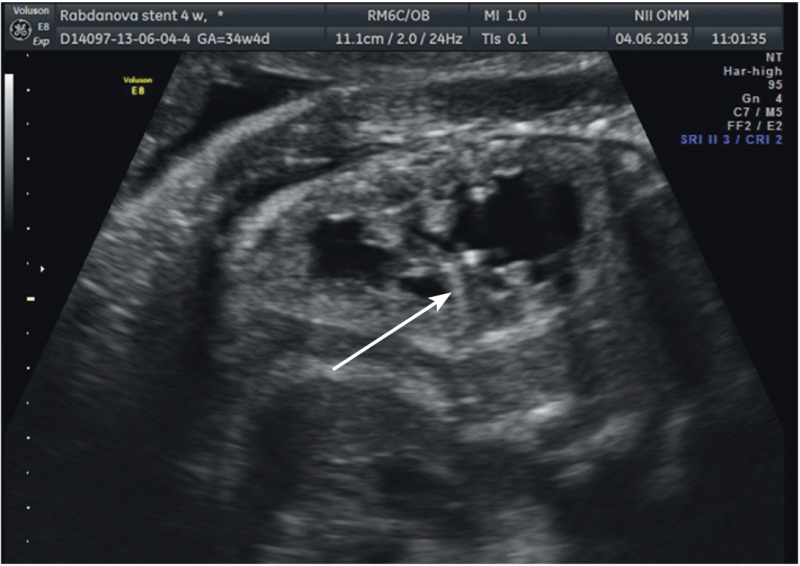
Для шунтирования почек мы применяли неонатальные стенты-эндопротезы фирмы Cook 3 Fr, роль проводника для стента выполняла спинальная игла 16G (рис. 3).
Рис. 3. Стент в почке плода
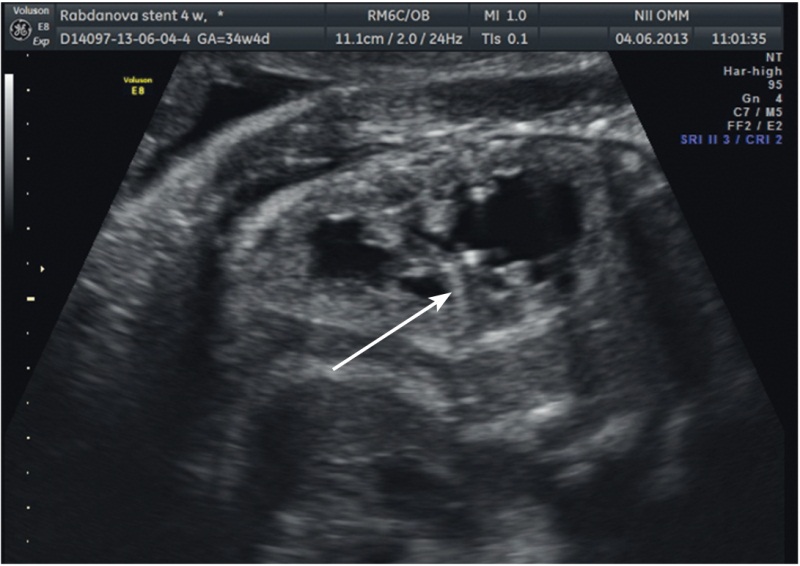
С учетом практического опыта Уральского НИИ ОММ по шунтирующим операциям на мочевыделительном тракте плодов разработан и изготовлен отечественный стент для внутриутробного нефро-амниального шунтирования (рис. 4). Наш стент имеет разнонаправленные спиральной формы пигтейлы и минимальный диаметр 3 Fr. Данное отечественное изделие апробировано в ряде экспериментов на беременных овцах, запатентовано и в настоящее время проходит государственную регистрацию [8].
Рис. 4. Общий вид стента для шунтирующих операций при пороках развития мочевыделительной системы плода, разработанный сотрудниками Уральского научно-исследовательского института охраны материнства и младенчества

ПАТОЛОГИЯ МОНОХОРИАЛЬНЫХ ДВОЕН
ФФТС формируется у 25–30% монохориальных двоен. Основоположники внутриутробного лечения ФФТС J. E. De Lia и соавт. (1999), R. Quintero (2002), J. Deprest (2002) с успехом применили лазерную коагуляцию плацентарных сосудов, а K. Benirschke и соавт. (1973) и B. K. Wittman с соавт. (1986) предлагали перевязку сосудов пуповины [9]. В нашей стране впервые коагуляция плацентарных анастомозов выполнена А. Е. Бугеренко в 2005 г. [10].
Основные методы коррекции, которые используются при синдроме трансфузии: септотомия (часто сочетается с амниоредукцией), серия амниоредукций (частота выживаемости хотя бы одного плода — 60–70%, неврологические нарушения — 24%); лазерная коагуляция сосудистых анастомозов в плаценте (частота выживаемости — 70–90%, неврологические нарушения — 8%) [11–14].
В нашей клинической практике мы применяли все методики коррекции ФФТС (серии амниоцентезов, септотомии) до селективной коагуляции плацентарных анастомозов, которая оказалась наиболее эффективным методом лечения (рис. 5). С 2010 по 2017 г. проведены 142 операции лазерной коагуляции плацентарных анастомозов. Коррекцию ФФТС производили при II–IV степени синдрома, эффективность лечения в 2016 г. составила 84% [15, 16].
Рис. 5. Лазерная коагуляция плацентарных анастомозов
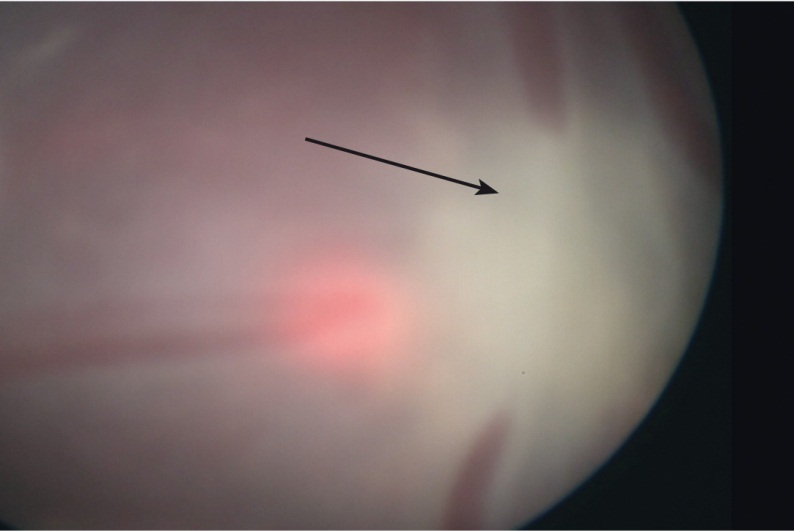
Как показывает практика, пациенток с ФФТС направляют в специализированные центры на более поздних стадиях. Запоздалая диагностика данного синдрома, особенно при ранней манифестации (до 20 недель), сопряжена с наименьшей частотой положительных перинатальных исходов. В настоящее время прогноз зависит от своевременной диагностики и метода лечения. При отсутствии коррекции прогноз, как правило, неблагоприятный и связан с высоким риском перинатальных потерь (70–90%) [16].
Особую актуальность приобретает поиск диагностических критериев, позволяющих прогнозировать формирование ФФТС на доклиническом этапе. На базе Уральского НИИ ОММ проводится научное исследование, которое направлено на изучение роли про- и антиангиогенных факторов роста и полиморфизмов генов, ассоциированных с нарушением ангиогенеза при патологиях монохориальной многоплодной беременности. Изменения ангиогенного статуса беременной на определенных этапах формирования плаценты могут быть одним из механизмов, связывающих аномальную плацентацию с развитием ФФТС. Фундаментальные исследования патогенеза ФФТС позволят в дальнейшем перейти на качественно новый уровень в области коррекции синдрома трансфузии и селективной задержки роста плода при монохориальном многоплодии.
СЕЛЕКТИВНЫЙ ФЕТОЦИД
Селективный фетоцид используют при дискордантных аномалиях, в частности при монохориальном многоплодии, когда один из плодов представляет угрозу для другого или создает риск прерывания беременности. В этих случаях редукция одного плода улучшает шансы другого и предотвращает прерывание беременности.
Окклюзия сосудов пуповины является одной из методик фетоцида и впервые начала применяться в пренатальной медицине с 1970–80 гг. прошлого столетия при осложненном течении беременности монохориальной двойней.
Окклюзия сосудов пуповины одного из плодов обеспечивает полное прекращение транзитного кровотока и предотвращает острую кровопотерю у второго плода. Это служит профилактикой гибели или грубых неврологических нарушений у оставшегося живым плода. В период с 2010 по 2014 г. был сформирован единый информационный массив, содержащий сведения о материнском акушерско-гинекологическом и соматическом анамнезе, особенностях течения настоящей беременности, способах родоразрешения, течении послеродового периода, перинатальных исходах монохориальных двоен. Из базы данных выделена группа из 40 пациенток, у которых была проведена лазерная коагуляция сосудов пуповины под контролем УЗИ [15–17].
На сегодняшний день мы испытываем большие трудности при обсуждении пациенток, которым необходима операция фетоцида, т. к. в российском законодательстве не прописаны показания к назначению данной манипуляции. Нет протоколов и порядка ее проведения, четко не обозначены пороки развития плода, при которых в любые сроки беременности возможно использование фетоцида [15–17].
ВНУТРИУТРОБНОЕ ВНУТРИСОСУДИСТОЕ ПЕРЕЛИВАНИЕ КРОВИ
Внутриутробное внутрисосудистое переливание крови производится для внутриутробной коррекция анемии, в большинстве случаев вызванной резус-конфликтной беременностью. Впервые лечение гемолитической болезни плода осуществили в 1977 г., когда P. L. Cooperberg провел первую интраперитонеальную трансфузию под контролем УЗИ, а в 1981 г. C. H. Rodek — первую внутрисосудистую трансфузию [18].
В настоящее время в России технологией внутриутробных гемотрансфузий владеют специалисты восьми перинатальных центров [19]. При наличии ультразвуковых признаков анемии у плода используют диагностический кордоцентез. При уровнях гематокрита меньше 30% и гемоглобина меньше 90 г/л плоду показана внутриутробная гемотрансфузия.
Внутриутробная внутрисосудистая гемотрансфузия является единственным эффективным методом лечения гемолитической болезни плода. В Уральском НИИ ОММ начиная с 2009 г. проведены 385 таких гемотрансфузий у 161 женщины в сроках беременности от 19 до 33–34 недель. Средний срок родоразрешения — 33,3 недели. Эффективность лечения составила 97,3%. Дети растут и развиваются нормально.
ОПЕРАЦИИ ПРИ ДИАФРАГМАЛЬНОЙ ГРЫЖЕ ПЛОДА
M. R. Harrison и соавт. в 1998 г. впервые опубликовали свои положительные результаты фетоскопической трахеальной окклюзии у плодов человека с помощью интратрахеально заполняемого пеной развертывающегося баллона. Данный вид операций внедрен в нашей клинике [20–22]. На сегодняшний день проведены 6 операций баллонной окклюзии трахеи в сроке беременности 26–27 недель (рис. 6).
Рис. 6. Внутриутробная трахеоскопия. GOOLDBAL — отделяемый баллон в трахее плода
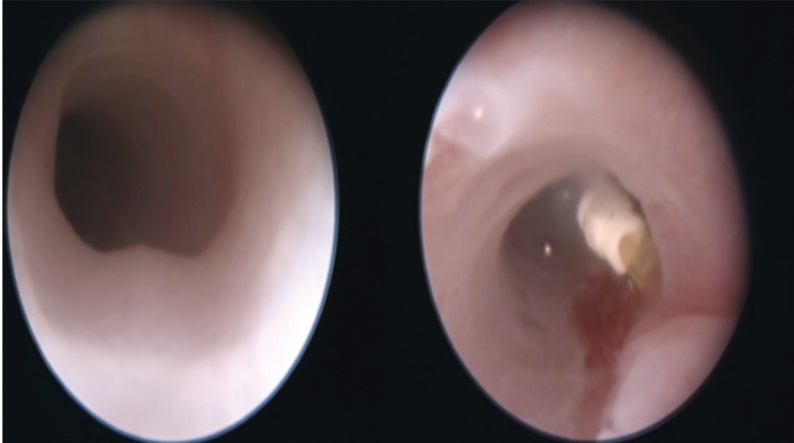
В 3 наблюдениях беременность удалось пролонгировать до 36–38 недель. Новорожденным проведена оперативная коррекция порока, дети выжили, растут и развиваются по возрасту. У троих пациенток в сроке 31–32 недели произошло преждевременное излитие вод, все они были родоразрешены путем кесарева сечения. Новорожденные погибли на вторые сутки жизни от дыхательной недостаточности. Таким образом, эффективность баллонной окклюзии трахеи составила 50%. В институте разработана система балльной оценки степени летальной гипоплазии легких у плода на основании данных УЗИ и МРТ для формирования показаний к внутриутробным вмешательствам.
ОПЕРАЦИИ ПРИ НЕИММУННОЙ ВОДЯНКЕ ПЛОДА
Пренатальная диагностика НИВП в настоящее время затруднений не вызывает. Основная проблема заключается в установлении причины ее развития, выборе метода лечения. Это зачастую возможно лишь в больших перинатальных центрах с хорошей лабораторной базой. Не всегда диагноз НИВП фатален.
Спектр нарушений, которые являются причиной НИВП, достаточно велик, и примерно у 30–60% причины остаются неизвестными. В Уральском НИИ ОММ за период 2012–2015 гг. проведено лечение 10 пациенткам, у плодов которых диагностировали НИВП и ультразвуковые признаки анемии (рис. 7): пиковая скорость в средне-мозговой артерии более 1,5 МоМ [23], кардио-феморальный индекс более 0,59.
Рис. 7. Неиммунная водянка плода в 22 недели беременности, выраженный подкожный отек у плода
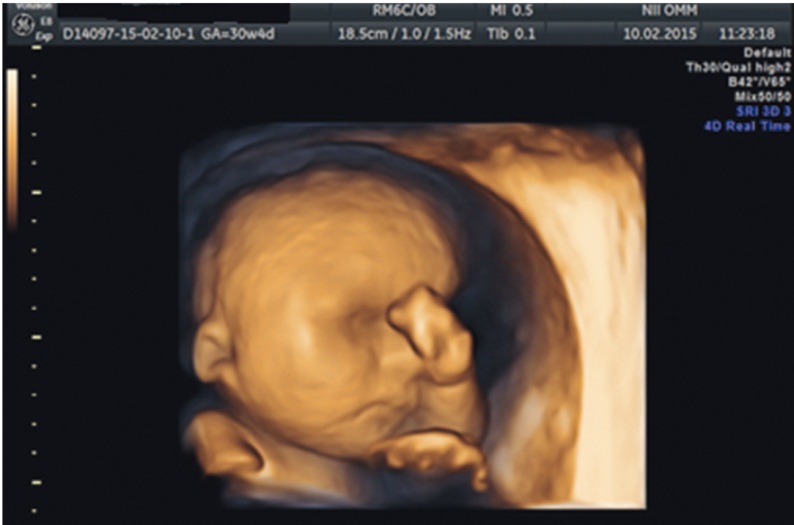
Все пациентки в первой половине II триместра беременности, в 15–17 недель, перенесли ОРВИ с клиническими признаками и подъемом температуры до субфебрильных цифр. Данные УЗИ, результаты лабораторных тестов при кордоцентезах и время развития симптомов НИВП схожи. Стоит отметить, что всем плодам был проведен кордоцентез с целью исключения хромосомной патологии.
У плодов была подтверждена вирусная этиология анемии — выявлены IgM к parvovirus B19 [24]. Поэтому беременной, перенесшей ОРВИ, необходимо регулярно (1 раз в 2 недели) проводить УЗИ, чтобы не пропустить анемию и развитие отека плода, при которых следует решить вопрос о ранней внутриутробной внутрисосудистой гемотрансфузии и, по возможности, лабораторными методами типировать возбудителя.
Во всех 10 наблюдениях в результате пренатального лечения НИВП анемия плода была скомпенсирована внутриутробными внутрисосудистыми переливаниями эритроцитарной массы и альбумина. Уровень гематокрита у плодов до внутриутробного переливания крови колебался от 5% до 12%. При дальнейшем динамическом УЗИ проявления НИВП полностью исчезли.
Роды, послеродовое наблюдение женщин и обследование новорожденных происходили в Уральском НИИ ОММ. Гестационный возраст наблюдаемых детей составил 38–39 недель. Все роды были оперативными, плановое кесарево сечение производили по совокупным показаниям со стороны матери и плода. Дети растут и развиваются по возрасту.
ОПЕРАЦИИ НА СЕРДЦЕ ПЛОДА
Коллектив института имеет собственный опыт дилатации закрытого овального окна плода в 30 недель беременности у пациентки П., 36 лет, которая наблюдалась в Уральском НИИ ОММ в связи с беременностью на фоне сахарного диабета 1 типа (длительность заболевания — с 20 лет). В 20 недель беременности пациентке было проведено экспертное УЗИ, и у плода установлен диагноз: фиброэластоз эндокарда левого желудочка, критический стеноз аортального клапана, дилатационная форма с уменьшенной систолической функцией, недостаточность митрального клапана и ретроградный поток крови в восходящей аорте (рис. 8). От прерывания беременности пациентка отказалась. В сроке 27–28 недель сформировалась гипоплазия левых отделов сердца (ГЛОС) с рестриктивным овальным окном. После проведения перинатального консилиума пациентке была предложена вальвулопластика овального окна.
Рис. 8. Пациентка П., 27–28 недель беременности: гипоплазия левых отделов сердца с рестриктивным овальным окном
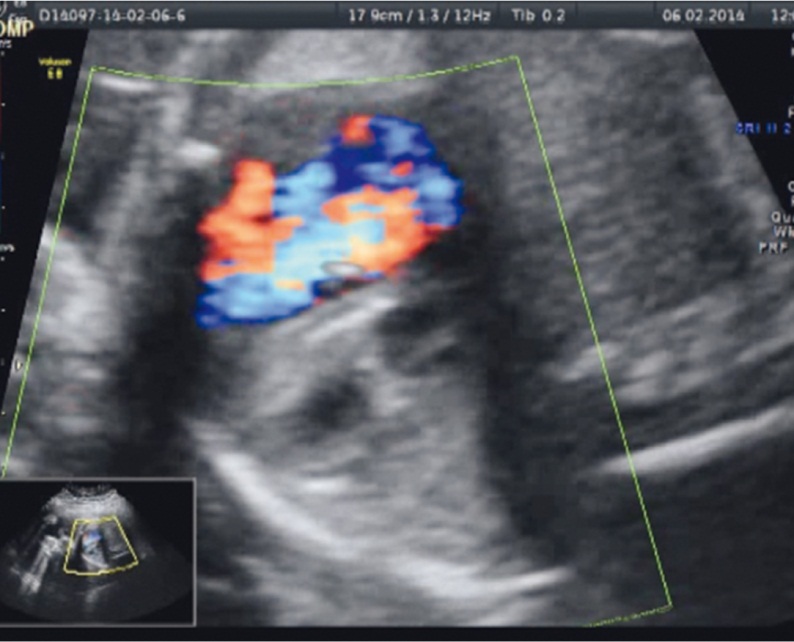
В 30 недель беременности нами совместно с сосудистым хирургом под постоянным ультразвуковым контролем проведена внутриутробная вальвулопластика овального окна. Через правое предсердие в полость левого предсердия введен проводник, затем стандартный коронарный дилатационный баллонный катетер MINI TREK 2,0 × 12 мм (Abbot Vascular, США). Баллон катетера трижды был максимально расширен, затем игла с баллонным катетером была удалена из предсердий. Во время операции особенностей в сердечной деятельности плода не было. При ЭхоКГ плода после операции зарегистрировано открытое овальное окно (рис. 9).
Рис. 9. Открытое овальное окно
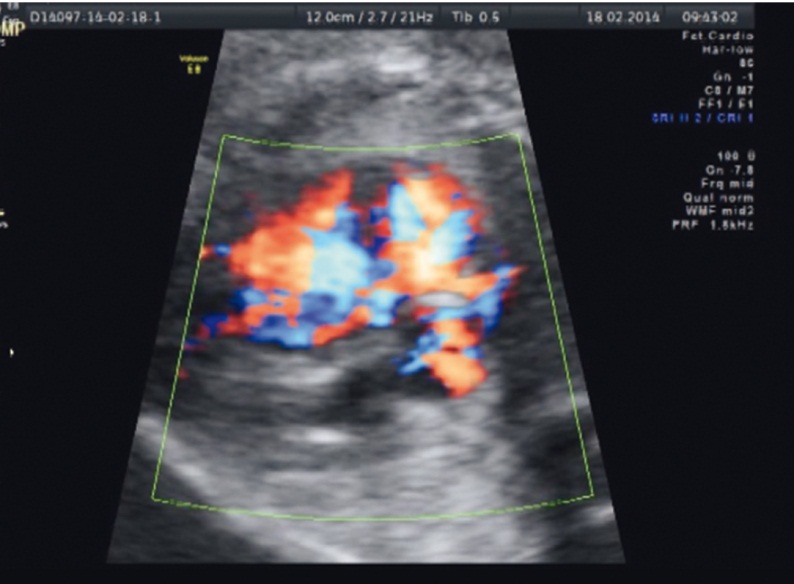
Пациентка П. была родоразрешена по акушерским показаниям путем операции кесарева сечения в сроке 34–35 недель. Новорожденный — мальчик, вес — 2090 г, рост — 43 см, 6/7 баллов по шкале Апгар, на самостоятельном дыхании. После консультации кардиохирурга младенцу непрерывно вводили алпростадил с целью профилактики закрытия фетальных коммуникаций [25].
Мы предполагаем продолжить исследования в области применения баллонной вальвулопластики клапанов сердца при ГЛОС, но столкнулись с проблемой позднего направления пациенток на данную манипуляцию.
ЗАКЛЮЧЕНИЕ
Развитие российской фетальной хирургии достигло стадии, когда стало возможным не только применять уже предложенные зарубежными авторами методики, но и разрабатывать собственные. Однако нужно производить отечественные инструментарий и расходные материалы. На собственном опыте мы убедились, что это возможно и необходимо.
Требуются система мониторирования всех внутриутробных вмешательств, проводимых в Российской Федерации, и оценка их эффективности, что позволит выделить центры, где внутриутробные вмешательства осуществляются с большей эффективностью [1]. Проведение отечественных мультицентровых исследований в данной области медицины поможет выработать единые подходы внутриутробной коррекции тех или иных патологических состояний плода.







