Вместе с тем одной из самых частых причин обращения к гинекологу пациенток в перименопаузе становятся аномальные маточные кровотечения (АМК), в этот период жизни не менее 50% женщин отмечают хотя бы один эпизод такого кровотечения [13].
По современной классификации причины АМК подразделяются на две группы: в первую входят структурные нарушения в матке, во вторую — причины, не связанные с ними [6]. Во второй группе одним из важнейших факторов нарушений менструальной функции в перименопаузе становится овуляторная и/или эндометриальная дисфункция. Поскольку гиполютеинизм и ановуляция на разных этапах закономерно сопровождают угасание функции яичников, нет ничего удивительного в возникновении рецидивов АМК дисфункционального происхождения. Считается, что именно маточные кровотечения дисфункционального генеза представляют собой наиболее частый вариант АМК в перименопаузе [1, 5].
Полный спектр факторов, вызывающих маточные кровотечения без структурных изменений, не определен, но, по-видимому, локальные гемостатические механизмы являются вторичными по отношению к отсутствию циклической продукции прогестерона, нарушению биосинтеза простагландинов и других субстанций, обеспечивающих контроль кровопотери [7]. Однако те же регуляторные расстройства повышают вероятность возникновения гиперпластических процессов эндометрия, причем его гиперплазия может развиваться при низких абсолютных показателях эстрадиола, поскольку ведущим фактором риска оказывается длительность «неприкрытых» эстрогенных воздействий. Следовательно, сочетание как АМК, так и гиперплазии эндометрия с симптоматикой климактерического синдрома вполне возможно.
Риск гиперпластических процессов и снижение качества жизни в связи с непредсказуемыми и часто обильными маточными кровотечениями обусловливают необходимость проведения противорецидивной терапии пациенткам с АМК в перименопаузе. Варианты такой терапии достаточно многообразны. Вместе с тем в возрасте 40 лет и старше у женщин закономерно появляются показания к менопаузальной гормональной терапии (МГТ). Возможно ли лечение гормональными препаратами для достижения двух целей: терапии климактерических расстройств и надежного контроля цикла с минимизацией риска гиперплазии эндометрия?
Цель настоящего исследования: определение эффективности и безопасности купирования симптомов климактерического синдрома препаратом МГТ, содержащим комбинацию 2 мг эстрадиола валерата и 0,15 мг левоноргестрела, у женщин в перименопаузе с АМК.
МАТЕРИАЛЫ И МЕТОДЫ
Исследование проводили в 2008–2010 гг. на базе кафедры акушерства и гинекологии № 1 ГБОУ ВПО «Первый Московский государственный медицинский университет им. И. М. Сеченова». Были обследованы 53 пациентки с климактерическим синдромом и АМК в перименопаузе. Возраст их варьировал от 43 лет до 51 года (в среднем — 46,9 ± 1,6 года).
Критериями включения в исследование стали возраст старше 40 лет; наличие вазомоторных симптомов климактерического синдрома (приливы жара и ночная потливость); нарушения менструального цикла, соответствовавшие критериям АМК, не далее чем за 3 месяца до момента включения в исследование; уровень ФСГ, превышавший 20 мМЕ/мл; информированное согласие на участие в исследовании.
Критерии исключения: кровотечения после года менопаузы; АМК, обусловленные субмукозной миомой матки, аденомиозом, атипической гиперплазией и раком эндометрия; наличие интерстициальной или субсерозной миомы матки с размером доминирующего узла 4 см и более; противопоказания к проведению МГТ; текущее или недавнее (в пределах 3 месяцев до момента включения в исследование) применение комбинированных эстроген-гестагенных препаратов.
Степень тяжести климактерического синдрома (нейровегетативных, психоэмоциональных и метаболических нарушений) оценивали в баллах модифицированного менопаузального индекса (ММИ). Обследование пациенток включало общий осмотр с оценкой антропометрических данных, гинекологическое исследование. Применяли клинические методы: клинический анализ крови, общий анализ мочи, биохимический анализ крови с определением параметров жирового и углеводного обменов, цитологический скрининг. В качестве данных маммологического скрининга принимали результаты маммографии, проведенной в пределах года до включения в исследование.
УЗИ органов малого таза производили всем пациенткам в начале исследования, на фоне лечения в 1, 3, 6-м циклах за 3–5 дней до окончания приема препарата и на 5-й день от начала менструального или менструальноподобного кровотечения для оценки толщины и структуры эндометрия. Сканирование проводили при помощи приборов Logiq 500 PRO (General Electric, США) c использованием абдоминального и влагалищного конвексных датчиков с частотой 3,5 и 7,5 МГц соответственно. При УЗИ определяли три размера матки и яичников, размеры шейки матки, величину М-эха и его структуру.
Гистероскопию с применением гистероскопа фирмы Storz (Германия) и раздельное диагностическое выскабливание стенок полости и шейки матки с последующим морфологическим исследованием соскобов делали 49 пациенткам; у 4 участниц от внутриматочного вмешательства было решено воздержаться ввиду того, что они перенесли данную процедуру за 2–3 месяца до обращения и имели медицинскую документацию, свидетельствовавшую о нормальном морфологическом состоянии эндометрия (эндометрий фазы пролиферации).
В качестве средства МГТ был выбран препарат Климонорм в режиме 3-недельного приема с недельным перерывом с 5-го дня 1–3-го спонтанного менструального кровотечения после проведенного кюретажа. Климонорм является комбинированным двухфазным препаратом для МГТ и содержит 2 мг эстрадиола валерата в 21 таблетке курсового лечения и 0,15 мг левоноргестрела в последних 12 таблетках. Длительность наблюдения составила 24 недели, после чего препарат был отменен.
Эффективность терапии в отношении симптомов климактерического синдрома оценивали по динамике ММИ. Влияние лечения на состояние эндометрия определяли по результатам УЗИ, а также морфологического исследования биоптатов/соскобов эндометрия. Материал для морфологического исследования эндометрия получали на 4-й неделе в цикле после отмены лечения. Его брали с помощью вакуум-кюретажа аспирационной одноразовой кюреткой Pipelle de Cornier у 31 пациентки и с помощью кюретажа под контролем гистероскопии у 22 женщин с исходной гиперплазией эндометрия.
Статистическая обработка данных была выполнена на персональном компьютере с использованием электронных таблиц Microsoft Excel и пакета прикладных программ Statistica for Windows v. 6.0 (StatSoft Inc., США). Все полученные количественные анамнестические, клинические, лабораторные и инструментальные данные обработаны методом вариационной статистики. Для каждого количественного параметра были определены среднее значение (М), среднеквадратическое отклонение (δ), ошибка среднего (m), медиана (Ме), для качественных данных — частоты (%). Применяли параметрические методы (парный критерий Стьюдента); анализ количественных данных, изменяющихся в динамике, осуществляли с помощью критериев Фридмана и Вилкоксона. Для нахождения различий между качественными показателями использовали метод χ2 с поправкой Йейтса на непрерывность, а также точный критерий Фишера для небольших выборок. Достоверными считали различия при р < 0,05 (95%-й уровень значимости).
РЕЗУЛЬТАТЫ
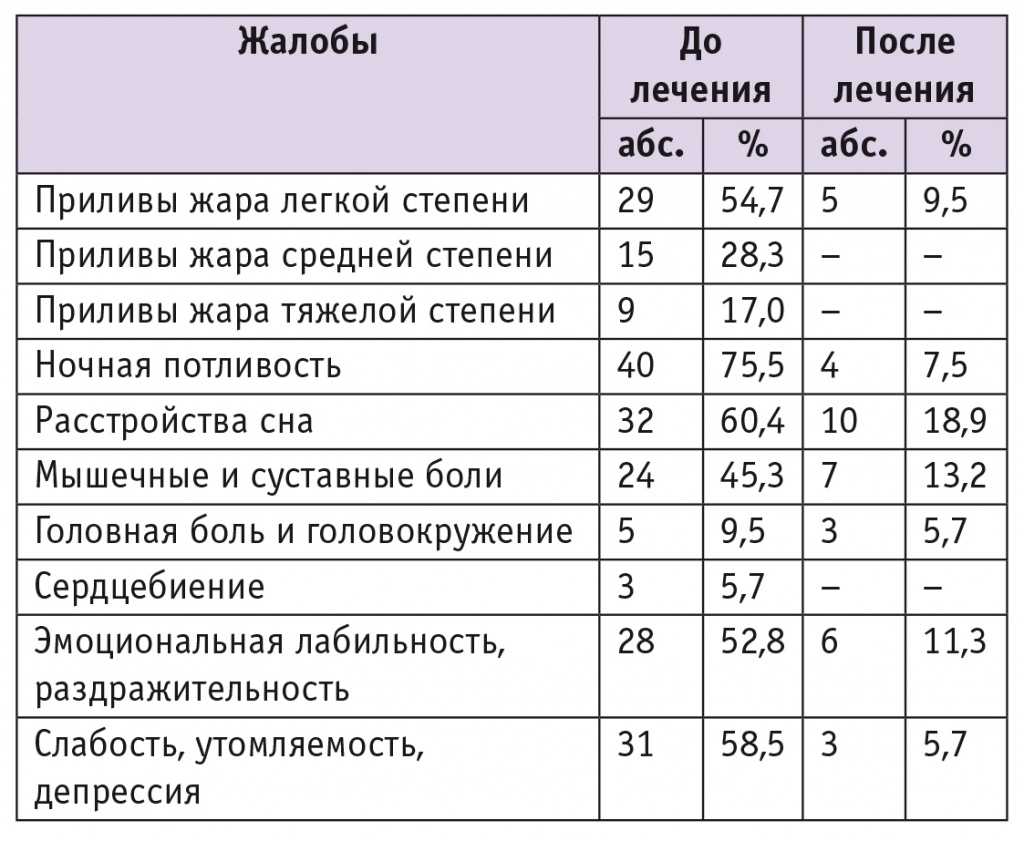
При опросе женщины предъявляли жалобы на приливы жара, число и интенсивность которых в большинстве наблюдений соответствовали легкой и средней степени климактерического синдрома (табл. 1). Среди других жалоб с разной частотой встречались ночная потливость, расстройства сна, мышечные и суставные боли, головная боль и головокружение, сердцебиение, эмоциональная лабильность, раздражительность, слабость, утомляемость, депрессия.
Таблица 1
Климактерические расстройства у обследованных пациенток до и после лечения (n = 53)
В анамнезе отмечали высокую частоту АМК в раннем и позднем репродуктивном возрасте: 29 (54,7%) пациенток перенесли хотя бы один эпизод кровотечения, не связанного с беременностью, в возрасте до 40 лет. В перименопаузе у 27 (50,9%) женщин наблюдался первый эпизод маточного кровотечения, у 26 (49,1%) нарушения цикла имели место в течение 3 месяцев и более. Аномальные маточные кровотечения были представлены необильными ациклическими кровотечениями у 27 (50,9%), обильными ациклическими кровотечениями — у 13 (24,5%), гиперполименореей — у 8 (15,1%), межменструальными кровотечениями — у 5 (9,5%) пациенток. Средняя продолжительность кровотечения у женщин с гиперполименореей составляла 8,1 ± 1,5 дня.
По результатам УЗИ, увеличение М-эха от 10 мм и более на 5–7-й день менструального цикла было отмечено у 20 (37,7%) пациенток. Размеры М-эха от 6 до 9 мм с неоднородной структурой эндометрия диагностировали у 15 (28,3%) женщин, нормальный по структуре и толщине эндометрий (М-эхо до 5 мм) наблюдали у 7 (13,2%) участниц, а в 11 (20,8%) случаях на фоне тонкого (нормального) эндометрия при УЗИ визуализировали гиперэхогенные образования или локальные утолщения размерами от 9 до 18 мм, расцененные как полипы.
При анализе морфологических заключений эндометрий без признаков функциональной активности желез (гипопластичный) был выявлен у 3 (5,7%), эндометрий фазы пролиферации — у 16 (30,2%), полипы эндометрия (без аденоматоза) — у 12 (22,6%), простая гиперплазия эндометрия — у 20 (37,7%), сложная гиперплазия без атипии — у 2 (3,8%) пациенток. Подозрение на патологию эндометрия по данным УЗИ не подтвердилось у 12 (22,6%) женщин: у 10 из них основанием для подозрения на нее стал показатель М-эха 6 мм, у 2 — локальные утолщения эндометрия.
При сопоставлении характера нарушений менструального цикла, ультразвуковой картины и результатов гистологического исследования мы обнаружили, что гиперплазия эндометрия ассоциировалась с обильным (56,1%) или необильным (43,9%) ациклическим кровотечением, длительными нарушениями цикла в перименопаузе, эпизодами аномальных кровотечений в репродуктивном возрасте и величиной М-эха 7 мм и более. У всех участниц исследования с гиперплазией эндометрия климактерический синдром протекал в легкой форме. Полипы эндометрия встречались у пациенток с сохраненным ритмом менструаций и гиперполименореей или межменструальными кровяными выделениями, наличием полипов эндометрия в анамнезе (58,3%) и с данными УЗИ, свидетельствовавшими о локальном утолщении эндометрия (гиперэхогенном образовании) у 10 (83,3%) женщин и неоднородном диффузном утолщении М-эха до 9 мм в 2 (16,7%) случаях.
Эффект гормональной терапии оценивали через 6 месяцев лечения. Положительную реакцию наблюдали в отношении всех климактерических жалоб, особенно вазомоторных симптомов и психоэмоциональных нарушений (см. табл. 1). Среднее значение ММИ на фоне лечения снизилось от 22,2 ± 2,53 балла до 9,5 ± 0,59 балла (p < 0,001).
В процессе лечения 47 (88,7%) женщин отмечали регулярные менструальноподобные кровотечения в перерыве между приемами препарата, у 6 (11,3%) кровотечения отмены начинались в последние 2 дня приема препарата, что не стало причиной для отказа от лечения. Субъективно уменьшение количества теряемой крови отметили 43 (81,1%) больные. Продолжительность менструальноподобного кровотечения уменьшилась до 5,4 ± 1,1 дня после 6 месяцев терапии (р < 0,01).
Для оценки динамики состояния эндометрия мы разделили участниц на четыре категории в зависимости от исходных данных УЗИ: 1 — величина М-эха 10 мм и более; 2 — М-эхо от 6 до 9 мм; 3 — М-эхо 5 мм и менее; 4 — локальные утолщения эндометрия размером 9–18 мм. Результаты трансвагинального эхографического сканирования эндометрия до и после лечения представлены в таблице 2.
Таблица 2
Эхографическая характеристика эндометрия обследованных пациенток до и после лечения, мм
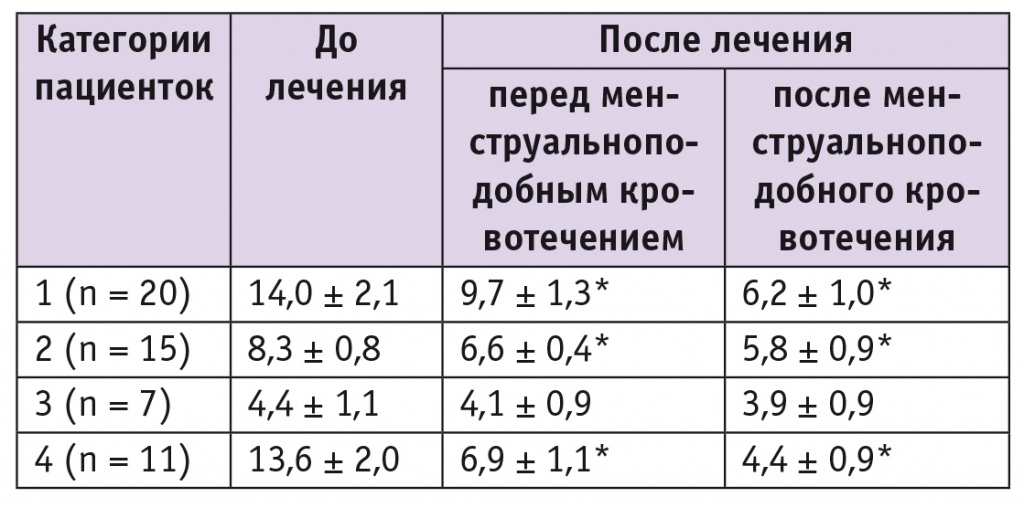
* Отличие от показателя до лечения статистически значимо (р < 0,05).
При динамическом ультразвуковом сканировании мы не отметили отрицательной динамики показателя М-эха. Его величина до и после менструальноподобного кровотечения в заключительном цикле исследования была достоверно меньше по сравнению с данными, полученными накануне выскабливания, у пациенток, М-эхо которых превышало 5 мм. У женщин с исходно тонким эндометрием величина М-эха не менялась на протяжении всего периода лечения. При индивидуальном анализе результатов УЗИ признаки гиперплазии эндометрия (неоднородная структура и/или М-эхо более 7 мм) были отмечены у 3 женщин, из них у двух до лечения была верифицирована сложная, у одной — простая гиперплазия эндометрия. При последующем морфологическом исследовании у этих 3 (5,7%) пациенток была подтверждена простая гиперплазия эндометрия.
Результаты морфологического исследования эндометрия до и после лечения представлены в таблице 3.
Таблица 3
Результаты морфологического исследования эндометрия пациенток до и после лечения (n = 53)
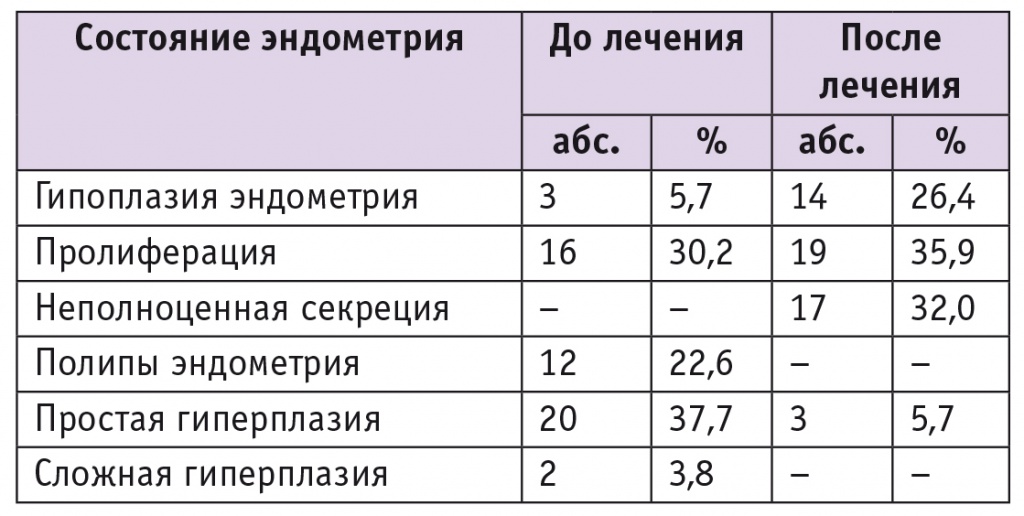
Таким образом, на фоне лечения менопаузальных расстройств препаратом, содержащим 2 мг эстрадиола валерата и 0,15 мг левоноргестрела, наблюдалась положительная динамика состояния эндометрия. В совокупности полипы и диффузная гиперплазия эндометрия до лечения были обнаружены у 34 (64,2%), а после лечения — у 3 (5,7%) пациенток (р < 0,01). Преобладающим морфологическим заключением до лечения являлась простая гиперплазия эндометрия, после лечения — нормальная пролиферация. Прогрессирования патологического процесса не отмечено ни в одном случае. Простая гиперплазия рецидивировала у одной больной, имевшей тот же морфологический диагноз до назначения лечения, и была выявлена у 2 пациенток с диагностированной до начала лечения сложной гиперплазией эндометрия.
ОБСУЖДЕНИЕ
Эстрогены используют для МГТ несколько десятилетий, и их положительное действие на симптомы климактерического синдрома доказано в многочисленных исследованиях [11]. Одним из неблагоприятных последствий длительного (10–15 лет) «неприкрытого» применения эстрогенов является повышение риска гиперплазии и рака эндометрия [12]. Основная стратегия защиты эндометрия — назначение прогестагенов в составе МГТ. Добавление прогестагенов существенно редуцирует или полностью нивелирует риск рака эндометрия у пациенток с интактной маткой, в результате риск этого заболевания у женщин, получавших комбинированную терапию эстрогенами и прогестагенами, оказывается сопоставимым или даже сниженным по сравнению с таковым у женщин, подобную терапию не получавших.
Но следует учитывать, что влияние циклических режимов МГТ на эндометрий далеко не однозначно и зависит от длительности применения, дозы и характеристик прогестина [12]. Применение современных эстроген-прогестагенных комбинаций с подобранными дозами и режимом компонентов является более предпочтительным, чем использование эстрогенного и прогестагенного компонентов в виде двух препаратов, требующее высокого уровня самоконтроля. Оптимальные эстроген-прогестагенные комбинации не только не повышают риск развития рака, но снижают его, как и риск гиперплазии эндометрия [9].
Как показало наше исследование, сочетание гиперпластического процесса и симптомов климактерического синдрома отнюдь не является невероятным. Основание для ожидания такого сочетания — новое понимание происхождения вазомоторных симптомов у женщин с сохраненной менструальной функцией и в перименопаузе, которое в качестве главной причины приливов жара полагает старение гипоталамуса и повышение порога его чувствительности к гормонам [2, 10]. В то же время овариальная эстрогенная секреция в первую фазу менопаузального перехода характеризуется перемежающимися эпизодами гиперэстрогении и гипоэстрогении, которые на фоне сниженной продукции прогестерона формируют симптомы АМК и климактерических расстройств [1].
Назначение циклической комбинированной МГТ с сильным прогестагенным компонентом в этой ситуации имеет очевидные преимущества, поскольку позволяет, с одной стороны, предотвратить рецидивы маточных кровотечений, а с другой стороны, уменьшить или полностью купировать проявления климактерического синдрома.
Естественно, что наличие гиперпластического процесса требует особой осторожности в проведении МГТ. Назначение препарата, содержащего комбинацию левоноргестрела и эстрадиола валерата, представляется целесообразным, поскольку левоноргестрел обладает высокой активностью в отношении эндометрия, и данный препарат обеспечивает надежную защиту эндометрия у большинства женщин.
Наши результаты свидетельствуют о безопасности 6-месячного приема препарата с точки зрения состояния слизистой тела матки. Безопасность применения этого средства МГТ демонстрируется и в других исследованиях, в том числе у женщин с подтвержденными гиперпластическими процессами эндометрия вплоть до сложной гиперплазии [3].
Целесообразность назначения комбинированного двухфазного препарата МГТ пациенткам с подтвержденной сложной гиперплазией является спорной; наши данные свидетельствуют о сохранении гиперплазии у таких женщин, хотя положительная динамика наблюдалась и в отмеченных ситуациях. Несмотря на сохранение простой гиперплазии эндометрия у одной из обследованных больных, мы считаем возможным назначать данный препарат таким пациенткам, тем более что динамическое УЗИ позволяет с высокой точностью своевременно выявлять патологические изменения эндометрия.
Тем не менее чрезмерная продолжительность использования циклических режимов МГТ не приветствуется [12]. Данный вид гормональной терапии рекомендуется только на этапе менопаузального перехода, и по мере приближения к возрасту естественной менопаузы стоит подумать о переводе пациентки, входящей в группу риска развития рака эндометрия, на низкодозированный монофазный режим.
В зависимости от исходного состояния здоровья женщины возможно индивидуально выбирать другие способы коррекции менопаузальных симптомов и контроля менструальных кровотечений [1, 8]. Можно полагать, что у пациенток с гиперплазией эндометрия и легкими вазомоторными проявлениями более адекватным подходом будет назначение прогестагенов, а при необходимости предохранения от беременности — комбинированных гормональных контрацептивов. Эстроген-прогестагенная комбинация с левоноргестрелом в этом ряду будет иметь преимущества для женщин с умеренными/тяжелыми вазомоторными симптомами в отсутствие гиперплазии эндометрия, но в индивидуальных случаях назначение такой терапии пациенткам с гиперплазией и легким течением климактерического синдрома не противопоказано.
ЗАКЛЮЧЕНИЕ
Улучшение самочувствия, статистически значимая редукция частоты и выраженности вазомоторных и психосоматических симптомов климактерического синдрома являются ожидаемым и давно известным позитивным эффектом терапии препаратом, содержащим левоноргестрел и эстрадиола валерат, отмеченным многими авторами. Анамнестические данные о гиперплазии и полипах эндометрия не должны служить основанием для отказа от назначения менопаузальной гормональной терапии (МГТ) женщинам, имеющим показания для этого вида терапии.
Лекарственное средство для МГТ необходимо выбирать с учетом прогестагенной активности в отношении эндометрия. Климонорм, в состав которого входит сильный прогестаген левоноргестрел, позволяет эффективно купировать симптомы климактерического синдрома, осуществлять профилактику аномальных маточных кровотечений, не оказывая негативного воздействия на состояние эндометрия.







