В отношении термина SSA/P консенсус до сих пор не достигнут. «Аденома» предполагает неопластический характер образования, что согласно законам общей патологии должно сопровождаться тканевым и/или клеточным атипизмом. «Полип» же является макроскопической характеристикой, однако не все SSA/P полиповидные — многие относятся к приподнятым (0-IIa), плоским (0-IIb) и углубленным (0-IIc) образованиям [3, 5], — что делает применение термина «полип» некорректным. Компромиссным решением может быть использование выражения «зубчатое образование на широком основании» [8], но данная терминология пока не введена, а традиционно используется термин SSA/P.
В настоящее время принята схема зубчатого пути канцерогенеза, берущего начало от очага аберрантных крипт гиперпластического типа и оканчивающегося зубчатой аденокарциномой [9, 13] (рис. 1). Вместе с тем понятие «зубчатая аденокарцинома» классификационно еще не определено [14].
Рис. 1. Схема зубчатого пути канцерогенеза [12].
Примечание. ACF-Hns — non-serrated hyperplastic-type aberrant crypt focus (очаг аберрантных крипт гиперпластического типа, незубчатый); ACF-Hs — serrated hyperplastic-type aberrant crypt focus (очаг аберрантных крипт гиперпластического типа, зубчатый); CIMP-H — CpG island methylator phenotype-high (метиляторный фенотип CpG island высокий); CIMP-L — CpG island methylator phenotype-low (метиляторный фенотип CpG island низкий); GCHP — goblet-cell-rich hyperplastic polyp (гиперпластический полип, богатый бокаловидными клетками); IGFBP7 — insulin-like growth-factor-binding protein 7 (белок 7, связывающий инсулиноподобный фактор роста); MAPK — mitogen-activated protein kinase — ERK pathway (митоген-активируемая протеинкиназа ERK-пути); MGMT — O6-methylguanine-DNA methyltransferase (О6-метилгуанин-ДНК-метилтрансфераза); MLH1 — MutL homolog 1 (гомолог MutL 1); MSI-H — high level microsatellite instability (высокий уровень микросателлитной нестабильности); MSI-L — low level microsatellite instability (низкий уровень микросателлитной нестабильности); MSS — microsatellite stable (микросателлитная стабильность); MVHP — microvesicular hyperplastic polyp (микровезикулярный гиперпластический полип); N — normal mucosa (нормальная слизистая оболочка); OIS — oncogene-induced senescence (онкоген-индуцированная последовательность); SAC — serrated adenocarcinoma (зубчатая аденокарцинома); SSA — sessile serrated adenoma (зубчатая аденома на широком основании); SSA-HGD — sessile serrated adenoma with high-grade dysplasia (зубчатая аденома на широком основании с дисплазией высокой степени); TSA — traditional serrated adenoma (традиционная зубчатая аденома); TSA-HGD — traditional serrated adenoma with high-grade dysplasia (традиционная зубчатая аденома с дисплазией высокой степени)
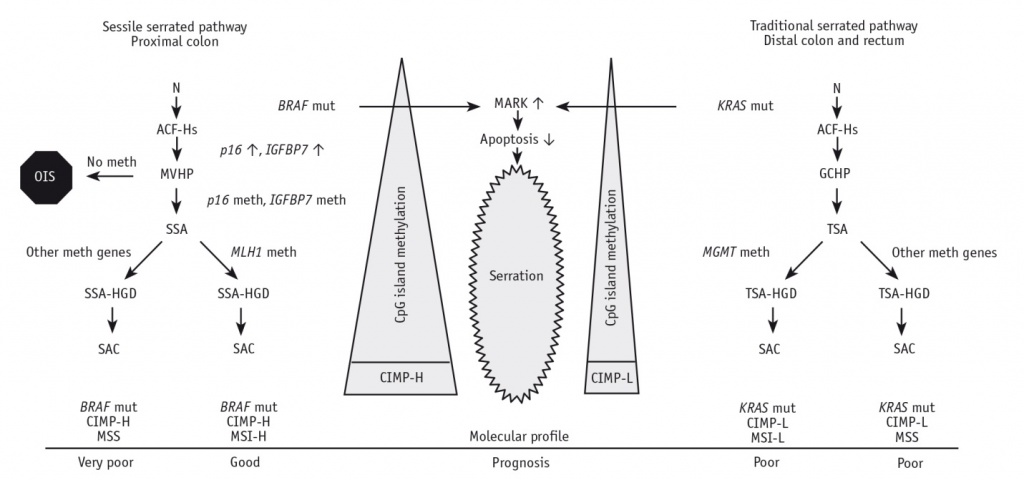
Зубчатый путь характеризуется уникальным молекулярным профилем и включает в себя ряд генетических и эпигенетических альтераций [14]. Начальной является активирующая мутация в одном из протоонкогенов KRAS или BRAF (мутации имеют взаимоисключающий характер). Эпигенетический механизм, лежащий в основе зубчатого пути канцерогенеза, основывается на гиперметилировании последовательностей пар нуклеотидов цитозин — гуанин (CpG island), обнаруживаемых в промотерных участках генов. Эти изменения приводят к формированию метиляторного фенотипа, который в большей или меньшей степени угнетает экспрессию генов, в том числе генов-супрессоров опухолевого роста р16 и IGFBP7, что препятствует апоптозу поврежденных клеток. Гиперметилирование может происходить в генах hMLH-1, ответственных за репарацию ДНК, а это приводит к быстрому накоплению генетических мутаций в клетке и к развитию рака [1].
В отношении каждого из видов зубчатых образований описаны особенности, которые позволяют предположить характер патологии еще на этапе эндоскопического исследования.
Для HP характерны следующие признаки:
- встречаемость во всех отделах толстой кишки, но с преимущественным распространением в прямой и сигмовидной кишках;
- размер чаще всего небольшой (менее 5 мм);
- тип образования плоско-возвышенный (0-IIa), на широком основании (0-Is) (Парижская классификация [17]);
- слизистая не отличается по цвету от окружающей или более белесоватая;
- структура ямок: 1-й тип по классификации NICE (англ. Narrow-band imaging International Colorectal Endoscopic classification) [6, 16];
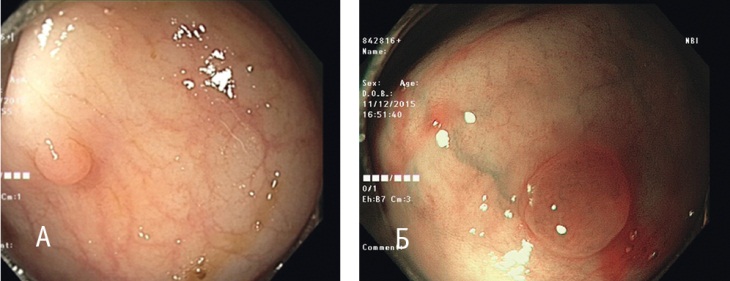
- капиллярный рисунок не расширенный, регулярный, сетчатого типа, вокруг ямок (рис. 2).
Образование сигмовидной кишки до 4 мм с четкими, ровными краями, гладкой поверхностью; структура 1-го типа по классификации NICE; капиллярный рисунок без расширения, регулярный, сетчатого типа.
Примечание. Здесь и далее NBI — narrow band imaging (узкий спектр света)
На основании рекомендаций ВОЗ по диагностике зубчатых образований толстой кишки [14] в качестве морфологических критериев HP приняты:
- наличие зубчатости цитоплазматического типа, формирование которой связано с выбуханием цитоплазмы клеток в просвет крипты в виде зубцов (просвет продольно-ориентированных крипт пилообразный, поперечно-ориентированных — звездчатый);
- отсутствие расширения базальных отделов крипт вдоль мышечной пластинки слизистой оболочки;
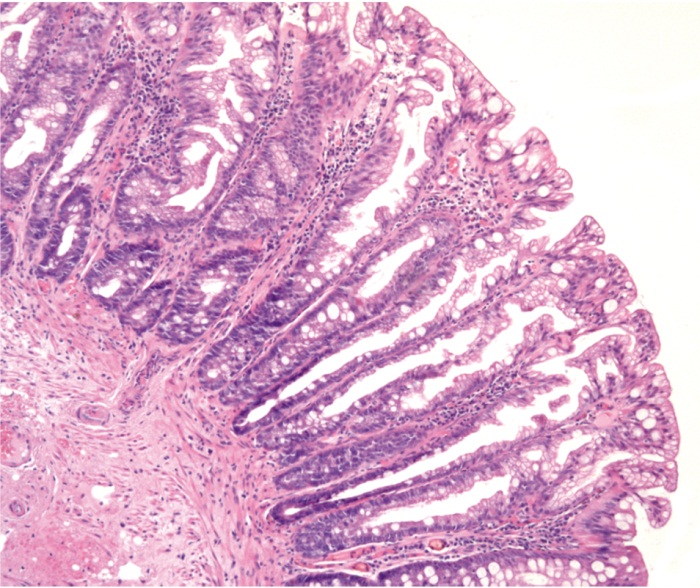
- отсутствие дисплазии эпителия (рис. 3).
Зубчатость цитоплазматического типа в верхней половине крипт (просвет пилообразный), базальные отделы крипт не расширены, дисплазия отсутствует
Помимо перечисленных критериев для HP характерно наличие зубчатости только в верхней половине крипт, однако расширение зубчатой зоны не является диагностически значимым.
По нашим наблюдениям, среди SSA/P наиболее часто встречаются SSA/P 1-го и 2-го типов, различия которых в большей степени проявляются при осмотре в режиме узкого спектра света (англ. narrow band imaging, NBI) с увеличением.
Общие признаки образований SSA/P:
- преимущественное распределение в правых отделах толстой кишки;
- размер более 5 мм;
- наличие на поверхности образования слизи желтого цвета — «муцинозной шапки»;
- тип образования плоско-возвышенный (0-IIa) [17];
- слизистая не отличается по цвету от окружающей, но во время исследования обращает на себя внимание локальная утеря сосудов подслизистого слоя за счет утолщения слизистой;
- фестончатые края;
- мелкозернистая поверхность (рис. 4, 5).
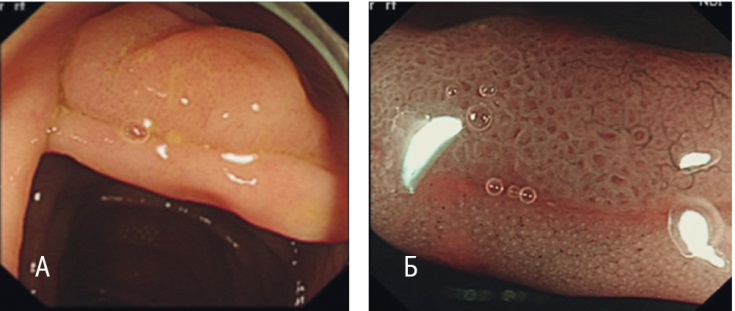
Рис. 5. Зубчатая аденома/полип на широком основании 2-го типа. А — режим белого света; Б — режим NBI c увеличением. Фото авторов
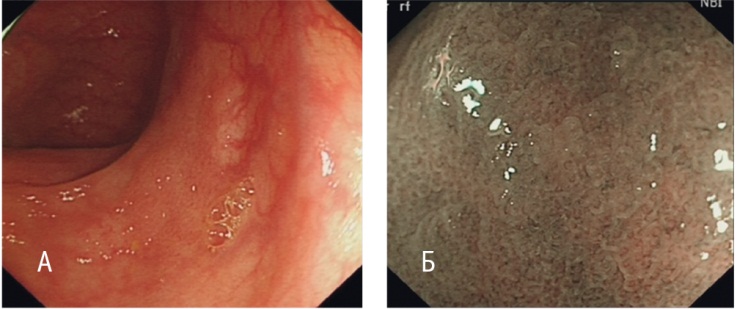
Осмотр SSA/P 1-го типа в режиме NBI с увеличением выявляет следующие особенности:
- структура ямок: 1-й тип по классификации NICE. Даже при отсутствии хромоскопии во время исследования можно различить выраженно дилатированные устья крипт, подобные изменения классифицируются как тип II-O (open-shape), впервые описанный T. Kimura и соавт. [7];
- капиллярный рисунок не расширенный, регулярный, сетчатого типа, вокруг ямок. Расширенные изолированные разветвленные сосуды по типу «морских звезд» (см. рис. 4).
- белесость поверхности;
- мелкодисперсная регулярная структура;
- структура ямок: 1-й тип по классификации NICE;
- капиллярный рисунок в виде коротких расширенных петель по краю белых структур крипт (см. рис. 5).
- наличие зубчатости цитоплазматического типа;
- расширение базальных отделов крипт вдоль мышечной пластинки слизистой оболочки.
Рис. 6. Зубчатая аденома/полип на широком основании. Окраска гематоксилином и эозином, об. × 10. Фото авторов.
Зубчатость цитоплазматического типа распространяется на все протяжение крипт (пилообразный просвет), базальные отделы трех крипт расширены
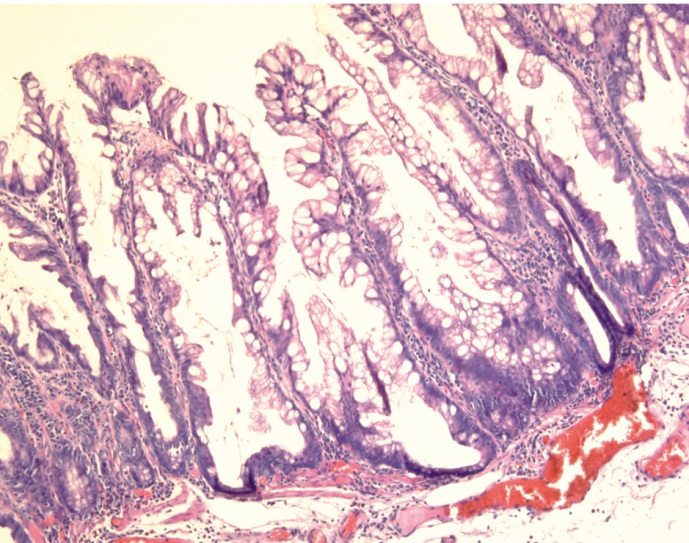
Для SSA/P характерно также расширение зоны зубчатости на нижнюю половину крипт, вплоть до базальных отделов.
В концепции зубчатого пути канцерогенеза появление в SSA/P очагов дисплазии определяется как пусковой механизм малигнизации [2, 18]. Поэтому важным моментом является возможность их идентификации во время эндоскопического исследования.
Вопрос о достоверных эндоскопических признаках дисплазии в SSA/Р остается нерешенным. В то время как наличие участков дисплазии тяжелой степени характеризуется такими очаговыми изменениями, как депрессия слизистой, гиперемия, неравномерность структуры, усиление и нерегулярность капиллярного рисунка, участки дисплазии слабой степени не имеют четких дифференциальных признаков (рис. 7).
Рис. 7. Зубчатая аденома/полип на широком основании с дисплазией слабой степени. А — режим белого света; Б — режим NBI c увеличением. Фото авторов.
Слизистая по цвету не отличается от окружающей; поверхность белесая; структура регулярная, 1-й тип по классификации NICE; капиллярный рисунок регулярный, сетчатый, вокруг крипт, без выраженного расширения
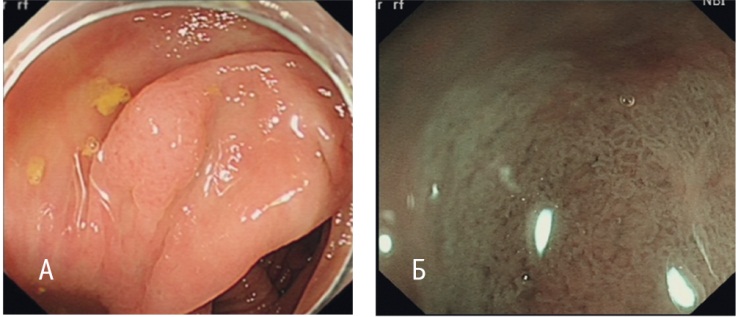
Наличие очагов дисплазии в SSA/P необходимо отражать в заключении, так как появление дисплазии в SSA/P является критическим событием в зубчатом пути канцерогенеза, после которого малигнизация происходит быстрыми темпами, сопоставимыми со скоростью малигнизации при синдроме Линча [4, 10, 11, 15]. Дисплазия в SSA/P не имеет особенных черт и характеризуется утратой специфической секреторной функции (отсутствием или резким снижением числа секреторных вакуолей), укрупнением, полиморфизмом и гиперхромией ядер, нарушением распределения хроматина, что проявляется неравномерностью окрашивания ядер, появлением стратификации ядер, увеличением митотической активности (рис. 8). Дисплазия в SSA/P нередко носит очаговый характер и обнаруживается в базальных отделах крипт, не проявляясь изменениями поверхностного рельефа слизистой оболочки, это лишает ее характерных эндоскопических черт.
Рис. 8. Зубчатая аденома/полип на широком основании. Окраска гематоксилином и эозином, об. × 20. Фото авторов.
Представлены базальные отделы крипт, в части из них видна зубчатость цитоплазматического типа (звездчатый просвет), в ряде крипт отмечаются признаки дисплазии слабой степени
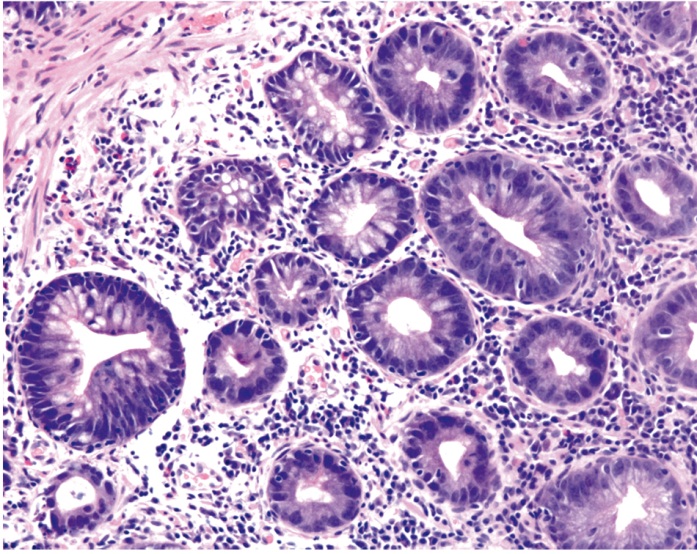
TSA занимает особое положение, как макроскопически, так и микроскопически отличаясь от HP и SSA/P. Типичные эндоскопические проявления TSA:
- левостороннее поражение;
- полиповидная форма типов 0-Is, 0-Ips, 0-Ip [17];
- красный цвет слизистой;
- ворсинчатая поверхность;
- структура с удлиненными расширенными и разветвленными криптами 2-го типа по классификации NICE;
- капиллярный рисунок расширенный, коричневого цвета при осмотре в режиме NBI.
Рис. 9. Традиционная зубчатая аденома. Режим NBI c увеличением. Фото авторов
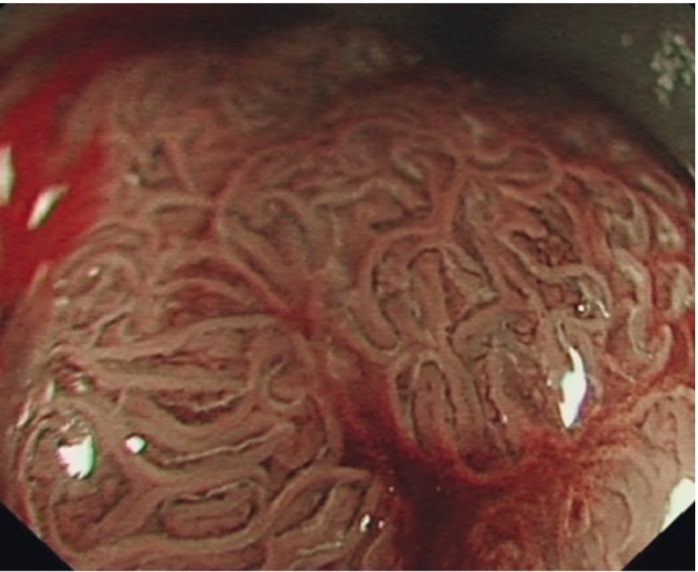
Рис. 10. Тубулярно-ворсинчатая аденома. Режим NBI c увеличением. Фото авторов
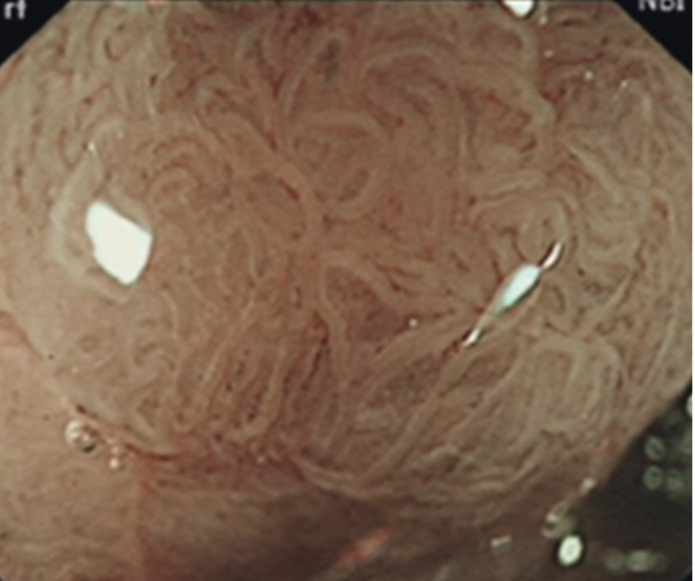
Единственным эндоскопическим отличительным критерием TSA является наличие неровной, зубчатой формы края крипт (тип IVH). Но определить его возможно только при осмотре образования с одновременным применением режимов NBI, увеличения и хромоскопии (рис. 11).
Рис. 11. Традиционная зубчатая аденома. Режим NBI с увеличением и хромоскопией с использованием генциана фиолетового [16]. Зубчатый контур крипт, тип IVH
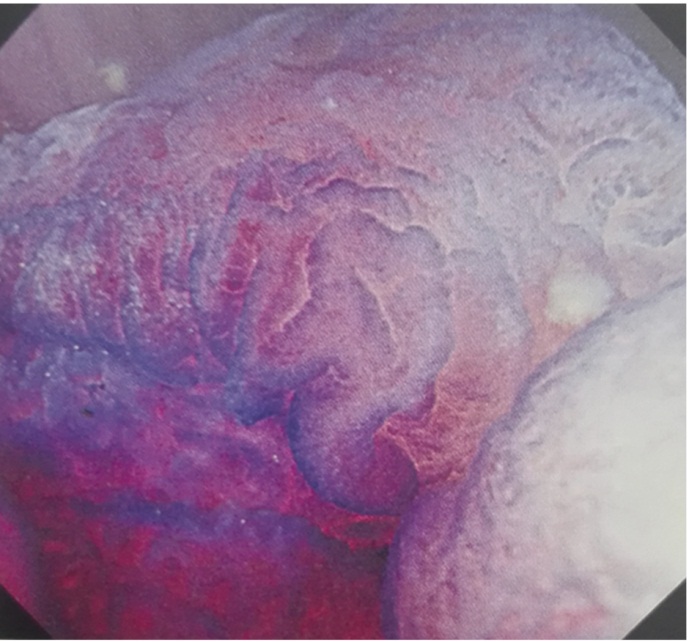
Достоверным морфологическим критерием TSA считается наличие эктопических крипт, которые отходят от основной крипты перпендикулярно продольной оси в толщу слизистой оболочки, не достигают мышечной пластинки слизистой оболочки и придают TSA зубчатость (рис. 12). Проиллюстрированный H. Tajiri и соавт. [16] зубчатый контур крипт, выявляемый при проведении эндоскопического исследования в режиме NBI с увеличением при окрашивании in vivo, вероятно, позволяет различить поверхностно расположенные эктопические крипты.
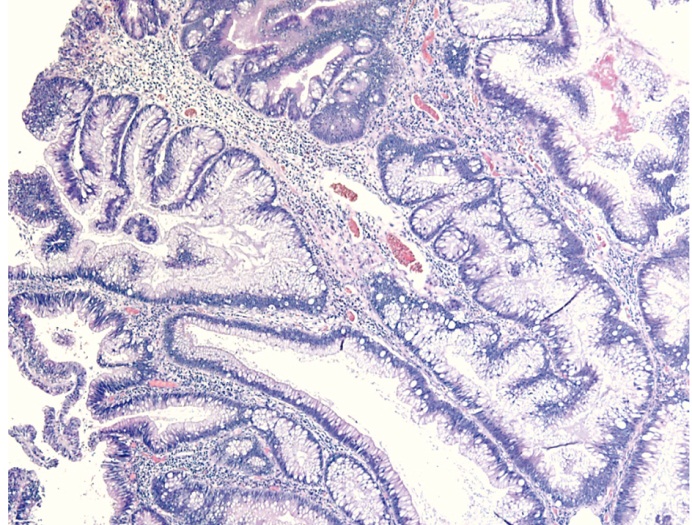
Рис. 12. Традиционная зубчатая аденома. Окраска гематоксилином и эозином, об. × 10. Фото авторов.
Зубчатость обусловлена наличием эктопических крипт
Однако остается неопределенность по ряду вопросов:
- отсутствуют точные морфометрические характеристики эктопических крипт (размер, длина, количество в одной крипте), что позволило бы отличать эктопические крипты от ветвления и почкования — феноменов, фиксируемых в тубулярных, тубуло-ворсинчатых и ворсинчатых аденомах;
- не установлено положение в классификации тубуло-ворсинчатых и ворсинчатых образований, в которых эктопические крипты единичны или фиксируются на ограниченном участке.
В практической работе нередко встречается полное или частичное несоответствие зубчатых образований толстой кишки описанным критериям.
Случай 1. При эндоскопическом исследовании в восходящем отделе толстой кишки определено плоско-возвышенное образование типа 0-IIа размером до 8 мм, с «муцинозной шапкой», по цвету не отличавшееся от окружающей слизистой, с мелкозернистой поверхностью, фестончатыми краями; структура ямок соответствовала 1-му типу по классификации NICE, с умеренно расширенными устьями крипт, близкими к типу II-O; капиллярный рисунок был регулярным, без усиления, но с наличием изолированных расширенных разветвленных сосудов. По эндоскопическим критериям образование расценено как SSA/Р (рис. 13).
Рис. 13. Случай 1. Гиперпластический полип. А — режим белого света; Б — режим NBI c увеличением. Фото авторов
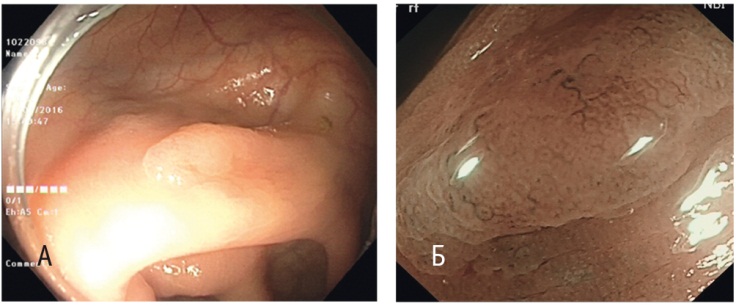
Рис. 14. Случай 1. Гиперпластический полип. Окраска гематоксилином и эозином, об. × 10. Фото авторов.
Зубчатость цитоплазматического типа (в части крипт просвет пилообразный, в части — звездчатый), базальные отделы крипт не расширены, дисплазия отсутствует
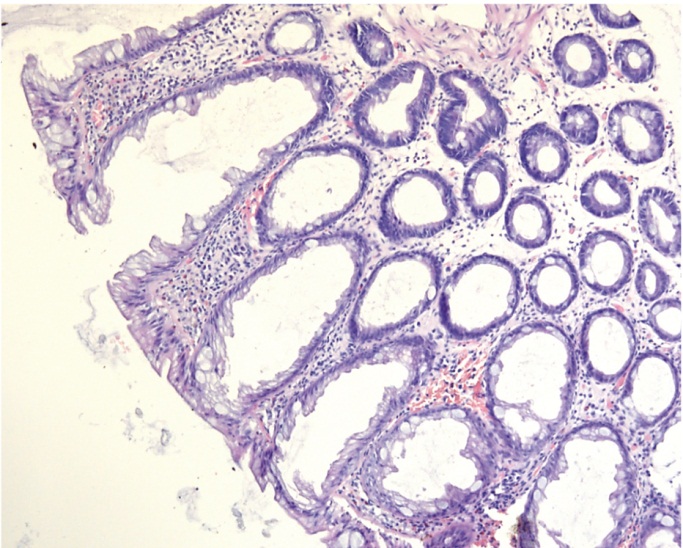
Микроскопически все формальные морфологические критерии соответствовали HP: зубчатость цитоплазматического типа, нерасширенные базальные отделы крипт, отсутствие дисплазии (рис. 14). Следует обратить внимание, что в данном образовании были расширены верхние отделы и устья крипт. Это не имело значения для диагноза, однако могло имитировать эндоскопическую картину крипт открытого типа II-O.
Случай 2. При эндоскопическом исследовании выявлено образование слизистой восходящей кишки в области баугиниевой заслонки типа 0-IIа размером до 7 мм, с «муцинозной шапкой», по цвету не отличавшееся от окружающей слизистой, с мелкозернистой поверхностью, фестончатыми краями; структура ямок соответствовала типу 1-2 по классификации NICE; капиллярный рисунок был расширенным, с коричневым оттенком при NBI. По эндоскопическим критериям образование расценено как классическая аденома (рис. 15).
Рис. 15. Случай 2. Гиперпластический полип. А — режим белого света; Б — режим NBI с увеличением. Фото авторов
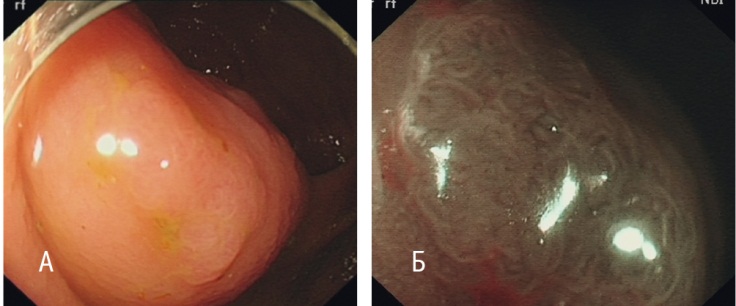
Микроскопически образование соответствовало HP. Нетипичным в данном случае являлось выраженное расширение поверхностных отделов крипт, что создавало картину выступов и углублений на поверхности слизистой оболочки и затрудняло эндоскопическое определение типа образования (рис. 16).
Рис. 16. Случай 2. Гиперпластический полип. Окраска гематоксилином и эозином, об. × 10. Фото авторов.
Зубчатость цитоплазматического типа, базальные отделы крипт не расширены, дисплазия отсутствует
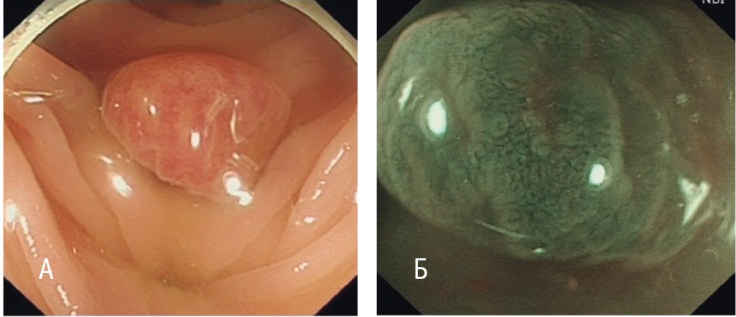
Случай 3. При эндоскопическом исследовании в сигмовидном отделе выявлено полиповидное образование размером до 9 мм, типа 0-Is, с гладкой поверхностью, красного цвета, с ровными краями; структура относилась к 1-му типу по классификации NICE; капиллярный рисунок был резко усиленным. По эндоскопическим признакам образование расценено как тубулярная аденома с признаками воспаления или воспалительный полип (рис. 17).
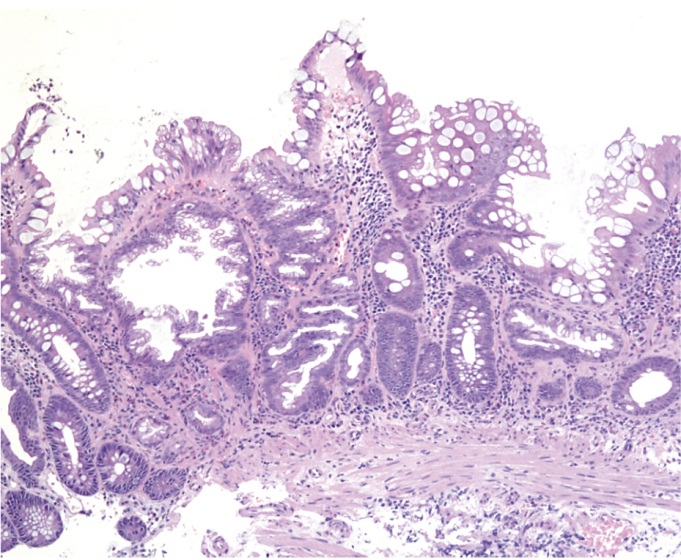
Рис. 17. Случай 3. Зубчатая аденома/полип на широком основании. А — режим белого света; Б — режим NBI с увеличением. Фото авторов
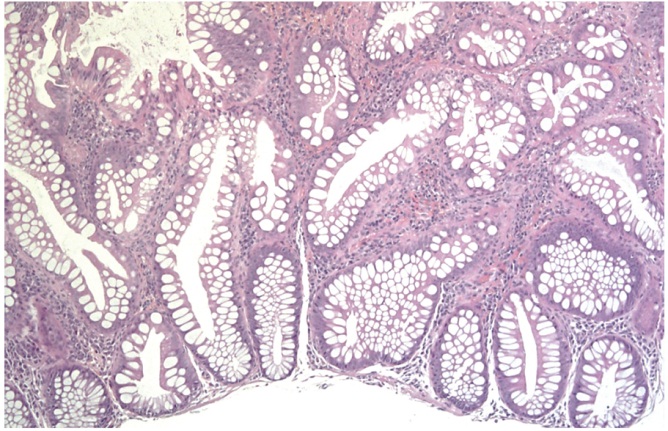
Микроскопически по формальным морфологическим критериям образование соответствовало SSA/P (рис. 18). Однако в связи с обилием бокаловидных клеток зубчатость была выражена в слабой степени и определялась не во всех полях зрения. Сочетание этих факторов, вероятно, затруднило эндоскопическую диагностику.
Рис. 18. Случай 3. Зубчатая аденома/полип на широком основании. Окраска гематоксилином и эозином, об. × 10. Фото авторов.
Зубчатость цитоплазматического типа (звездчатый просвет крипт в правом верхнем квадранте), расширение базальных отделов двух крипт вдоль мышечной пластинки слизистой оболочки, дисплазия отсутствует, обилие бокаловидных клеток
ЗАКЛЮЧЕНИЕ
Зубчатые образования определяются как этап развития рака толстой кишки, поэтому в целях профилактики колоректального рака рекомендованы их выявление и удаление.
Активное изучение зубчатых образований позволило разработать специфические методы эндоскопической визуализации и описать ряд их эндоскопических признаков. Однако нередко на основании одних только эндоскопических признаков не удается четко определить тип образования. В связи с этим остается необходимым морфологический контроль выявляемых в толстой кишке образований.
Для полноценной диагностики зубчатых образований необходима дальнейшая совместная работа по сопоставлению их морфологических и эндоскопических характеристик.







