В последние десятилетия, по данным литературы, отмечается рост числа пациентов с диффузными заболеваниями печени (ДЗП) [3, 6, 13, 14]. В основном они продолжают поступать в стационары только при развитии осложнений, наиболее частым из которых является портальная гипертензия. Кроме того, сохраняется неуклонное увеличение численности больных циррозом печени. Одной из главных целей и важнейшим компонентом диагностических мероприятий является ранняя и своевременная диагностика прогрессирования фиброзного процесса в паренхиме печени [1, 4, 7, 11-15]. Активное внедрение инструментальных методов инвазивной и неинвазивной диагностики фиброзного процесса в печени в клиническую практику позволяет эффективно сочетать диагностические мероприятия, направленные в первую очередь на раннюю диагностику [2, 7, 8, 11, 13-15].
Печень является мультисекторным и мультисегментарным органом; разделение печени на сегменты необходимо не только для четкой локализации очаговых изменений в ее ткани, но и для оценки развития фиброзного процесса в ней, который с точки зрения патолого-анатомического процесса развивается неравномерно [2-5, 8, 13]. С учетом того что границами секторов и сегментов печени являются малососудистые участки, где нет анастомозов между желчными протоками, а сосудистые анастомозы малочисленны, возможности эластографических методов расширяются в связи с отсутствием артефактов. Если говорить о сегментах печени, то, являясь пирамидальными участками, группируясь, они образуют анатомические сектора, каждый из которых требует к себе определенного внимания и логистического подхода.
Определенными преимуществами в ранней диагностике фиброзного процесса обладают неинвазивные методы исследования [11]. В последние годы все шире применяются эластографические методы [11-15]. Своевременная диагностика ДЗП и последующий выбор рациональной лечебной тактики у таких больных остаются сложными и во многом нерешенными проблемами. В этой связи особую актуальность приобретают эластографические методы исследования, особенно важно внедрение их комплексного применения.
Цель исследования: изучить вопросы выбора методов диагностики в комплексном эластографическом обследовании пациентов, страдающих ДЗП.
МАТЕРИАЛЫ И МЕТОДЫ
В составе основной группы в исследовании приняли участие 124 человека с ДЗП: 99 (79,8%) мужчин и 25 (20,2%) женщин (табл. 1). Группы были рандомизированы по полу, возрасту и фоновой патологии. Больные стеатозом были отнесены к первой подгруппе, гепатитом — ко второй, циррозом — к третьей. Кроме того, с целью оценки значений жесткости паренхимы печени у здоровых лиц по сегментам для разработки схем эластографического обследования была набрана контрольная группа, в которую вошли 58 человек, не страдавших ДЗП.
Таблица 1
Распределение больных основной группы по полу и возрасту в зависимости от клинических форм диффузных заболеваний печени
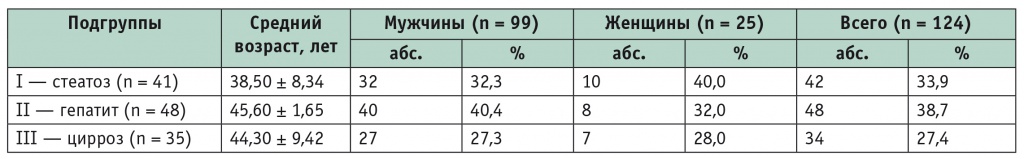
Примечание. Различия между подгруппами по всем параметрам не имеют статистической значимости: p ≥ 0,05.
Статистически значимых различий по гендерному составу между подгруппами пациентов с разными клиническими формами ДЗП не получено (критерий χ2, p ≥ 0,05). Медиана (интерквартильный размах) возраста в основной группе — 43 года (38-46), в контрольной — 45 лет (39-49) (p = 0,81).
Референтным методом служила биопсия печени, которая проводилась 61 исследуемому (49,2%) после предварительного подписания информированного согласия. Для подтверждения клинического диагноза ДЗП анализу подвергались данные лабораторных (общий анализ крови, биохимический анализ крови) и инструментальных методов исследования (УЗИ органов брюшной полости, эзофагогастродуоденоскопия).
При анализе структуры соматической патологии в исследуемых группах (в контрольной группе это было необходимо с целью исключения заболеваний, приводящих к развитию фиброзного процесса в паренхиме печени) установлено, что в обеих группах часто регистрировались заболевания ЖКТ: язвенная болезнь желудка и/или двенадцатиперстной кишки, хронический гастрит, хронический панкреатит, хронический холецистит. У 51 пациента (41,1%) основной группы регистрировались заболевания со стороны сердечно-сосудистой и дыхательной систем.
С целью стандартизации алгоритма комплексного эластографического обследования паренхимы печени на первом этапе проводилось ее сегментарное обследование у пациентов контрольной группы (n = 53), а затем основной группы (n = 119). Для определения стадии фиброзного процесса в паренхиме печени на основании данных, полученных в контрольной группе, выполнялось комплексное эластографическое обследование пациентов с ДЗП. Всем обследуемым делали УЗИ печени в В-режиме и в режиме цветного допплеровского картирования. Транзиентную эластографию проводили на аппарате FibroScan (Echosens, Франция); компрессионную эластографию — на аппарате Hitachi Preirus (Hitachi, Япония); для эластографии сдвиговых волн применяли цифровую ультразвуковую портативную систему «АНГИОДИН-Соно/П-Ультра» (НПФ «БИОСС», Россия); компрессионную эластографию при эндоскопической ультрасонографии (эндосонографии) выполняли при помощи аппаратов PENTAX EG 387OUTK (Pentax, Япония) и Hitachi Preirus. Задачей этих исследований являлась четкая топическая диагностика фиброзного процесса в печени с оценкой его распространенности, за основу было взято деление печени по сегментам (рис. 1). Путем последовательного проведения различных видов эластографии создавалось целостное представление об исследуемом органе.
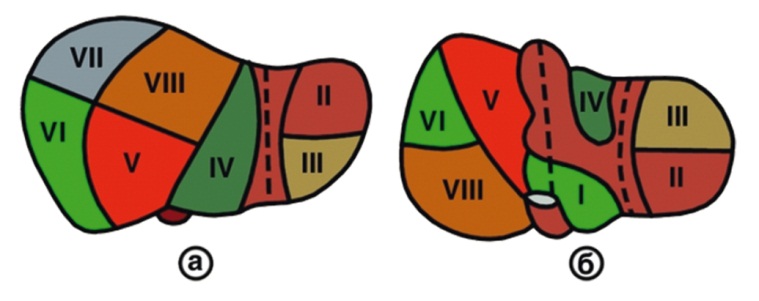
Рис. 1. Сегментарное строение печени: диафрагмальная (а) и висцеральная (б) поверхности [10].
Примечание. Римскими цифрами обозначены номера сегментов
Транскутанное эластографическое обследование проводили пациенту на твердой ровной поверхности в положении лежа. При транзиентной эластометрии трансдуцер датчика устанавливался перпендикулярно межреберью, результат выражался в килопаскалях (кПа) (рис. 2); при компрессионной — ось линейного датчика была направлена к оси сердца (с целью получения толчкообразных движений), результат выражался в индексе фиброза (LF) (рис. 3); в ходе эластографии сдвиговых волн конвексным датчиком создавалось «акустическое окно» при последующем получении окраса «зоны интереса» паренхимы печени, результат выражался в кПа и метрах в секунду (м/с) (рис. 4); в процессе компрессионной эластографии при эндоскопической ультрасонографии (эндосонографии) направление сканирования конвексного датчика совпадало с осью эндоскопа, требовался плотный контакт всей его рабочей поверхности с «зоной интереса», длительность устойчивого контакта составляла не менее 3-5 секунд, результат определялся при помощи расчета коэффициента разницы (SR) и выражался в условных единицах (у. е.) (рис. 5). Для стабилизации эластографической картины при эндосонографии целесообразно проведение седации и/или вводного наркоза до и во время исследования: при невозможности или отсутствии данных условий увеличивается активность пациента, значительно искажающая полученные данные.
Рис. 2. Методика проведения транзиентной эластографии печени.
Примечание. 1 — эластографический датчик; 2 — паренхима печени (зона 60 × 10 мм)
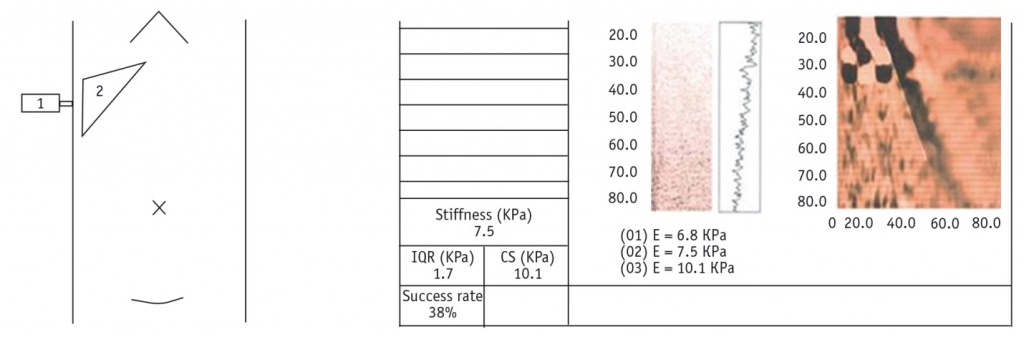
Рис. 3. Методика проведения компрессионной эластографии печени.
Примечание. 1 — эластографический датчик; 2 — паренхима печени; 3 — зона исследования 35 × 25 мм; 4 — сокращение сердечной мышцы
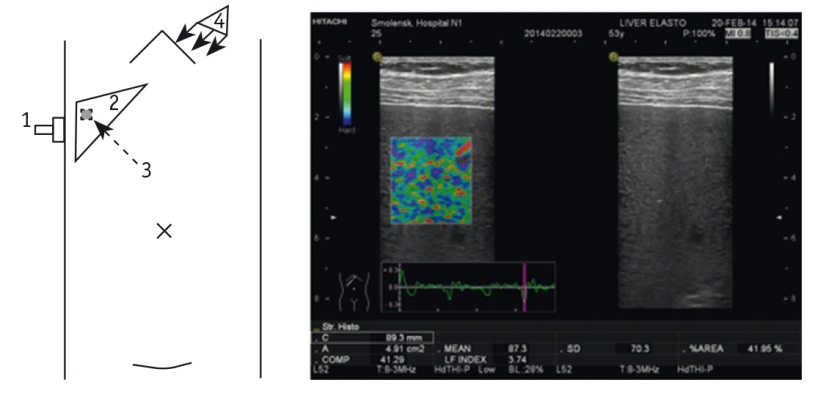
Рис. 4. Методика проведения эластографии сдвиговых волн печени.
Примечание. 1 — эластографический датчик; 2 — паренхима печени; 3 — зона исследования от 30 до 80 мм
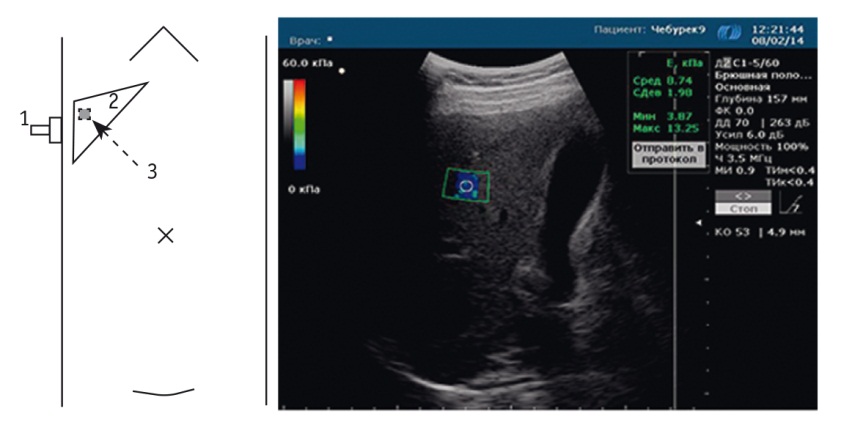
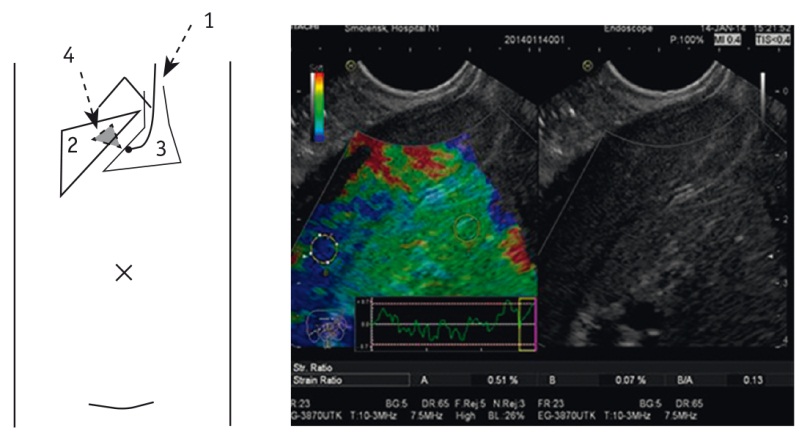
Рис. 5. Методика проведения компрессионной эластографии печени при эндосонографии.
Примечание. 1 — эхоэндоскоп с ультразвуковым датчиком на конце; 2 — паренхима печени; 3 — желудок; 4 — зона исследования паренхимы печени
Сравнение средних величин показателей в основной и контрольной группах проводили с применением непараметрических и параметрических критериев. Анализ данных осуществляли с помощью статистической программы SPSS 17.0. С целью определения пригодности выбранной модели алгоритма для прогнозирования рассчитывали площадь под кривой (area under curve — AUC) ROC (receiver operating characteristic) и соответствующий 95%-й ДИ. Оценивали чувствительность, специфичность и точность выбранной модели обследования. Различия между средними значениями показателей анализировали с использованием величин стандартного отклонения и считали статистически значимыми при p ≤ 0,05 (критерий Стьюдента).
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Для комплексного эластографического обследования нами использовался принцип мультисекторности и мультисегментарности печени. Проводили анализ возможных результатов эластографических показателей по сегментам печени в контрольной группе, за исключением VIII сегмента (табл. 2). Выполнение исследования в VIII сегменте было невозможно вследствие анатомических особенностей и технических ограничений эластографических методик. Результаты комплексного эластографического обследования позволили установить значения жесткости паренхимы в группе здоровых лиц.
Таблица 2
Результаты комплексного эластографического обследования сегментов печени у здоровых лиц
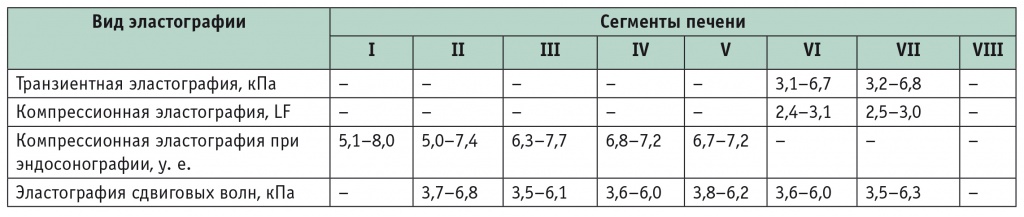
Примечание. Прочерки означают невозможность исследовать сегмент данным методом.
Далее комплексное эластографическое обследование проводилось пациентам с ДЗП (табл. 3).
Таблица 3
Результаты комплексного эластографического обследования пациентов с диффузными заболеваниями печени
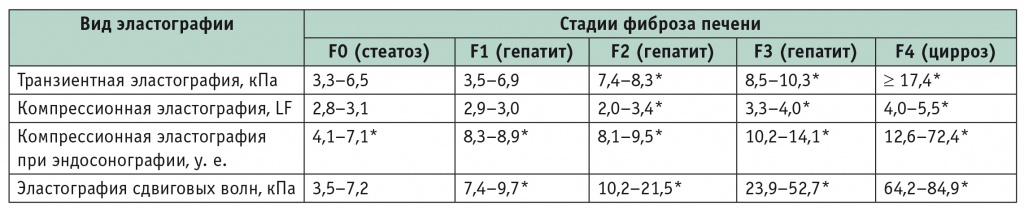
* Различия с контролем статистически значимы: p ≤ 0,05.
Представленные данные свидетельствуют о наличии статистически значимых различий между показателями основной и контрольной групп при комплексном эластографическом обследовании (p ≤ 0,05) и об отсутствии различий в результатах эластометрии у пациентов со стеатозом и здоровых лиц (p > 0,05).
Внутри комплексного алгоритма эластографического обследования имеется элемент взаимозаменяемости, который помогает врачу корректировать алгоритм обследования пациентов, не применяя тот или иной эластографический метод, а также предусмотрена способность расширять алгоритм обследования за счет параллельного проведения дополнительного исследования (например, компрессионной эластографии при эндосонографии, компрессионной эластографии или эластографии сдвиговых волн при УЗИ печени).
На втором этапе исследования определялись чувствительность, специфичность и точность эластографических методов (табл. 4). Проводилась оценка площади под ROC-кривой (AUC) для всех видов эластографических методик (табл. 5).
Таблица 4
Диагностическая значимость эластографических методов, %
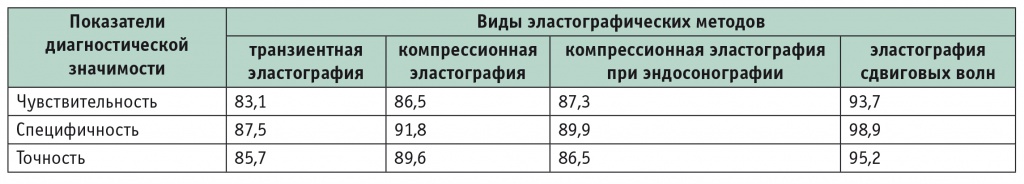
Таблица 5
Площадь под ROC-кривой (AUC)
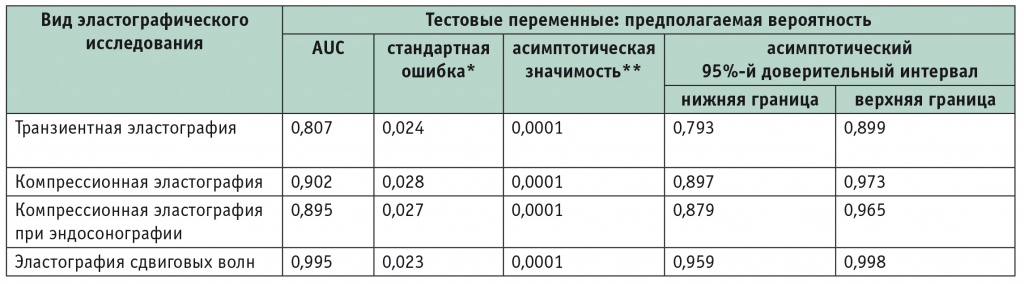
* В непараметрическом случае.
** Истинная площадь.
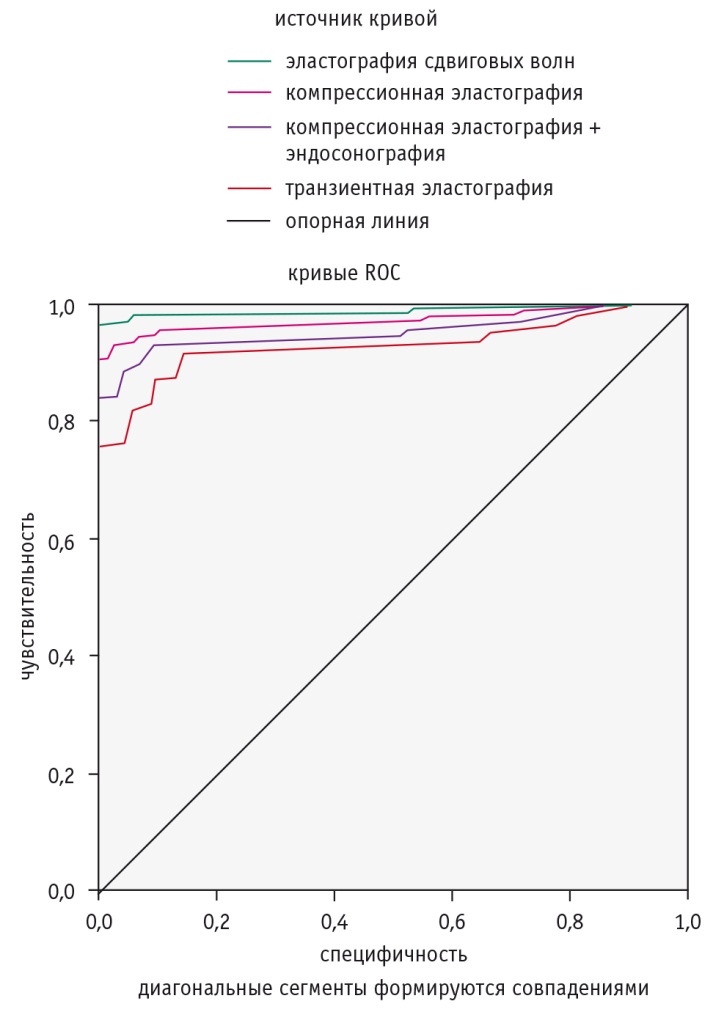
По результатам анализа данных комплексного эластографического обследования при различных комбинациях методов эластографии специфичность составила 98,9%, чувствительность — 95,1%, точность — 96,9%. ROC-кривые представлены на рисунке 6. AUC статистически значимо отличалась от 0,5 (p = 0,0001).
Рис. 6. ROC-кривая для диагностической и прогностической ценности эластографических методик
Таким образом, эта модель логистической регрессии пригодна для оценки значимости комплексного эластографического обследования.
ЗАКЛЮЧЕНИЕ
Результаты эластографических исследований сегментов печени у здоровых лиц позволили стандартизировать эластометрические показатели у пациентов с различными клиническими формами диффузных заболеваний печени.
Комплексное эластографическое обследование дает возможность оценить все сегменты печени, что не всегда доступно при применении только одной методики.
Стандартизированные схемы проведения эластографических методов исследования позволяют комбинировать методы инструментальной диагностики, модифицировать алгоритм обследования пациентов, взаимозаменять методы эластографии.
Анализ данных комплексного эластографического обследования при различных комбинациях методов эластографии выявил специфичность 98,9%, чувствительность 95,1%, точность 96,9%.







