Эпидемиологические данные ВОЗ показывают, что в мире наблюдается тенденция к увеличению количества больных сахарным диабетом (СД) [1]. Панкреатогенный диабет, так называемый сахарный диабет 3с-типа (СД3с), связан с заболеваниями поджелудочной железы (ПЖ) и развивается при хроническом панкреатите (ХП), муковисцидозе, раке ПЖ, как осложнение после резекционных операций на ПЖ [2, 3]. Развитие СД3с у больных ХП значительно ухудшает прогноз заболевания [4]. Существует прямая корреляция между выявлением СД3с и заболеваниями ПЖ [5]. Кроме того, имеется мировая тенденция к увеличению количества случаев как ХП, так и СД3с, что, во-первых, связывают с факторами образа жизни, а во-вторых — с улучшением методов диагностики [5]. В настоящее время СД3с составляет 10% среди других случаев диабета [6, 7].
Превентивная индивидуализированная диагностика — актуальная биомедицинская, научно-практическая задача с фундаментальным основанием для разработки, создания и изучения новых фармакологических препаратов. В качестве одного из методов предложено изучение регуляторов инкретиновых сигнальных путей [8, 9]. В частности, показана антидиабетическая активность GIP, GLP-1 и панкреатического полипептида [10].
Диагностические критерии СД3с: наличие экзокринной панкреатической недостаточности; изменения, соответствующие признакам ХП, по результатам МСКТ, МРТ, эндо-УЗИ. Дополнительными диагностическими критериями СД3с, отличающими его от СД 2 типа, являются снижение секреции С-пептида и отсутствие инсулиновой резистентности. Ранняя дифференциальная диагностика СД3с достаточно сложна, поэтому в клинической практике СД3с часто ошибочно относят к СД 2 типа. СД3с рассматривается как заболевание, возникающее вследствие патологии экзокринной части ПЖ, имеющее свои механизмы реализации патофизиологического процесса [10–12]. Для дифференциальной диагностики СД3с и СД 1 типа определяют наличие и/или отсутствие антител к клеткам ПЖ, глутаматдекарбоксилазе и инсулину [13].
Наиболее простым и доступным методом на сегодняшний день остается определение гликемии. Преимущество этого метода связано с эссенциальной функцией глюкозы как важнейшего компонента энергетического обмена клеток, главным образом клеток мозга. Последние данные литературы говорят о тесной связи процесса пищеварения, и в том числе функций ПЖ, с состоянием и функционированием ЦНС [14–16]. Несмотря на то что патофизиологическая теория нервизма сдает свои научные позиции, классические результаты исследования процессов пищеварения демонстрируют, что согласованная деятельность ЦНС, ПЖ, кишечника является залогом здорового пищеварения и сохранения гомеостаза обмена углеводов [14–16]. Таким образом, данные исследований внешнесекреторной функции ПЖ, состояния энтероинсулярной оси при заболеваниях ПЖ предоставляют новые возможности для выявления патогенетических механизмов развития СД3с.
Существуют морфологические особенности ПЖ. Так, выявленная тесная взаимосвязь между островками и ацинусами и развитая капиллярная сеть обеспечивают взаимное синергичное влияние экзо- и эндокринной ткани ПЖ [17–19]. Развитие экзокринной недостаточности у больных приводит к мальдигестии и мальабсорбции, нарушению секреции гастроинтестинальных гормонов [18, 20, 21].
Анатомо-морфологические изменения ПЖ, возникающие вследствие циклически рецидивирующего воспаления, приводят к разрушению ткани ПЖ с постепенной потерей β-клеток (нарушением синтеза инсулина), α-клеток (нарушением синтеза глюкагона и его транспорта в кровоток), δ-клеток (изменением синтеза и поступления в местную капиллярную систему соматостатина, отсутствием замыкания оси «ЦНС — кишечник») [22] и PP-клеток (нарушением синтеза и доступности панкреатического полипептида для тканей органа и соседних систем: печени, желчного пузыря, двенадцатиперстной кишки) [23–25]. В сочетании вышеназванные нарушения могут привести к нестабильному течению диабета, который характеризуется резкими колебаниями уровня глюкозы в крови, вызывая гипер- или гипогликемию [26].
Цель исследования: поиск диагностических и прогностических индивидуализированных предиктивных биомаркеров панкреатогенного сахарного диабета в лабораторной диагностике и/или в сочетании с данными клинических исследований.
МАТЕРИАЛЫ И МЕТОДЫ
В исследование были включены 152 пациента в возрасте от 24 до 66 лет, проходивших обследование и лечение в ГБУЗ МКНЦ им. А. С. Логинова ДЗМ в 2015–2017 гг.; из них мужчин — 97, женщин — 55. Критерии включения: средняя длительность заболевания ХП не менее 5 лет (минимум 4, максимум 14 лет), отсутствие ожирения. Клинический диагноз ХП подтвержден инструментальными и лабораторными методами; методом ELISА определяли концентрацию холецистокинина (ХЦК), секретина в сыворотке крови, панкреатической эластазы-1 в кале. Уровень С-пептида устанавливали иммунохемилюминесцентным методом.
Все больные в зависимости от уровня гликемии натощак были разделены на две группы: в 1-ю группу вошли больные с уровнем глюкозы ≥ 5,7 ммоль/л (73 пациента, мужчины/женщины — 49/24) и развернутой клинической картиной СД3с у 34 больных; во 2-ю группу вошли пациенты с концентрацией глюкозы < 5,7 ммоль/л (79 пациентов, мужчины/женщины — 48/31), латентный СД3с выявлен у 4 из них. Концентрация глюкозы крови измерялась в сыворотке венозной крови утром, натощак, рутинным биохимическим методом в условиях закрытой системы Olympus. Характеристика обследованных больных представлена в таблице.
Таблица
Характеристика больных в зависимости от уровня гликемии натощак
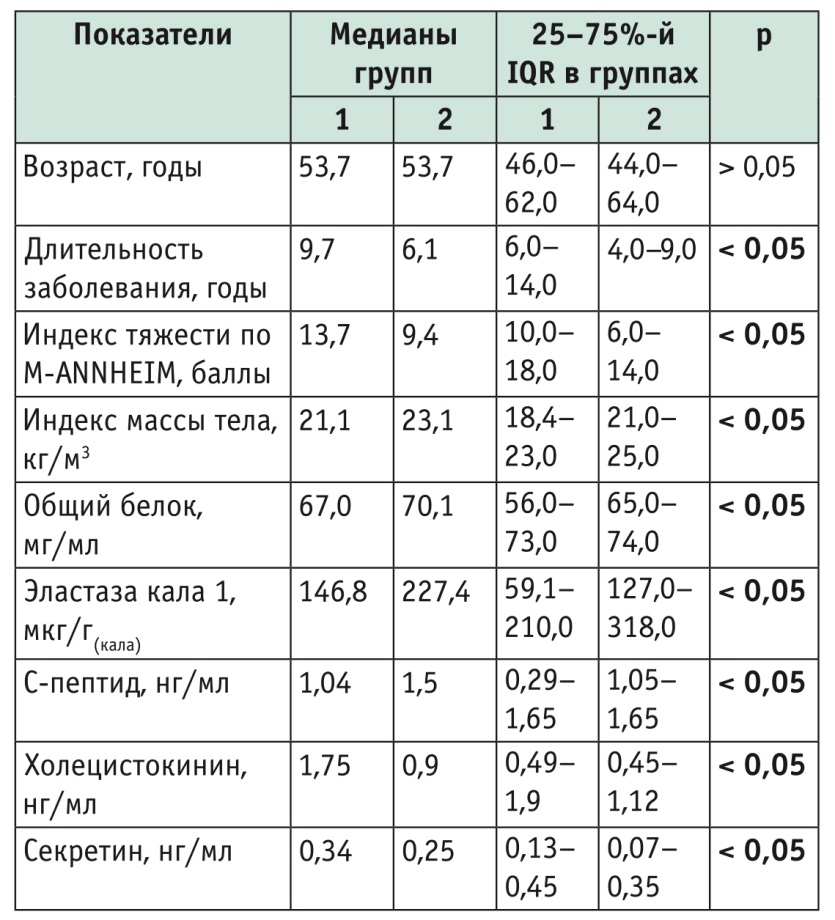
Примечание. IQR — интерквартильный размах.
Статистическая обработка результатов была проведена после определения характера распределения полученных числовых данных при помощи пакета прикладных программ Statistica 6.0 и в программе R. Все численные данные представлены как mean ± SD или медиана (M) c 25–75%-м интерквартильным размахом (IQR). Статистическую значимость различий одноименных количественных показателей между группами определяли при помощи непарного критерия Манна — Уитни (U-тест); качественные различия между группами оценивали при помощи точного теста Фишера. Различия считались статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
При анализе полученных результатов следует отметить, что в 1-й группе выявлено 36 больных с хроническим кальцифицирующим панкреатитом (ХКП), панкреато-дуоденальная резекция (ПДР) была проведена 28, дистальная резекция (ДР) ПЖ — 7 больным. Во 2-й группе больных ХП выявлено 18 пациентов с ХКП, ПДР проведена 17, а ДР — 12 больным. Количество больных с выявленным кальцинозом ПЖ в группе с повышенной концентрацией глюкозы было в 2 раза больше, что согласуется с данными литературы [27]. Относительный риск развития СД колеблется от 3,2 (у послеоперационных пациентов) [28] до 7,7 (при идиопатическом ХП). В когорте из 418 пациентов с наследственным панкреатитом, наблюдавшихся в 14 странах мира, прослеживался четкий линейный кумулятивный риск эндокринной недостаточности — от 1,3% в возрасте 10 лет до 79,1% в возрасте 80 лет. Риск СД составил 50% через 10 лет и возрастал до 83% через 25 лет [28].
По возрасту и количеству обследованных больных группы были сопоставимы (см. табл.). Из данных таблицы 1 видно, что длительность ХП в этих группах статистически значимо различается: в 1-й группе медиана составила 9,7 года, в то время как в группе 2 — 6,1 года. В нашем исследовании индекс тяжести ХП по M-ANNHEIM также был статистически значимо выше для 1-й группы, чем для 2-й; длительность процесса рецидивирующей воспалительной деструкции ПЖ приводит к ухудшению состояния больных, что согласуется с данными литературы [18].
Медианные значения ИМТ составили для 1-й группы 21,1 кг/м2, для 2-й — 23,1 кг/м2. Эти различия были статистически значимыми и свидетельствуют о том, что существует вероятность выявления метаболических нарушений обмена белка у этих больных вне зависимости от группы наблюдения. При снижении внешнесекреторной функции ПЖ развивается мальнутриция. Этот синдром складывается из синдрома нарушения переваривания (мальдигестии) и синдрома снижения всасывания (мальабсорбции). Синдром мальнутриции подразумевает широкий спектр трофологических нарушений, которые развиваются вследствие белковой, витаминной недостаточности, изменений жирового, углеводного, минерального обмена [2]. Нами была исследована концентрация общего белка в крови. Показано, что в группах 1 и 2 существуют статистически значимые различия по этому показателю (р < 0,05). Медианное значение общего белка в группе 1 составило 67,0 мг/мл, в то время как в группе 2 — 70,1 мг/мл. При анализе данных также было установлено, что в обеих группах присутствуют больные как со сниженной концентрацией белка, так и с сохранной (в пределах референсных значений).
При исследовании экзокринной функции ПЖ, которая оценивалась по уровню панкреатической эластазы-1, выявлено статистически значимое снижение количества фермента в 1-й группе в сравнении со 2-й (см. табл.). Этот факт говорит в пользу теории волнообразного течения микронекротизации ткани ПЖ с последующим сокращением ферментпродуцирующей популяции клеток органа [26]. Для 1-й группы концентрация эластазы-1 составила 146,8, а для 2-й — 227,4 мкг/г(кала). Интересным фактом явились определенные параметры IQR: для 1-й группы он составил 59,1–210,0, а для 2-й — 127,0–318,0. Концентрация данного фермента не зависит от применяемых препаратов ферментозаместительной терапии, так как они содержат ксеногенные ферменты, которые не влияют на уровень панкреатической эластазы-1 человека. Этот факт является важным компонентом адекватной лабораторной диагностики и мониторинга течения заболеваний ЖКТ и препятствует гипердиагностике ХП даже в случае приема ферментативных препаратов.
При определении концентрации С-пептида было установлено его значимое снижение в 1-й группе, где медианное значение составило 1,04 нг/мл, в то время как во второй — 1,5 нг/мл. При этом параметры IQR были следующими: для 1-й группы — 0,29–1,65 нг/мл, для 2-й — 1,05–1,65 нг/мл. Таким образом, можно заключить, что в обследованной группе больных наиболее выраженными нарушениями стали сокращение количества β-клеток ПЖ и связанное с ним снижение функции секреции инсулина.
В настоящее время общепризнанной является тесная взаимосвязь между секретином и ХЦК, которые регулируют секреторную деятельность ПЖ. Кроме того, эти гормоны являются важными регуляторами гомеостаза глюкозы. Их действие связано с влиянием как на продукцию инсулина, так и на систему глюкагона [22]. Нами были определены концентрации ХЦК и секретина и выявлено статистически значимое различие исследуемых групп: в 1-й группе концентрация ХЦК составила 1,75 нг/мл, а во 2-й — 0,9 нг/мл, секретина — 0,34 нг/мл и 0,25 нг/мл соответственно.
Поскольку нарушение обмена глюкозы при ХП является сложной проблемой, изучение перспективных диагностических и прогностических биомаркеров СД3с как изолированного патофизиологического процесса, связанного с хроническим воспалением ПЖ, необходимо для разработки новых подходов в профилактике СД3с и его осложнений.
Изучение сложных механизмов взаимодействия ХЦК, секретина, инсулина и глюкозы является актуальной задачей для современной гастроэнтерологии необходимо, в частности, для более глубокого понимания механизмов развития СД3с у больных ХП.
ЗАКЛЮЧЕНИЕ
Обнаруженное в нашем исследовании статистически значимое увеличение уровней холецистокинина и секретина можно связать с существованием возможного компенсаторного механизма, направленного на сохранение нормального уровня глюкозы крови и поддержание постоянства эффективного пластического белкового обмена. Учитывая, что при неблагоприятных условиях живые клетки организма стремятся сохранить эффективный энергообмен, инсулин и связанные с ним рецепторные механизмы могут быть рассмотрены в качестве ростовых факторов. Однако для того чтобы энергообмен позволял восстанавливаться ткани, необходимо полноценное снабжение белком клеток, способных к делению. В случае с хроническим панкреатитом этот процесс сложен физиологически по причине возникновения мальабсорбции и мальадгезии, развивающихся как результат нарушения экзокринной и эндокринной функций поджелудочной железы. Таким образом, хронический панкреатит может быть рассмотрен как серьезный фактор нарушения обоих типов обмена: пластического и энергетического. Это требует дальнейшего изучения более тонких механизмов регуляции обмена глюкозы при хроническом панкреатите.







