В последние годы в эндокринной хирургии наблюдается неуклонный рост количества оперативных вмешательств, которые выполняются при патологии надпочечников. Основной причиной данного явления стало широкое распространение инновационных методик топической и лабораторной диагностики, что позволило значительно повысить частоту выявления различных новообразований [12, 14]. Если 10 лет назад считалось, что новообразования адреналовых желез имеются примерно у 3,0% населения, то на сегодняшний день оценка распространенности надпочечниковых неоплазий значительно изменилась. Исследования, основанные на результатах лучевых методов диагностики и на данных аутопсий, продемонстрировали, что объемные образования коры надпочечников более 1,0 см в диаметре могут быть обнаружены у 7,0% населения. И несмотря на то, что не все такие образования подлежат хирургическому лечению, данная цифра заслуживает отдельного внимания. Новообразования мозгового слоя надпочечников встречаются реже: отмечают от 2 до 8 и более новых случаев на 1 000 000 населения в год. Среди пациентов, страдающих вторичной артериальной гипертензией, частота выявления феохромоцитомы достигает 0,6%. Кроме того, в соответствии с некоторыми работами, общая частота распространения объемных образований адреналовых желез достигает 8,7%. Следует также отметить, что эндокринные гипертензии надпочечникового генеза, по различным статистическим данным, обуславливают до 14,0% случаев всех симптоматических артериальных гипертензий [3, 5, 6, 17, 20].
Эндовидеохирургическая адреналэктомия представляет собой операцию выбора у пациентов с доброкачественными новообразованиями надпочечников. К настоящему моменту исследования четко продемонстрировали преимущества эндохирургического доступа над традиционным при выполнении адреналэктомии. В первую очередь, снижается частота возникновения осложнений, уменьшаются травматичность вмешательства и уровень послеоперационного болевого синдрома, а также длительность пребывания пациентов в стационаре. Кроме того, при эндовидеохирургической адреналэктомии отмечено снижение сроков реабилитации и послеоперационной нетрудоспособности [7, 11, 13, 15, 19, 22].
С ростом числа оперируемых в хирургии надпочечников все чаще стали проявляться относительно нестандартные ситуации, требующие отдельного подхода (крупные размеры новообразования; анатомические особенности взаиморасположения органов, приводящие к трудностям при первичной идентификации структур; плотное прилегание анатомических образований друг к другу). В подобных ситуациях у ряда хирургов возникают опасения, что при проведении эндохирургической адреналэктомии может повыситься частота осложнений. Необходимо отметить, что в целом осложнения при проведении эндовидеохирургических адреналэктомий возникают в 5-15% случаев; это значительно меньше, чем после открытых операций, но все еще является довольно высоким показателем [2, 9, 10, 23].
Одним из путей профилактики осложнений в хирургии надпочечников является применение методики трехмерного виртуального моделирования и последующей интраоперационной навигации, основанной на данных предоперационной диагностики (в первую очередь КТ и МРТ) [4, 16, 21]. Соответствующая методика в абдоминальной хирургии известна достаточно давно и продемонстрировала возможность уверенного снижения частоты осложнений. Однако широкого распространения виртуальное моделирование с последующей навигацией не получило [8, 18]. Основными сдерживающими факторами здесь выступают малая доступность и высокая стоимость оборудования, необходимого для проведения всего протокола диагностики и лечения, включающего моделирование и навигацию.
Поэтому, получив возможность на собственном опыте оценить возможности трехмерного виртуального моделирования и интраоперационной навигации при проведении лапароскопической адреналэктомии, а также накопив дальнейший опыт выполнения лапароскопических вмешательств на надпочечниках в различных клинических ситуациях, мы решили вновь проанализировать преимущества и недостатки методики моделирования в современных условиях.
Цель исследования: провести ретроспективное сравнительное исследование результатов лапароскопических адреналэктомий, осуществленных с применением методики трехмерного виртуального моделирования и интраоперационной навигации и выполненных без использования данной методики, с учетом накопленного практического опыта и при применении современных систем визуализации. В том числе сравнить частоту осложнений, значения периоперационных показателей; оценить преимущества и недостатки протокола лечения пациентов, включающего моделирование и навигацию; определить перспективы методики трехмерного виртуального моделирования и интраоперационной навигации в эндохирургии надпочечников.
МАТЕРИАЛЫ И МЕТОДЫ
Для анализа было отобрано 123 наблюдения доброкачественных односторонних новообразований надпочечников, при которых лапароскопическая адреналэктомия была выполнена посредством бокового трансперитонеального доступа. С применением методики трехмерного виртуального моделирования и интраоперационной навигации проведены 24 (19,5%) операции, они составили исследуемую группу (группа 1); 99 (80,5%) вмешательств, осуществленных стандартно, были включены в контрольную группу (группа 2).
Распределение больных в группах в зависимости от нозологической природы новообразования представлено в таблице 1.
Таблица 1
Нозологическая природа новообразований в изучаемых группах, n (%)
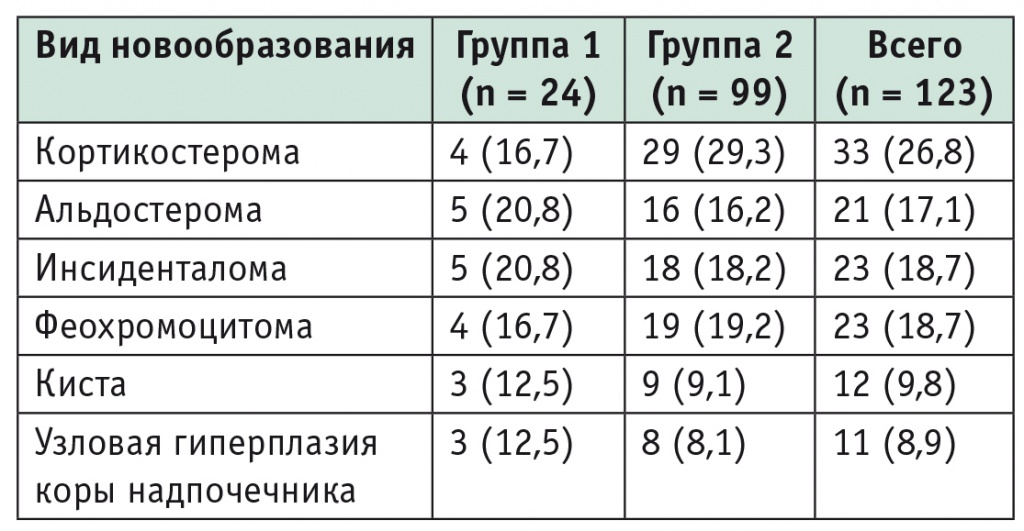
Примечание. В таблицах 1-3 группа 1 — больные, оперированные с применением методики трехмерного виртуального моделирования и интраоперационной навигации; группа 2 — пациенты, которым выполнялись стандартные оперативные вмешательства.
Диагноз того или иного новообразования надпочечника устанавливали на основании тщательной оценки клинической симптоматики, данных лабораторных исследований, результатов УЗИ, КТ и МРТ.
Для качественных показателей проводили расчет критерия χ2 по методике четырехпольных таблиц. В случае если математическое ожидание значений в любой из ячеек таблицы с заданными границами оказывалось ниже 10, применяли вычисление точного критерия Фишера. Для количественных показателей определяли статистическую значимость различий с помощью расчета t-критерия Стьюдента, а также производили расчет доверительных интервалов для вероятности, равной 95%.
С целью сравнения исходных данных в изучаемых группах на дооперационном этапе были зафиксированы основные параметры, характеризовавшие отобранных пациентов (табл. 2).
Таблица 2
Дооперационные усредненные параметры пациентов в изучаемых группах
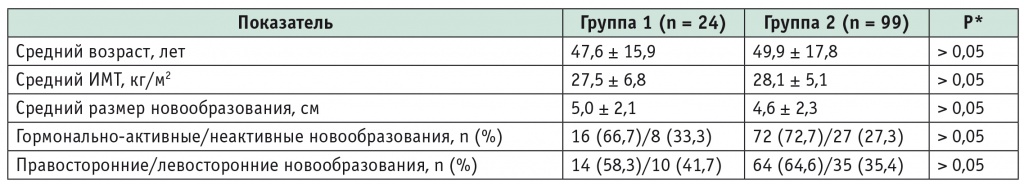
* Различия статистически значимы при p < 0,05.
Примечание. ИМТ — индекс массы тела.
Группы оказались однородными по среднему возрасту, ИМТ, среднему размеру новообразования, доле гормонально-активных новообразований и распределению в зависимости от стороны локализации неоплазии. Следует отметить, что в группе 1 размер удаляемого образования составил от 3,0 до 8,5 см, а в группе 2 — от 1,5 до 8,7 см.
Методика трехмерного виртуального моделирования и интраоперационной навигации
Моделирование в нашем исследовании выполнялось на основе данных рентгеновской КТ. Трехмерная реконструкция производилась средствами рабочей станции, подключенной к спиральному компьютерному томографу. Для трехмерного виртуального моделирования были определены следующие задачи:
-
точное определение размеров образования в разных плоскостях;
- выяснение взаимоотношений между новообразованием и органами брюшной полости;
-
определение толщины прослоек жировой ткани между опухолевидным образованием и сосудистыми структурами (нижняя полая вена, левые почечные вена и артерия и т. д.);
-
четкая идентификация центральной вены надпочечника;
-
выявление признаков смещения или прорастания новообразования.
Лапароскопическая адреналэктомия в группе 1 была составной частью лечебно-диагностического алгоритма, включавшего трехмерное виртуальное моделирование и интраоперационную навигацию, который условно можно разделить на 4 этапа.
Первым этапом являлись КТ, которая выполнялась на мультиспиральном компьютерном томографе Volume Zoom (Siemens Medical Systems, Германия), и верификация диагноза новообразования надпочечника. Обследование пациентов проводилось в три фазы: нативную, раннюю артериальную и венозную фазу контрастирования.
На втором этапе выполняли построение виртуальной модели области предполагаемой операции. Полученные средствами рабочей станции трехмерные изображения передавались на персональный компьютер, где при помощи специального программного обеспечения проводилось построение объемной модели с учетом схемы выбранного цветового кодирования (рис. 1). В последующем производилось определение взаимоотношения новообразования и ткани собственно надпочечника, отношения патологически измененного органа к крупным сосудам брюшной полости и к органам брюшной полости (рис. 2). Определялись локализация и протяженность центральной вены надпочечника. Особенностью использованного программного обеспечения была возможность оценки взаимоотношений исследуемых структур как со стороны свободной брюшной полости, так и со стороны сосудистого русла (рис. 3), что значительно облегчало задачу определения зон тесного прилегания новообразования к стенкам крупных артерий и вен, если таковое имело место.
Рис. 1. Компьютерная томограмма с трехмерной реконструкцией изображения области предполагаемой операции при новообразовании правого надпочечника. Фото авторов
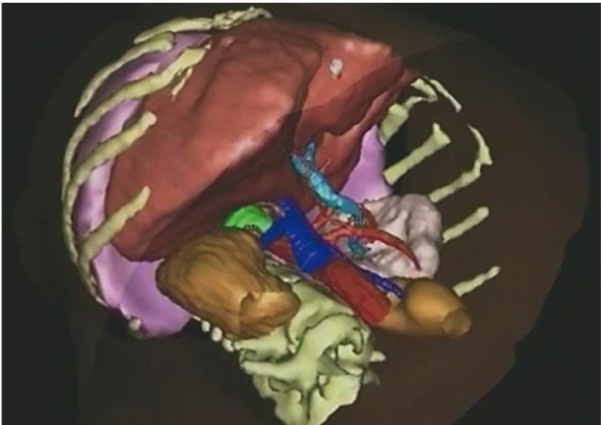
Рис. 2. Оценка взаимоотношений новообразования правого надпочечника с окружающими сосудистыми структурами и паренхиматозными органами по данным компьютерной томограммы с трехмерной реконструкцией изображения. Фото авторов
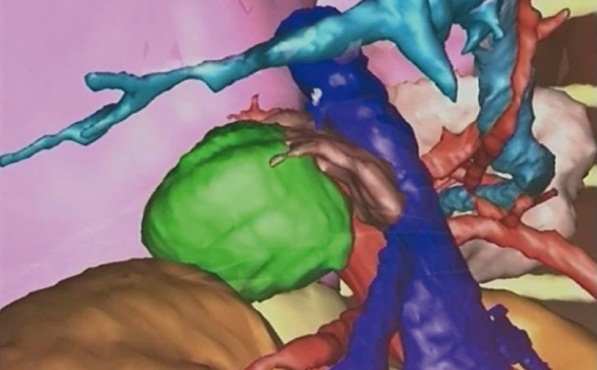
Рис. 3. Оценка зон тесного прилегания опухоли левого надпочечника к почечной вене со стороны сосудистого русла по данным компьютерной томограммы с трехмерной реконструкцией изображения. Фото авторов
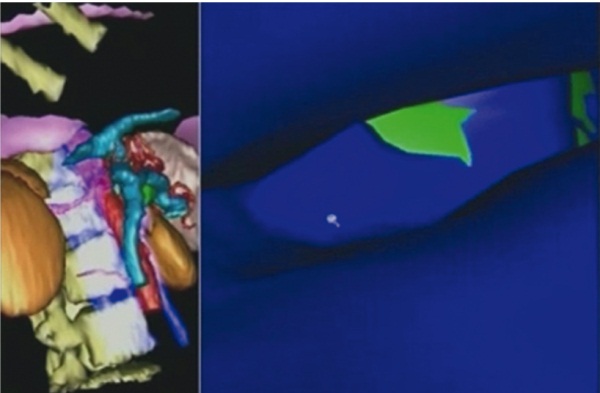
Третьим этапом было планирование вмешательства. В соответствии с ранее полученными данными определялись наилучшие точки введения троакаров. Изменение местоположения точек оперативного доступа производилось с расчетом обеспечения оптимального угла оси операционного действия и ширины операционного поля (рис. 4). Составляли план выделения и клипирования центральной вены, а также диссекции ткани надпочечника. Коррекцию предполагаемого алгоритма осуществляли в соответствии с картиной патологической анатомии заинтересованной области.
Рис. 4. Сравнение прогнозируемых показателей оперативного доступа для левосторонней лапароскопической адреналэктомии с оптимальными теоретическими критериями. Фото авторов
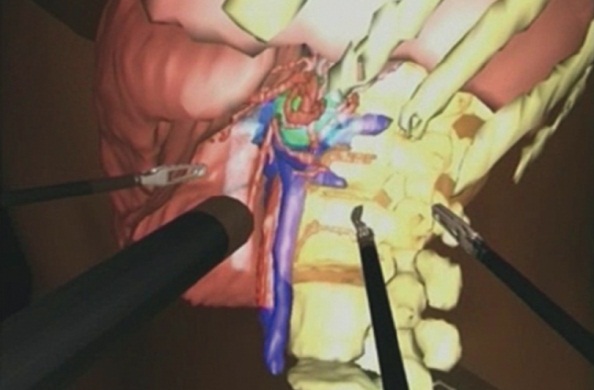
На четвертом этапе проводили собственно оперативное вмешательство. Необходимым условием для использования реконструированной модели в качестве ориентира для интраоперационной навигации являлось наличие эндохирургической видеосистемы с выделенным процессором для обработки и наложения ранее подготовленной трехмерной информации. Требовалось также участие в операции дополнительного ассистента — оператора системы компьютерного моделирования и навигации. Совмещение на экране монитора изображения в реальном времени с изображением ранее построенной трехмерной модели позволяло в значительной мере упростить и ускорить идентификацию заинтересованных органов и сосудистых структур, а также проводить уверенную и безопасную диссекцию тканей вблизи крупных сосудов и паренхиматозных органов, снижая опасность их ранения (рис. 5).
Рис. 5. Совмещение в реальном времени на экране монитора интраоперационной картины и ранее построенного изображения области вмешательства при правосторонней лапароскопической адреналэктомии. Фото авторов
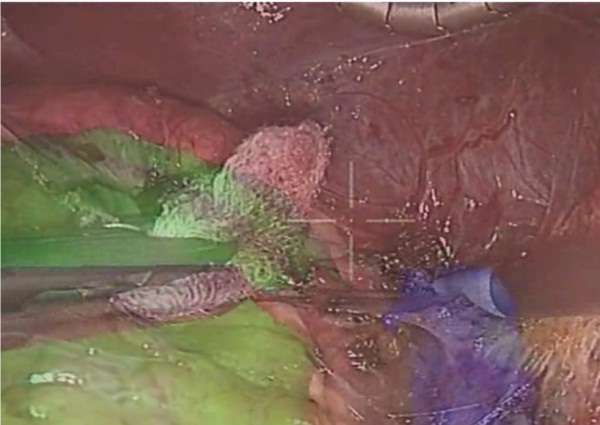
Оперативная техника самого хирургического вмешательства в обеих группах была стандартной с точки зрения принятой в нашей клинике методики, которая была неоднократно описана в предшествующих публикациях [1, 3].
РЕЗУЛЬТАТЫ
В первую очередь были проанализированы непосредственные результаты операций, проведенных в обеих группах, а также данные, отражающие течение раннего послеоперационного периода (табл. 3).
Таблица 3
Результаты оперативных вмешательств в изучаемых группах
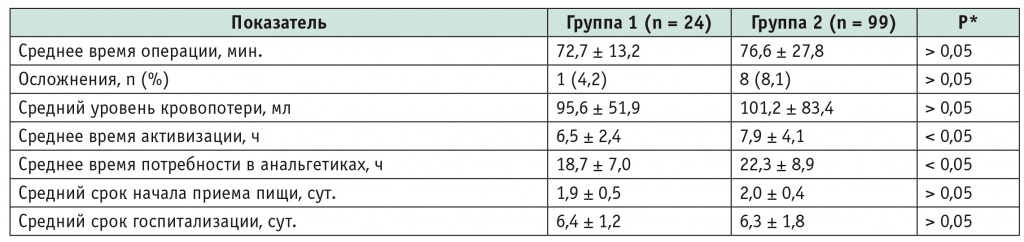
* Различия статистически значимы при p < 0,05.
Среднее время оперативного вмешательства, частота осложнений и средний уровень интраоперационной кровопотери в группах не имели статистически значимой разницы (p > 0,05), однако в относительном выражении доля осложнений в группе, где применялась методика моделирования и навигации, оказалась в 1,93 раза меньше, чем в контрольной группе. Такие результаты позволяют ожидать, что при большем числе наблюдений различия в частоте осложнений приобретут статистическую значимость.
Следует отметить, что в исследуемой группе имело место 1 (4,2%) осложнение, связанное с развитием реактивного панкреатита, который был успешно купирован консервативными методами. В контрольной группе было 8 (8,1%)осложнений. В их числе наблюдались 1 (1,01%) клинически значимое кровотечение из печени и 2 (2,02%) кровотечения из селезенки, которые были устранены лапароскопически и не повлияли на дальнейшее течение послеоперационного периода. У 3 (3,03%) пациентов в послеоперационном периоде имел место реактивный панкреатит, явления которого были успешно разрешены консервативно. Подкапсульная гематома селезенки, потребовавшая проведения конверсии доступа и спленэктомии, развилась в 1 (1,01%) случае. Данный переход на открытый доступ был единственным в наших наблюдениях в обеих группах. Натечная гематома в предбрюшинной клетчатке, в проекции троакарного доступа, развилась в послеоперационном периоде у 1 (1,01%) пациента, в связи с ней была проведена хирургическая коррекция. Отдаленных послеоперационных осложнений, равно как и случаев летальности, в наших наблюдениях не было ни в одной из групп пациентов.
Такие показатели, как время активизации больных после операции и срок потребности в обезболивании, оказались статистически значимо (p < 0,05) меньше в группе 1, а различия в сроке начала приема пищи и продолжительности госпитализации не имели статистической значимости (p > 0,05).
Необходимо заметить, что данные предоперационного планирования с использованием трехмерного виртуального моделирования в нашем исследовании послужили причиной изменения ранее намеченного доступа в 3 (12,5%) случаях. Вследствие индивидуальных анатомических особенностей пациентов было решено применить отличную от стандартной схему расположения троакаров. В 2 (8,3%) других случаях результатом использования дооперационной трехмерной визуализации стало изменение последовательности этапов лапароскопического оперативного вмешательства. У одного пациента с поражением левого надпочечника тесное прилегание опухоли к левой почечной вене, а также расположение центральной вены кзади от новообразования сделали невозможным ее клипирование и пересечение на первом этапе. В этом случае вначале была выполнена прецизионная диссекция надпочечника вместе с опухолью, после чего центральную вену выделили, клипировали и пересекли. У другого больного с опухолью правой адреналовой железы была определена схожая локализация центральной вены позади образования и имело место интимное прилежание новообразования к нижней полой вене, что также потребовало первоначального выполнения частичной диссекции опухоли, а последующим этапом было произведено пересечение центральной вены. Таким образом, применение методики предоперационного виртуального моделирования способствовало изменению плана оперативного вмешательства в исследуемой группе в 5 (20,8%) наблюдениях.
В обеих группах во всех случаях динамическое наблюдение за больными показало отсутствие признаков рецидивов новообразований надпочечников, а также разрешение клинических симптомов и лабораторных признаков, связанных с гормональной активностью опухолей, в случаях, когда таковая изначально имела место.
ОБСУЖДЕНИЕ
Лапароскопическая адреналэктомия на настоящий момент представляет собой оптимальный вариант хирургического лечения пациентов с новообразованиями надпочечников. При этом резерв для снижения частоты осложнений в хирургии адреналовых желез не представляется исчерпанным, и одним из путей повышения безопасности оперативных вмешательств является применение методики трехмерного виртуального моделирования и интраоперационной навигации [11, 13, 15, 23].
Наш собственный опыт применения данной методики продемонстрировал, что трехмерное моделирование с последующей интраоперационной навигацией позволяет уменьшить частоту возникновения осложнений практически в 2 раза. При статистической обработке данная разница оказалась незначимой, но это можно связать в первую очередь с объемом клинического материала. Стоит ожидать, что при увеличении количества пациентов, оперированных с использованием представленной вспомогательной методики визуализации, различия в доле осложнений примут характер статистически значимых. Кроме того, и в изученной когорте больных трехмерное виртуальное моделирование и интраоперационная навигация привели к статистически значимому снижению части показателей течения раннего послеоперационного периода (время активизации, срок потребности в обезболивании). Этот факт мы объясняем тем, что более подробные данные об анатомическом строении заинтересованной области, полученные при проведении виртуального моделирования, позволяют повысить степень прецизионности манипуляций, снизить уровень операционной агрессии и предотвратить излишнюю хирургическую травму. В то же время методика моделирования и интраоперационной навигации не продемонстрировала в нашем исследовании тенденции к сокращению длительности госпитализации пациентов.
Следует отметить, что изучаемый метод проявил и ряд недостатков, которые в основном были связаны с организационными трудностями и ростом себестоимости лечебно-диагностического алгоритма. Обязательным условием для проведения операции с применением интраоперационной навигации является наличие специализированной видеосистемы, что повышает общую стоимость оборудования операционной. Этап виртуального моделирования также должен проводиться с применением соответствующего компьютерного томографа, а обработка и перенос трехмерной информации требуют наличия специального программного обеспечения, что еще более повышает экономические затраты [4, 21].
Вследствие этого применение изучаемой методики у всех больных, требующих хирургического вмешательства в связи с патологией надпочечника, невозможно, что подтверждается и мировым опытом [8, 18]. В то же время основными кандидатами для использования трехмерного виртуального моделирования и интраоперационной навигации становятся пациенты с ожидаемыми трудностями во время осуществления лапароскопической адреналэктомии (например, с большими размерами новообразования и неясной анатомией, отмеченными при выполнении стандартной дооперационной КТ или МРТ) [16, 21].
Таким образом, вышеприведенные данные демонстрируют, что методика трехмерного виртуального моделирования и интраоперационной навигации в лапароскопической хирургии надпочечников позволяет добиться улучшения результатов, а также перспективна с точки зрения снижения частоты осложнений. Однако реализация преимуществ в условиях реального здравоохранения может быть достигнута при условии большого потока пациентов и оперирования больных с анатомически более сложной патологией. Поэтому приобретение соответствующего аппаратного обеспечения и применение методики трехмерного виртуального моделирования и интраоперационной навигации при проведении лапароскопических адреналэктомий следует признать целесообразными только в условиях специализированных клинических центров, в которых постоянно ведется лечение большого количества пациентов, имеющих различные новообразования адреналовых желез.
ЗАКЛЮЧЕНИЕ
Методика трехмерного виртуального моделирования и интраоперационной навигации при проведении лапароскопической адреналэктомии характеризуется снижением частоты осложнений и улучшением течения раннего послеоперационного периода, однако преимущества методики могут быть реализованы только в условиях крупных специализированных хирургических центров, где постоянно осуществляются оперативные вмешательства у большого количества больных с патологией надпочечников.







