ВВЕДЕНИЕ
COVID-19 — это опасное для жизни инфекционное заболевание, вызываемое вирусом SARS-CoV-2, который впервые был обнаружен в китайском городе Ухань в ноябре 2019 года и после этого быстро распространился по всему миру. В марте 2020 года ВОЗ классифицировала COVID-19 как пандемическое заболевание[1].
Согласно данным ВОЗ, по состоянию на 24 мая 2023 года во всем мире было зарегистрировано 766 895 075 подтвержденных случаев заболевания COVID-19, из них 6 935 889 летальных[2]. Описаны явные гендерные различия в исходах COVID-19. При одинаковом уровне заражения мужчин и женщин одного региона пациенты мужского пола сталкиваются с более высоким риском госпитализации и смерти, чем больные женского пола[3]. У женщин, находящихся в пре- и постменопаузе, вероятность тяжелого течения COVID-19 и смерти от заболевания ниже, чем у мужчин того же возраста[4–6]. Мужской пол определен как фактор риска тяжелого течения COVID-19[6–9]. Это позволяет предположить наличие определенных защитных механизмов женского организма, обусловленных благоприятным влиянием половых гормонов, в частности эстрогенов, на клиническое течение и исходы COVID-191.
В исследовании R. Costeira и соавт. с участием 152 637 пациенток в возрасте 40–60 лет обнаружено, что женщины в постменопаузе имеют более высокий риск тяжелого течения COVID-19, чем женщины в пременопаузе[10]. В ряде работ, среди которых метаанализ, получены данные о том, что менопаузальная гормональная терапия (МГТ) снижает риск тяжелого течения COVID-19 и ассоциирована с более низкой вероятностью смерти от всех причин, связанных с COVID-19 (ОШ = 0,28; 95%-й ДИ: 0,18–0,44), у женщин в постменопаузе[4, 11–13].
Установлено, что эстрогены влияют на множество компонентов врожденного и адаптивного иммунного ответа[10]. Эстрогены могут оказывать противовоспалительное действие при инфекции, вызываемой вирусом SARS-CoV-2, на различных стадиях: начиная от повышения противовирусной резистентности отдельных клеток и заканчивая подавлением продукции провоспалительных цитокинов[14].
С учетом весьма убедительной доказательной базы в отношении положительного влияния МГТ на клиническое течение COVID-19 представляется актуальным изучение воздействия различных видов МГТ на течение этого заболевания. В настоящее время в международных медицинских источниках нами не обнаружено исследований, в которых анализировалось бы влияние различных способов доставки МГТ у женщин в пери- и постменопаузе на течение инфекции, вызываемой вирусом SARS-CoV-2.
Цель исследования: оценить симптомы и тяжесть течения коронавирусной инфекции, вызываемой вирусом SARS-CoV-2, у пациенток в пери- и постменопаузе на фоне менопаузальной гормональной терапии различных форм (пероральной и трансдермальной) и при ее отсутствии.
МАТЕРИАЛЫ И МЕТОДЫ
Ретроспективное когортное исследование выполнялось в отделении гинекологической эндокринологии ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России с ноября 2021 по март 2023 года.
Работа была одобрена локальным этическим комитетом ФГБУ «НМИЦ АГП им. В.И. Кулакова» Минздрава России (протокол № 11 от 11 ноября 2021 года). Все пациентки подписывали информированное добровольное согласие на участие в исследовании.
Критериями включения были пери- и постменопауза (в том числе хирургическая менопауза в результате овариоэктомии).
Критериями исключения являлись: ВИЧ-инфекция и другие врожденные и приобретенные иммунодефициты; наличие системных, онкологических, аутоиммунных заболеваний, а также заболеваний соединительной ткани в анамнезе.
В исследование были включены 93 пациентки в пери- и постменопаузе, которые перенесли инфекцию, вызываемую вирусом SARS-CoV-2, в разных условиях: на фоне пероральной МГТ (n = 22, первая группа), трансдермальной МГТ (n = 22, вторая группа) с применением стандартных и низких доз препаратов в обеих группах и без МГТ (n = 49, третья группа, или группа сравнения). Проводился опрос пациенток, включавший вопросы о симптомах, длительности, тяжести течения и терапии COVID-19.
В соответствии с методическими рекомендациями Минздрава России «Профилактика, диагностика и лечение новой коронавирусной инфекции COVID-19» случаи заболевания считали подтвержденными при: положительном результате лабораторного исследования на наличие РНК SARS-CoV-2 (с применением методов амплификации нуклеиновых кислот) или на наличие антигена SARS-CoV-2 (с применением иммунохроматографического анализа) вне зависимости от клинических проявлений; положительном результате исследования на антитела IgA, IgM, IgG у пациенток с клинически подтвержденной инфекцией COVID-19. Критериями легкого течения COVID-19 являлись температура не выше субфебрильной (< 38 °C) и отсутствие критериев среднетяжелого и тяжелого течения. Среднетяжелое и тяжелое течение заболевания констатировали на основании медицинских документов, содержавших информацию о степени тяжести COVID-19[15].
Все полученные сведения заносили в специально разработанную анкету с последующим оформлением базы данных в формате таблиц Microsoft Excel. Статистический анализ проводили с использованием программного пакета Statistica 13.5.0.
Количественные параметры были проверены на соответствие нормальному распределению с помощью критерия Шапиро — Уилка. По количественным параметрам с нормальным распределением данные в тексте и таблицах представлены в виде M (SD), где М — среднее значение, SD — стандартное отклонение среднего значения. Для качественных показателей были рассчитаны частоты (%). С целью установления различий между группами для нормально распределенных числовых показателей использовали критерий ANOVA для нескольких групп, затем проводили попарное сравнение групп с помощью t-критерия Стъюдента для двух независимых выборок. С целью сравнения независимых выборок по дихотомическим показателям и установления статистически значимых различий между ними использовали метод хи-квадрат (χ2) Пирсона, при попарном сравнении групп применяли точный критерий Фишера для небольших выборок.
Критический уровень значимости (p) при проверке статистических гипотез принимали равным 0,05, с учетом поправки Бонферрони на непрерывность при сравнении трех групп он составил 0,017 (0,05/3).
РЕЗУЛЬТАТЫ
Клинико-анамнестические данные пациенток и сведения о препаратах, применявшихся в группах пероральной и трансдермальной МГТ, представлены в таблицах 1, 2.
Таблица 1
Клинико-анамнестические данные пациенток исследуемых групп
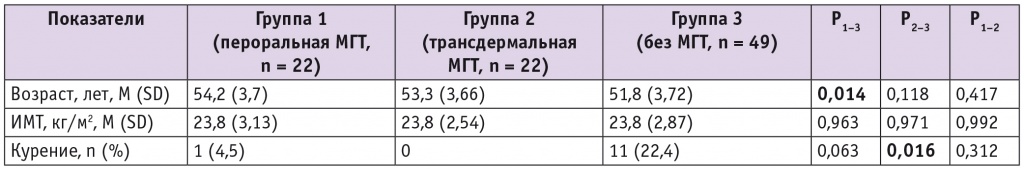
Примечание. В таблицах 1, 3 критический уровень значимости (p) с поправкой Бонферрони: 0,05/3 = 0,017.
Таблица 2
Препараты, применявшиеся в группах менопаузальной гормональной терапии

Средний возраст пациенток в группах пероральной и трансдермальной МГТ статистически значимо не различался (p = 0,417). Пациентки с пероральной МГТ были статистически значимо старше женщин, не применявших МГТ (p = 0,014). Курящих женщин было значительно больше в группе без МГТ, чем в группе, получавшей трансдермальную МГТ (p = 0,016) (см. табл. 1).
Как показано в таблице 3, длительность заболевания COVID-19, а также частота различных симптомов болезни у пациенток, не применявших МГТ и использовавших пероральную или трансдермальную МГТ, статистически значимо не различались, за исключением частоты ринита. У женщин с трансдермальной МГТ в сравнении с женщинами, использовавшими пероральную МГТ, ринит встречался чаще (p = 0,008). Тяжелое течение COVID-19 наблюдалось у 26,5% пациенток, не использовавших МГТ, и с одинаковой частотой (9,1%) у женщин, применявших пероральную или трансдермальную МГТ.
Таблица 3
Характер течения и виды терапии COVID-19 у пациенток исследуемых групп
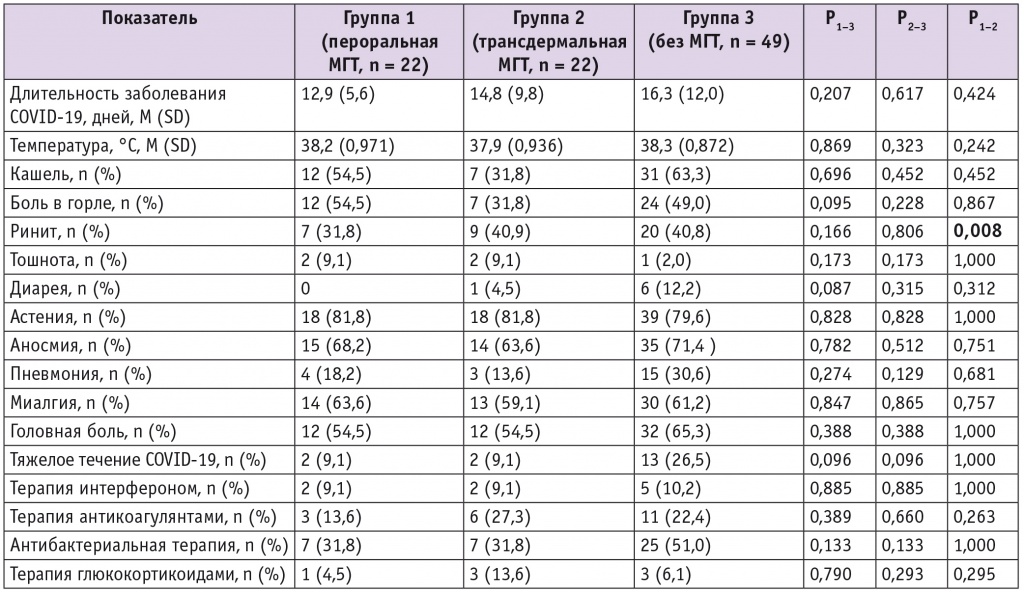
При объединении пациенток с пероральной и трансдермальной МГТ в одну группу (n = 44) и сравнении ее с группой без МГТ (n = 49) обнаружено, что тяжелое течение COVID-19 статистически значимо чаще встречалось у женщин, не применявших МГТ (р = 0,030) (рис.).
Рис. Частота тяжелого течения COVID-19 у пациенток, применявших и не применявших менопаузальную гормональную терапию, %
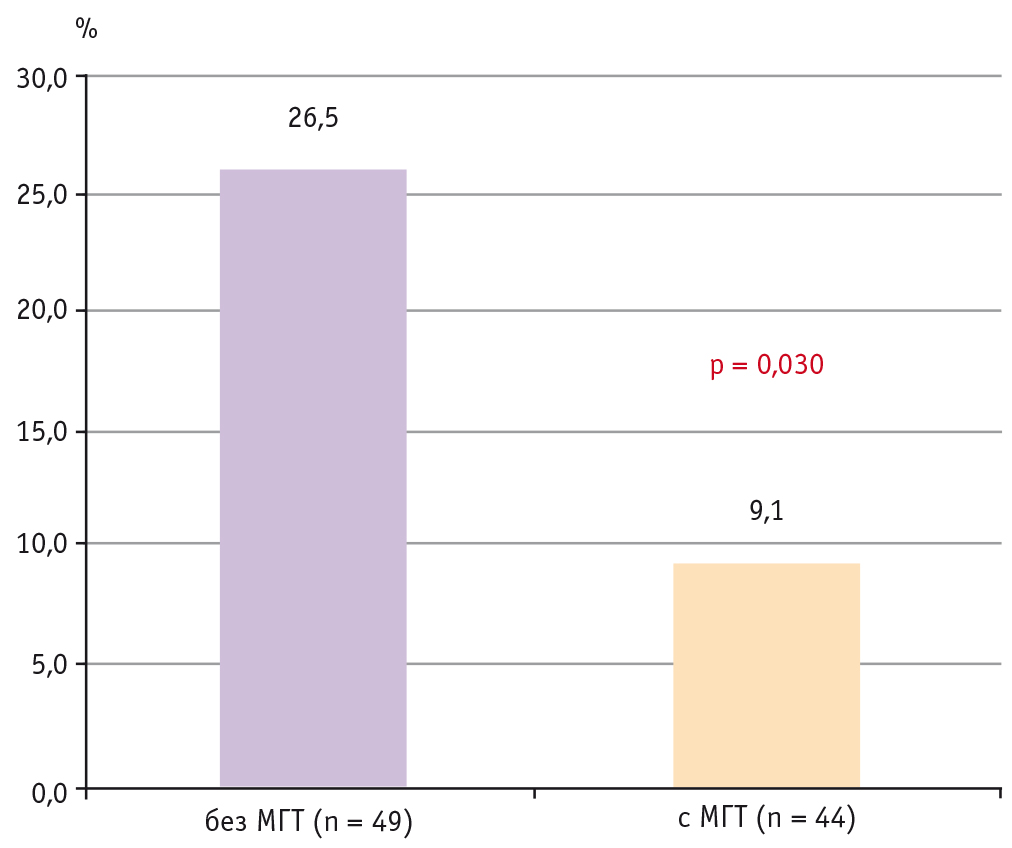
Вероятность тяжелого течения COVID-19 в группе пациенток, использовавших МГТ, была ниже, чем в группе без МГТ (ОШ = 0,27; 95%-й ДИ: 0,08–0,92).
ОБСУЖДЕНИЕ
Новая коронавирусная инфекция SARS-CoV-2 (ранее — 2019-nCoV) в короткие сроки после ее появления в Ухане достигла масштабов пандемии[16]. Это привело к принятию широкого спектра мер во всем мире с объявлением чрезвычайной ситуации и ограничениями в повседневной жизни.
Рядом авторов была показана связь между приемом женщинами эстрадиола в составе МГТ и снижением риска смерти от COVID-19[10, 12].
В настоящем исследовании тяжелое течение COVID-19 обнаружено практически у каждой четвертой пациентки в пери- и постменопаузе, не использовавшей МГТ (26,5%), а при применении МГТ значительно реже — у каждой 11-й пациентки (p = 0,030). При этом частота тяжелого течения заболевания в группах с разным путем введения МГТ (пероральным или трансдермальным) не различалась и составила по 9,1% (р = 1,000).
Крупномасштабные данные самонаблюдений, полученные из британского приложения для отслеживания симптомов COVID-19 (> 151 тыс. женщин в постменопаузе, применяющих МГТ), показали более низкую частоту тяжелого течения заболевания (госпитализаций и потребности в респираторной поддержке) у пациенток с МГТ по сравнению с больными без МГТ[17]. Аналогичные результаты приводятся в метаанализе Y. Liu и соавт.[4].
На основе базы данных Центра исследований и наблюдения Королевского колледжа врачей общей практики Оксфордского университета (1 863 478 женщин) показано, что использование МГТ связано со значительно более низкой вероятностью смерти от всех причин при COVID-19 (скорректированное ОШ = 0,22; 95%-й ДИ: 0,05–0,94; р = 0,041)[10].
В рамках когортного исследования, включавшего 68 466 пациентов мужского и женского пола с COVID-19 из 17 стран, выявлено, что среди женщин старше 50 лет риск летального исхода у получающих терапию эстрадиолом более чем на 50% ниже, чем у тех, кто не принимает эстрадиол (ОШ = 0,33)[12]. На момент написания настоящей статьи мы не нашли исследований, где сравнивались бы различные способы доставки МГТ у женщин в пери- и постменопаузе на фоне инфекции SARS-CoV-2.
Сложная взаимосвязь между половыми гормонами и иммунной системой указывает на то, что, возможно, МГТ оказывает плейотропное воздействие на иммунную функцию у женщин в пери- и постменопаузе. Результаты проведенных исследований позволяют предположить, что МГТ у женщин в перименопаузе благоприятно действует на состояние иммунной системы[14].
Большинство исследований, где оценивался эффект МГТ (монотерапии эстрогенами или комбинации с прогестинами), продемонстрировали подавление продукции таких провоспалительных цитокинов, как ФНО-α, ИЛ-1β и ИЛ-6, мононуклеарными клетками периферической крови ex vivo или in vivo в сыворотке крови женщин, получавших МГТ[18–20].
В недавнем исследовании показано, что применение МГТ, включающей трансдермальный эстрадиол в сочетании с микронизированным прогестероном интравагинального применения, ассоциировано с изменением иммунных параметров крови: лимфоцитов (значимое увеличение количества T-хелперов — главных регуляторов иммунной системы) и моноцитов. Причем у моноцитов разных субпопуляций меняется фенотип, что, вероятно, вносит свой вклад в иммунопотенцирующие свойства МГТ[21].
Во время пандемии COVID-19 были разработаны рекомендации по ведению женщин на фоне МГТ. Согласно документу Итальянского общества по контрацепции (2020 г.), МГТ и КОК не следует отменять у тех пациенток, которые переносят COVID-19 в легкой и среднетяжелой форме, однако при тяжелой форме заболевания в этих средствах нет необходимости, при значительном ухудшении может быть рассмотрено назначение антикоагулянтов[22]. В совместных рекомендациях Испанского общества по менопаузе, Испанского общества гинекологии и акушерства и Испанского общества по тромбозу и гемостазу установлено, что в случае легкого течения COVID-19 следует перейти на применение трансдермальных препаратов, при среднетяжелой форме требуется добавить к парентеральной терапии антикоагулянты, а при тяжелой — отменить МГТ и продолжить антикоагулянтную терапию[23].
Другие исследователи считают, что надо с осторожностью относиться к утверждениям о том, что половые стероидные гормоны определяют гендерные различия в тяжести течения и смертности от COVID-19; по их мнению, при угрожающем жизни течении заболевания врожденные генетические поломки в иммунной системе оказываются более критичными, чем циркулирующие стероидные гормоны. Сторонники такой точки зрения указывают на то, что использование половых стероидов для лечения больных COVID-19 не подтверждается биохимическими, физиологическими данными или клинически достоверными результатами[24].
ЗАКЛЮЧЕНИЕ
В нашем исследовании у лиц, применявших менопаузальную гормональную терапию (МГТ), статистически значимо реже наблюдалось тяжелое течение COVID-19 по сравнению с женщинами, не использовавшими МГТ.
Патогенетические особенности влияния коронавируса SARS-CoV-2 и специфическое воздействие МГТ на систему гемостаза требуют тщательной оценки рисков продолжения использования МГТ. Однако следует учесть, что эстрогены являются «ключевым игроком» в формировании иммунологического ответа и оказывают многогранное протективное влияние на эндотелий сосудов. Корреляции между уровнями половых гормонов, тяжестью заболевания и смертностью показывают потенциал использования МГТ для модуляции иммунного ответа и повышения устойчивости к развитию неблагоприятных исходов заболевания.
Требуются дополнительные исследования для поиска защитных механизмов половых стероидов в отношении коронавирусной инфекции, чтобы в дальнейшем медицинские работники были готовы локализовать данную инфекцию и справиться с ней как можно скорее.
Поступила: 07.06.2023
Принята к публикации: 13.07.2023
________
1 COVID-19 National Emergency Response Center; Epidemiology and Case Management Team; Korea Centers for Disease Control and Prevention. Coronavirus Disease-19: The First 7,755 Cases in the Republic of Korea. Osong Public Health Res. Perspect. 2020; 11(2): 85–90. DOI: 10.24171/j.phrp.2020.11.2.05







