До недавнего времени наиболее эффективным методом скрининга распространенных ХА плода (синдромов Дауна, Эдвардса, Патау и Тернера) считали биохимический и ультразвуковой скрининг в I триместре беременности. Общая оценка уровней биохимических маркеров (свободного хорионического гонадотропина человека и плазменного протеина, связанного с беременностью) в сочетании с толщиной воротникового пространства в 11–13 недель беременности и возрастом матери позволяет выявить до 80–90% плодов с трисомией по 21й хромосоме при количестве ложноположительных результатов 5% [1, 2].
Использование дополнительных биохимических и ультразвуковых маркеров, включая определение плацентарного фактора роста в сыворотке беременной, оценку носовых костей и кровоток в венозном протоке, может повысить выявляемость до 95% и снизить уровень ложноположительных результатов до 3% [1, 3].
Инвазивная пренатальная диагностика (биопсия ворсин хориона или амниоцентез), проведение которой требуется беременным групп риска, в 0,5–2% случаев сопряжена с риском осложнений вплоть до самопроизвольного прерывания беременности.
Доказательство наличия ДНК плода, циркулирующей в плазме крови матери, и развитие методов высокопроизводительного секвенирования позволили разработать новый способ скрининга анеуплоидий плода. Поскольку в кровотоке матери, помимо материнской ДНК, циркулирует внеклеточная ДНК плода, то, взяв кровь у беременной женщины, можно обнаружить нарушение числа хромосом плода, избежав при этом внутриматочного вмешательства. Обычно концентрация ДНК плода в плазме крови беременной с 11 недель составляет более 4% общего объема свободно циркулирующей ДНК. Доля ДНК плода нарастает с увеличением гестационного срока.
Данные широкомасштабных исследований [2–11] показали высокую чувствительность неинвазивного пренатального ДНКскрининга (НИПС) в отношении наиболее частых анеуплоидий плода (синдромов Дауна, Эдвардса, Патау, Тернера), которые составили 99% всех хромосомных нарушений. В нашем предшествующем исследовании, посвященном валидации метода, выявляемость трисомии по 21й хромосоме при НИПС была равна 99% при уровне ложноположительных результатов 0,2% [3].
Целью настоящего исследования является оценка эффективности НИПС методом высокопроизводительного секвенирования для выявления трисомий по 21й, 18й, 13й хромосомам и половых хромосом плода в образцах крови женщин с отягощенным акушерским анамнезом и осложненным течением данной беременности.
МАТЕРИАЛЫ И МЕТОДЫ
Всего обследовали 506 женщин в сроках беременности от 11 до 17 недель. Проводили сбор анамнестических данных, клиническое обследование, скрининг I триместра беременности — эхографию, определение содержания сывороточных маркеров, компьютерный анализ (программа ASTRAYA). При отборе пациенток учитывали ограничения метода: онкологические заболевания у беременной женщины; многоплодная беременность, включая случаи спонтанной редукции одного из плодов; ИМТ более 30 кг/м2.
Исследование проводилось лабораторией молекулярногенетических методов Научного центра акушерства, гинекологии и перинатологии им. акад. В. И. Кулакова с 2015 по 2017 г. Анализировали образцы материнской венозной крови (10 мл ЭДТА), была предоставлена информация по каждому образцу, код пациентки выставлялся автоматически, учитывались возраст женщины, гестационный срок, дата забора крови. У всех участниц было получено добровольное согласие на исследование и забор периферической крови из вены.
Материал анализировали с помощью полупроводникового высокопроизводительного секвенирования. В периферической крови женщины определяли наличие или отсутствие у плода анеуплоидий, а также его пол. На первом этапе из крови матери отделяли плазму, на втором — выделяли внеклеточную ДНК, содержащую материнскую и фетальную фракции. В последующем последовательно осуществляли приготовление библиотек ДНК для высокопроизводительного секвенирования, эмульсионную ПЦР и секвенирование на приборе Ion Proton (Life Technologies, США). Результаты оценивали с помощью биоинформатической обработки данных секвенирования ДНК. Для сравнения покрытия внутри образца применяли Ttest.
РЕЗУЛЬТАТЫ
Из 506 обследованных женщин беременность завершена у 246, в остальных случаях беременность пролонгируется.
Проанализированы клинические и анамнестические данные беременных: возраст, социальноэкономическое положение, профессиональные вредности, наследственность, экстрагенитальная и гинекологическая заболеваемость, характер менструальной функции, репродуктивный анамнез.
Средний возраст женщин составил 34,6 ± 6,5 года. Распределение женщин по возрасту показано в таблице 1.
Таблица 1
Распределение обследованных женщин по возрасту
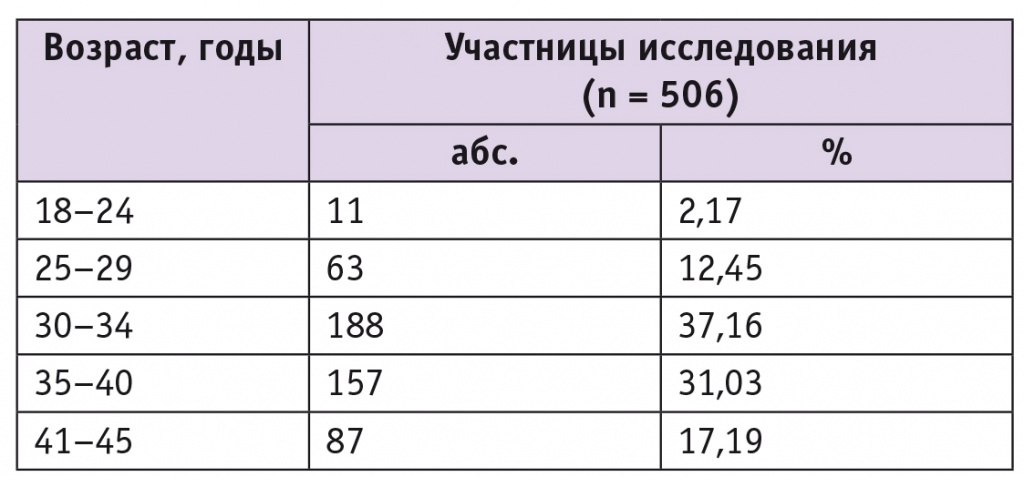
Как следует из представленных данных, возраст 48,22% участниц исследования — от 35 до 45 лет, старше 30 лет было большинство — 85,38%.
Все женщины проживали в одинаковых климатогеографических условиях, преимущественно в Москве и Московской области, имели среднее и высшее образование. Профессиональные вредности при сборе анамнеза не выявлены.
Субклинический гипотиреоз, медикаментозно компенсированный, был установлен у 154 (30,43%) участниц, он являлся наиболее частой экстрагенитальной патологией. Вероятно, это связано с преобладанием женщин старшего репродуктивного возраста, а также беременных с отягощенным акушерским анамнезом, что часто сопряжено с сопутствующим заболеванием щитовидной железы.
При анализе частоты гинекологических заболеваний обнаружен высокий процент хронических ВЗОМТ, пролеченных до наступления данной беременности, чаще всего в анамнезе отмечены эндометрит и/или сальпингит, оофорит (табл. 2).
Таблица 2
Структура гинекологических заболеваний у обследованных женщин
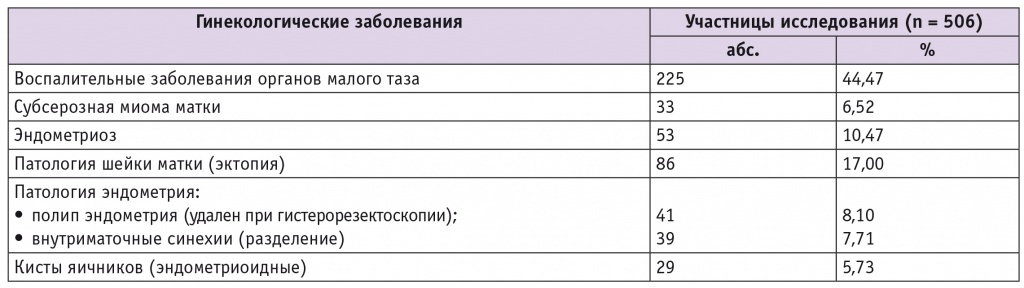
Менархе в возрасте 10–14 лет наступило у 95,5% женщин.
Проанализирована репродуктивная функция у обследованных женщин. Установлено, что 259 (51,18%) участниц страдали привычным выкидышем. Проведение неинвазивного пренатального скрининга у данной группы продиктовано необходимостью подтверждения отсутствия анеуплоидий у плода при беременности, осложненной кровотечением, при нецелесообразности использования инвазивных диагностических методик как первой линии вмешательств после общепринятого скрининга.
Выявлено, что у 259 пациенток с привычным выкидышем в анамнезе было 806 беременностей. У 21 (4,1%) женщины в анамнезе отмечено рождение детей с ХА. В большинстве случаев им проводили инвазивные диагностические процедуры с последующим кариотипированием, однако беременные изъявили желание пройти НИПС как предварительный этап перед инвазивной процедурой. Всем участницам были разъяснены возможности и ограничения НИПС, несмотря на это 5 беременных отказались от амниоцентеза по личным соображениям.
98 (19,37%) женщин были первобеременными, из них у 50 беременность наступила после периода бесплодия в результате ЭКО. Исследование проведено по желанию женщин у 72 (14,23%) с второй и у 56 (11,07%) с третьей беременностью, в анамнезе у них — рождение здоровых доношенных детей.
В таблице 3 представлены анамнестические данные о числе беременностей у участниц исследования.
Таблица 3
Число беременностей у обследованных женщин
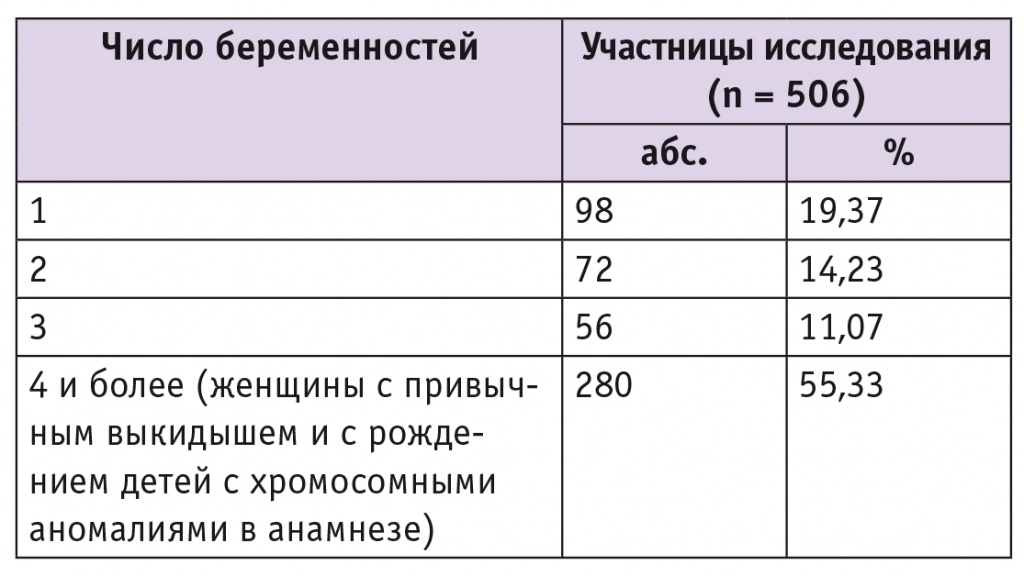
Наиболее часто у женщин с привычным выкидышем в анамнезе имелись ранние гестационные потери — самопроизвольные выкидыши или неразвивающиеся беременности, что составило 50,25% от числа всех наступивших беременностей, данные представлены в таблице 4.
Таблица 4
Исходы предыдущих беременностей у женщин с привычным выкидышем
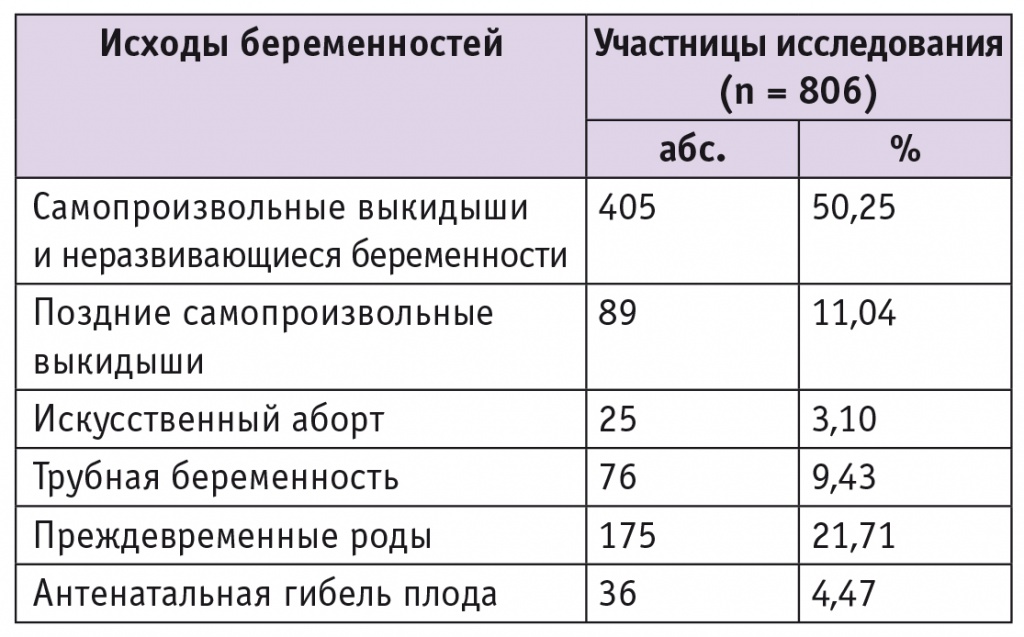
В 11,04% наблюдений произошли поздние выкидыши, причиной которых был хориоамнионит и излитие околоплодных вод.
Таким образом, 51,25% женщин страдали привычным выкидышем, что диктует необходимость выбора правильной терапевтической тактики: своевременного выявления ХА плода и определения показаний для проведения инвазивных процедур в случае крайне высокого риска рождения ребенка с патологией.
В исследовательских целях с учетом всех необходимых условий для проведения теста беременным было предложено пройти неинвазивный пренатальный скрининг с обязательным разъяснением его возможностей и ограничений. После подписания формы информированного согласия проводили НИПС, интерпретировал результаты врачгенетик. Во всех случаях, когда требовалось изменение тактики ведения беременности, пациентки были направлены на инвазивную процедуру (амниоцентез) с последующим кариотипированием.
Течение и исходы беременностей у женщин после неинвазивного пренатального ДНКскрининга
Большинство женщин наблюдались и родоразрешены в Научном центре акушерства, гинекологии и перинатологии им. акад. В. И. Кулакова, где проведен анализ течения беременностей с сопоставлением частоты гестационных осложнений.
В 268 (52,9%) наблюдениях беременность осложнилась угрожающим/начавшимся выкидышем на сроках 12–16 недель, подтвержденным клиническими признаками и данными УЗИ.
Признаками угрожающего выкидыша стали кровянистые выделения и тянущие боли внизу живота, они встречались у 198 (39,1%) пациенток. В 70 (13,9%) наблюдениях отмечены боли внизу живота и в пояснице без кровянистых выделений из половых путей. У остальных 238 (47,0%) женщин жалоб в первой половине беременности не было.
У пациенток до 22 недель беременности регистрировали следующие осложнения: ОРВИ с субфебрильной температурой тела — 12,5%, умеренная рвота беременных — 26,6%, анемия беременных — 16,6%.
При угрожающем/начавшемся выкидыше пациенток госпитализировали, им проводилась терапия, направленная на пролонгирование беременности, включавшая гормональные, гемостатические, спазмолитические препараты.
По данным НИПС, патология кариотипа была представлена трисомией по 21й хромосоме у 7, по 13й — у 2, по 18й — у 1 беременной, моносомия хромосомы Х (синдром Тернера) встретилась в 6 наблюдениях. Искусственные прерывания беременности до 22 недель были произведены в связи с подтвержденной кариотипированием ХА у 11 женщин, в 2 случаях отмечены множественные пороки развития, несовместимые с жизнью: пороки развития ЦНС, омфалоцеле. В 3 случаях, когда была подтверждена моносомия хромосомы Х, женщины отказались от прерывания беременности, в настоящее время беременности пролонгируются.
У одной пациентки имел место поздний самопроизвольный выкидыш в 16 недель (излитие околоплодных вод) при нормальном кариотипе плода. Антенатальная гибель плода произошла у 2 женщин, преждевременные роды в сроках от 27 до 35 недель — у 5: в связи с излитием околоплодных вод, несостоятельностью рубца на матке после кесарева сечения, тяжелой плацентарной недостаточностью, задержкой роста плода. Во всех этих случаях у плодов был установлен нормальный кариотип.
ОБСУЖДЕНИЕ
В настоящее время общепринятый комбинированный скрининг беременных на ХА плода позволяет оценить только косвенные маркеры, в связи с чем он имеет недостаточно высокую чувствительность и специфичность [2, 4–8]. Однозначный результат может быть получен только при инвазивной диагностике. Однако после ее проведения возможны осложнения, основным из которых является прерывание беременности: от 0,5% до 2% [9]. В то же время увеличение числа женщин старше 35 лет, с тяжелой соматической и гинекологической патологией, нарушениями репродуктивной функции, которые планируют деторождение, может повысить частоту выявляемой хромосомной патологии [10–14].
В представленной работе в исходах беременности 246 женщин группы риска, отобранных на основе существующего неинвазивного пренатального скрининга беременных, высокий риск ХА выявлен у 11 (4,5%). Высокие риски по НИПС были подтверждены цитогенетическим кариотипированием. В то же время метод НИПС имеет некоторые ограничения, в частности невозможно с его помощью определить микроаномалии и мозаицизм по отдельным хромосомам и полиплоидии, получить корректные результаты при низкой доле фетальной ДНК. Ложноположительный результат моносомии Ххромосомы, вероятно, был обусловлен плацентарным мозаицизмом [11–23]. Достоверно установлена трисомия по 13й хромосоме. Однако единичные наблюдения относительно этой трисомии не позволяют сделать однозначный вывод о чувствительности и специфичности метода в данном случае.
Таким образом, с учетом результатов настоящего исследования можно рекомендовать высокопроизводительное секвенирование для неинвазивного скрининга на анеуплоидии 21й, 18й, 13й и половых хромосом с последующим инвазивным обследованием при их обнаружении.
Многие авторы [10, 20, 21] указывают, что методы НИПС до сих пор не могут быть альтернативой или заменить инвазивные процедуры, особенно в случаях мозаицизма, когда число анеуплоидных клеток уступает нормальным. Однако НИПС возможно использовать для скрининга и определения риска у всех беременных независимо от возраста до постановки окончательного диагноза, как самостоятельный метод, так и в дополнение к другим существующим методам.
Исследователи полагают, что определение свободной ДНК эмбрионального происхождения может заменить или усовершенствовать существующие скрининговые тесты [2–10, 13, 18–21]. Подобные выводы были сделаны на основании результатов нескольких проспективных исследований, во всех случаях подтвержденных классическим кариотипированием.
ЗАКЛЮЧЕНИЕ
Данное исследование показало, что неинвазивный пренатальный ДНКскрининг является перспективным методом для скрининга хромосомных аномалий плода с ранних сроков беременности, который может быть рекомендован женщинам в качестве высокоэффективного пренатального теста.
Работа поддержана Министерством образования и науки Российской Федерации (соглашение № 14.607.21.0136, идентификатор проекта RFMEFI60715X0136).







