Аутоиммунные нарушения все чаще признают причинами фармакорезистентной эпилепсии. Аутоиммунный энцефалит представляет собой группу синдромов с развитием амнезии, поведенческими нарушениями и эпилептическими приступами. Эпилептические приступы регистрируются у 50% пациентов с диагнозом лимбического энцефалита (ЛЭ).
Различают два иммунологических субтипа ЛЭ: паранео-пластический и аутоиммунный. Паранеопластический ЛЭ встречается относительно редко, преимущественно у пожилых людей, практически всегда одновременно имеется системная онкопатология. В основе патогенеза данного вида ЛЭ лежит необратимый Т-клеточный цитотоксический ответ на внутриклеточные нейрональные антигены. Клиническое течение ЛЭ — монофазное, и ответ на лечение ограничен.
Аутоиммунный ЛЭ ассоциирован с LG1, GABABR, AMPAR, GAD и другими антителами к различным структурам ЦНС [1]. Встречается он значительно чаще, в любом возрасте, но особенно часто у детей, подростков, молодых взрослых, преимущественно у иммунокомпетентных. В основе патогенеза аутоиммунного ЛЭ лежит обратимая дисфункция нейронов в результате обратимого взаимодействия аутоантител с поверхностно-клеточными синаптическими антигенами нейронов. Аутоиммунный ЛЭ имеет рецидивирующее клиническое течение с хорошим ответом на терапию, достижением ремиссии заболевания в 70-80% случаев [2].
Около 15% пациентов страдают фармакорезистентной эпилепсией на фоне аутоиммунного энцефалита. Эпилептические приступы и фацио-брахиальная дистония могут предшествовать появлению когнитивных нарушений [3]. Некоторые специфические антинейрональные антитела с патогенным потенциалом присутствуют у пациентов с фармакорезистентной фокальной эпилепсией [4].
Дебют эпилепсии опережает диагностику аутоиммунных заболеваний в 30% случаев. В первые 1-2 года от дебюта аутоиммунного заболевания наблюдается тенденция к максимальному учащению эпилептических приступов. До 47-50% пациентов с аутоиммуннной эпилепсией могут иметь нормальную картину МРТ головного мозга на момент дебюта эпилептических приступов [5]. В остальных случаях обнаруживают патологические изменения на МРТ головного мозга, при этом у 50% больных они находятся на уровне амигдало-гиппокампального комплекса, у 20% — на уровне латеральных отделов височной доли и у 30% — на экстратемпоральном уровне. Отсутствие структурных изменений, по данным нейровизуализации, и патологических изменений ликвора не исключает аутоиммунную эпилепсию [6].
Важными диагностическими предикторами аутоиммунной эпилепсии являются специфические паттерны на ЭЭГ. ЭЭГ при данном заболевании позволяет оценить тяжесть и локализацию эпилептиформной активности, кроме того, такое исследование необходимо для наблюдения за пациентами с неконвульсивным эпилептическим статусом [7].
В большинстве опубликованных работ, связанных с оценкой электроэнцефалографических изменений при аутоиммунной эпилепсии, описаны следующие изменения на ЭЭГ [8, 9]:
-
фронтальная, бифронтальная, темпоральная, битемпоральная, фронтотемпоральная, париетальная и биокципитальная интериктальная/иктальная фокальная эпилептиформная активность;
-
диффузное замедление корковой ритмики в тета-/дельта-диапазоне частот с дельта-пароксизмами;
-
фокальное замедление;
-
лобная и височная интермиттирующая ритмическая дельта-активность (1-4 Гц), продолжающаяся не менее 2 секунд (FIRDA, TIRDA);
-
бессудорожный эпилептический статус;
-
периодическая латерализованная эпилептиформная активность;
-
генерализованная периодическая эпилептиформная активность.
Специфическим ЭЭГ-коррелятом аутоиммунной эпилепсии, ассоциированной с антителами к NMDA-рецепторам, является ритмическая продолженная дельта-активность 1-3 Гц с наложенной бета-активностью от 20 до 30 Гц на каждой дельта-волне (экстремальные дельта-щетки) [10].
КЛИНИЧЕСКИЙ СЛУЧАЙ
Представляем клинический случай пациентки А., 20 лет. Пациентка в сопровождении родственников обратилась к неврологу-эпилептологу Неврологического центра эпилептологии, нейрогенетики и исследования мозга Университетской клиники ФГБОУ ВО «Красноярский государственный медицинский университет им. проф. В.Ф. Войно-Ясенецкого» в ноябре 2017 года с жалобами на сонливость, вялость, спутанность мыслей, нарушение памяти, преимущественно о текущих событиях и событиях недавнего прошлого, на эпизоды по типу «задумывания», рассеянность внимания, снижение интереса к окружающему миру, нежелание общения с родственниками и друзьями, плаксивость, жалостливость, чувство страха. Девушка не могла вспомнить события предыдущих дней. Нарушения памяти развились после депривации сна в течение двух суток.
В анамнезе: обострения лабиального герпеса с подросткового возраста (у матери пробанда были частые обострения лабиального герпеса). В октябре 2017 г. отмечала нарушение моторной памяти (забывала танцевальные движения во время выступлений). В ноябре 2017 г. после депривации сна возникли выраженная диффузная головная боль, дневная сонливость. На следующий день пациентка не могла вспомнить события предыдущих двух суток.
Объективно: сознание ясное, контакт несколько затруднен, мышление замедлено, отмечаются нарушение памяти о событиях недельной давности, трудности концентрации внимания, спутанность мыслей; фон настроения варьирует, плаксива. Критика снижена. В неврологическом статусе: черепно-мозговые нервы — зрачки d = s, фотореакции живые, глазные щели d = s, движения глазных яблок в полном объеме, нистагма нет. Легкая асимметрия носогубных складок при мимической нагрузке. Язык по средней линии, глоточный рефлекс вызывается, глотание сохранено. Двигательная сфера: мышечный тонус и мышечная сила сохранены. Сухожильные рефлексы D = S живые. Чувствительность сохранена. Симптомов натяжения, менингеальных знаков, координаторных и тазовых нарушений нет.
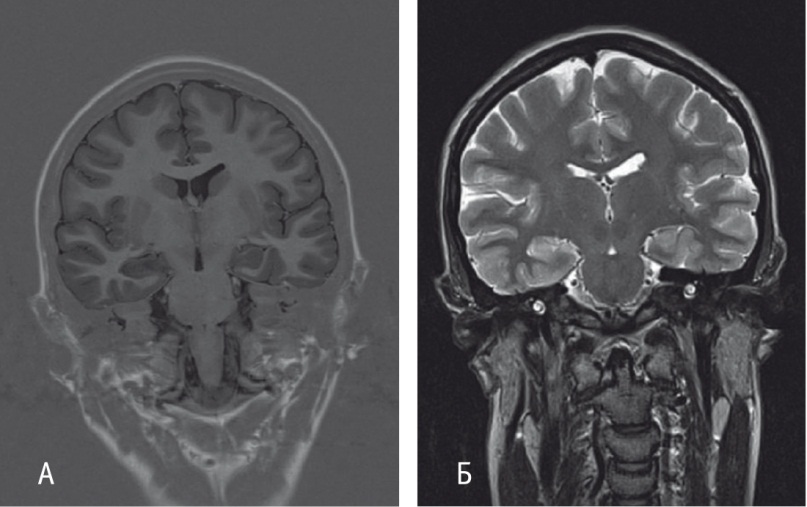
По результатам нейропсихологического тестирования выявлен амнестический синдром (по типу фиксационной амнезии). МРТ головного мозга показала уменьшение размеров правого гиппокампа с повышением сигнала в Т2, FLAIR-взвешенных изображениях (ВИ) в области правого гиппокампа и миндалевидном теле справа (рис. 1А); повышение сигнала в Т2-ВИ в левом гиппокампе (рис. 1Б). Антитела к GAD, NMDA-рецепторам в крови и антинейрональные антитела (Hu, Yo-1, CV2, Ма2, Ri, амфифизин) отрицательные.
Рис. 1. Магнитно-резонансная томограмма головного мозга больной А., 20 лет (декабрь 2017 года). А — уменьшение размеров правого гиппокампа с повышением сигнала в FLAIR-взвешенных изображениях (ВИ) в области правого гиппокампа и миндалевидном теле справа; Б — повышение сигнала в Т2-ВИ в левом гиппокампе. Иллюстрация авторов: Панина Ю.С., Дмитренко Д.В. (2018)
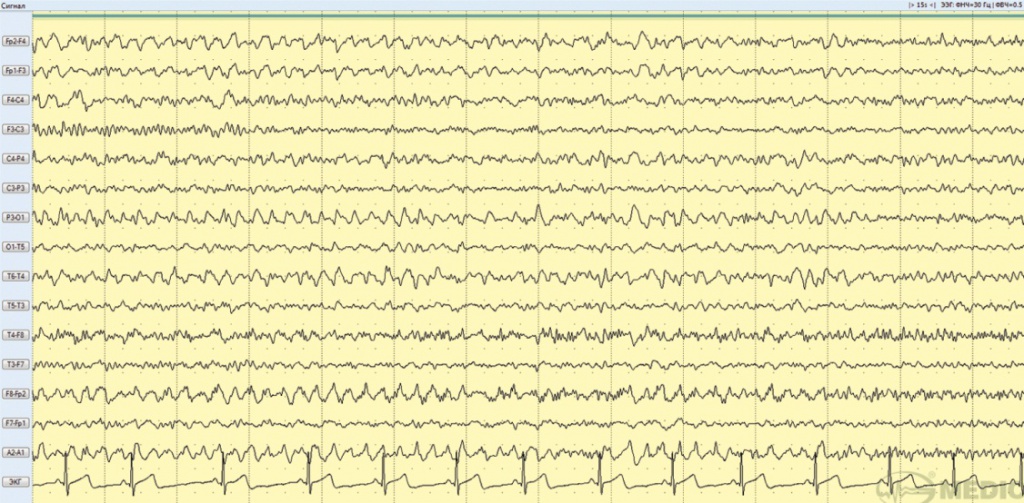
По данным ЭЭГ (в состоянии бодрствования) зарегистрирована продолженная интериктальная эпилептиформная активность в правой лобно-височной области, представленная медленными волнами тета- и дельта-диапазона частот амплитудой до 50 мкВ по лобно-теменно-височным отведениям, с периодическим распространением по полушариям, амплитудным преобладанием по правому полушарию головного мозга (рис. 2).
Рис. 2. Фрагмент электроэнцефалограммы больной А., 20 лет (декабрь 2017 года): зарегистрирована продолженная интериктальная эпилептиформная активность в правой лобно-височной области, представленная медленными волнами тета- и дельта-диапазона частот амплитудой до 50 мкВ по лобно-теменно-височным отведениям, с периодическим распространением по полушариям, амплитудным преобладанием по правому полушарию головного мозга. Иллюстрация авторов: Панина Ю.С., Дмитренко Д.В. (2018)
По результатам исследования гормонов щитовидной железы, уровень тетрайодтиронина повышен, тиреотропного гормона — в пределах нормы, антитела к тиреопероксидазе значительно повышены (в пределах 192,7 Ед/мл).
Таким образом, по данным жалоб, анамнеза, неврологического осмотра, нейровизуализационного, нейрофизиологического и лабораторного обследования уточнен клинический диагноз: аутоиммунный ЛЭ с поражением медиобазальных отделов правой височной доли и левого гиппокампа с выраженными когнитивными, эмоционально-волевыми нарушениями. Аутоиммунная эпилепсия с приступами с фокальным началом, немоторными когнитивными приступами с заторможенностью поведенческих реакций; серийное течение. Аутоиммунный тиреоидит. Проведено лечение: в/в глюкокортикоиды (ГК) с последующим переходом на пероральную форму, в/в высокодозные иммуноглобулины, противоэпилептические препараты (леветирацетам в дозе 750 мг/сут).
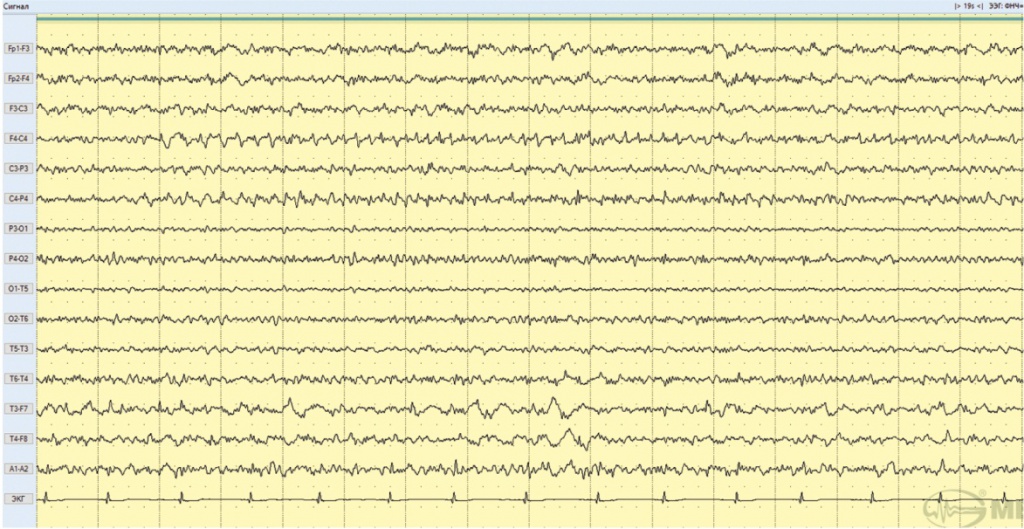
В результате проводимой терапии через месяц, по данным ЭЭГ, на фоне доминирующей полиморфной низкоамплитудной активности зарегистрирована периодическая интериктальная эпилептиформная активность в правой лобно-центральной области, представленная острыми волнами альфа-1 и тета-диапазона частот амплитудой до 40 мкВ, продолжительностью 5-30 секунд, высокого индекса (рис. 3).
Рис. 3. Фрагмент электроэнцефалограммы больной А., 20 лет (февраль 2018 года): периодическая интериктальная эпилептиформная активность в правой лобно-центральной области, представленная острыми волнами альфа-1 и тета-диапазона частот амплитудой до 40 мкВ, продолжительностью 5-30 секунд, высокого индекса. Иллюстрация авторов: Панина Ю.С., Дмитренко Д.В. (2018)
Отмечалась позитивная клиническая динамика в виде улучшения памяти о текущих событиях и событиях недавнего прошлого, а также внимания и эмоционального фона. Эпилептические приступы во время наблюдения не регистрировались. Через 3 месяца от дебюта заболевания, по данным ЭЭГ, изменения в сравнении с предыдущим исследованием положительные: иктальная и интериктальная эпилептиформная активность отсутствовала.
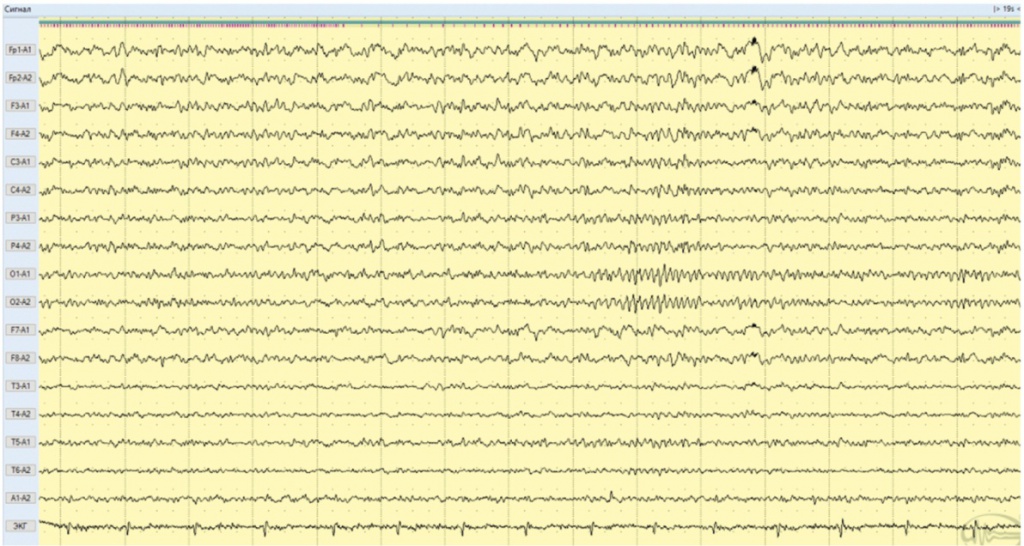
Через 5 месяцев от дебюта заболевания терапия ГК завершена, продолжен курс лечения в/в иммуноглобулином, антиконвульсантами. На ЭЭГ иктальная и интериктальная эпилептиформная активность не отмечена. Доминировала полиморфная низкоамплитудная активность. Индекс альфа-ритма низкий, амплитудой до 30 мкВ (рис. 4). Эпилептических приступов не было, астенический синдром, эмоционально-волевые, когнитивные нарушения купированы.
Рис. 4. Фрагмент электроэнцефалограммы больной А., 20 лет (июнь 2018 года): иктальная и интериктальная эпилептиформная активность не зарегистрирована. Доминирует полиморфная низкоамплитудная активность. Индекс альфа-ритма низкий, амплитудой до 30 мкВ. Иллюстрация авторов: Панина Ю.С., Дмитренко Д.В. (2018)
ОБСУЖДЕНИЕ
Аутоиммунная эпилепсия является актуальной проблемой здравоохранения. Больные аутоиммунной эпилепсией нуждаются в комплексном подходе, своевременной диагностике и совместном ведении врачом неврологом-эпилептологом, психологом (по показаниям — психиатром), иммунологом. При поздней диагностике в условиях хронического течения аутоиммунного ЛЭ прогноз может быть неблагоприятным, а заболевание осложнено мезиальным темпоральным склерозом с развитием фармакорезистентной структурной фокальной эпилепсии, эмоционально-волевыми и когнитивными (дисмнестическими) расстройствами.
ЗАКЛЮЧЕНИЕ
Ранняя диагностика аутоиммунной эпилепсии с помощью амбулаторного видеоЭЭГ-мониторинга с регистрацией характерных для нее ЭЭГ-коррелятов имеет решающее значение, поскольку своевременное начало противоэпилептической терапии, иммуносупрессивного лечения увеличивает вероятность достижения ремиссии заболевания, уменьшает частоту и тяжесть эпилептических приступов.







