В подавляющем большинстве (≈ 90%) случаев возбудителями ОРИ служат различные вирусы, поражающие разные отделы дыхательных путей и вызывающие системные проявления инфекции той или иной степени выраженности (табл.) [3, 6].
Таблица
Характерные клинические проявления острых респираторных вирусных инфекций в зависимости от возбудителя
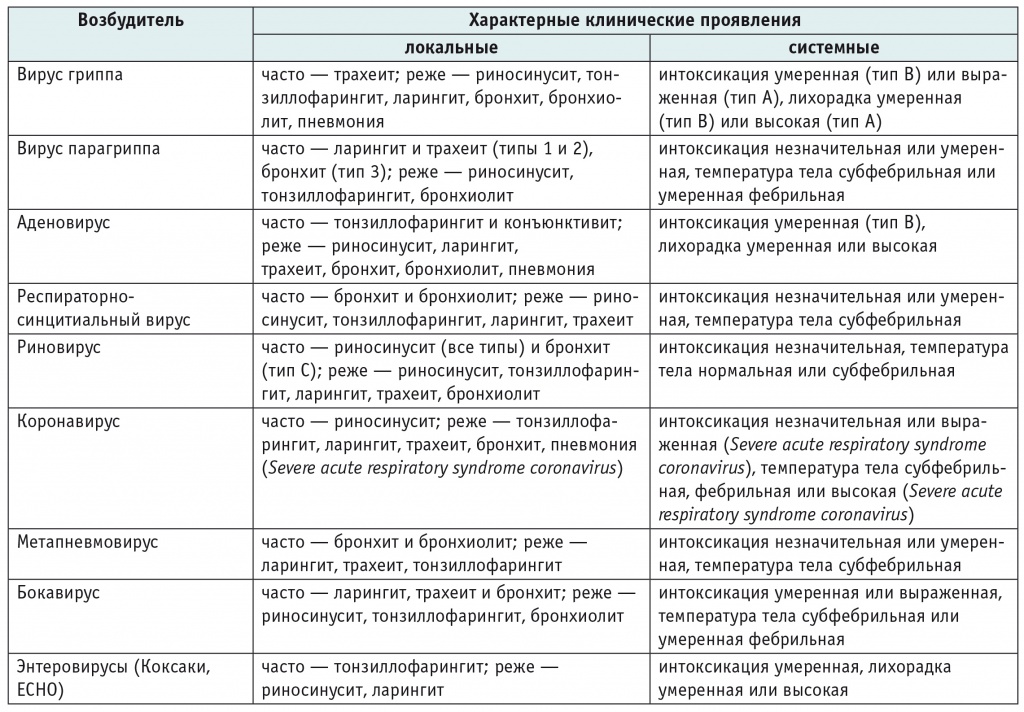
Принято считать, что на долю бактериальных возбудителей приходится только около 10% заболеваний, однако в последнее время педиатрам все чаще приходится сталкиваться с вирусно-бактериальными микст-инфекциями. Учитывая большое количество возбудителей, полиморфизм обусловливаемых ими клинических проявлений и разнообразие клинических форм, даже при самом тщательном обследовании больного не всегда удается установить возбудителя, вызвавшего респираторную инфекцию [3, 7].
Как известно сегодня, дыхательные пути, в том числе легкие, нестерильны. Получены данные о микробиоме легких в норме и при развитии некоторых заболеваний [12]. Условия в дыхательных путях здорового человека не способствуют размножению патогенной микрофлоры, но при развитии инфекционного заболевания ситуация меняется. Удаление возбудителей из дыхательных путей обеспечивается мукоцилиарным транспортом при участии иммунной системы [10].
Клиническая картина респираторных инфекций определяется не только этиологическим фактором, но и возрастом пациента, преморбидным фоном, состоянием эпителиальных барьеров. Вне зависимости от возбудителя симптомы ОРИ во многом сходны: повышение температуры тела (преимущественно в первые 2−3 суток заболевания), снижение аппетита, астения. Одним из самых частых проявлений заболеваний респираторного тракта служит такой хорошо известный симптом, как кашель. Кашель — сложный рефлекс, направленный на восстановление проходимости дыхательных путей, одна из важнейших защитно-приспособительных реакций органов дыхания на изменение физиологического равновесия [3].
ПОДХОДЫ К ТЕРАПИИ КАШЛЯ
Рациональный выбор и адекватное применение терапии у детей предполагают знание причин кашля, специфики механизма формирования кашлевого рефлекса в детском возрасте и, конечно, особенностей препаратов, используемых при лечении кашля.
Защитная реакция в виде увеличения количества бронхиальной слизи проявляется сразу, в первые минуты заболевания, когда вирусы (или бактерии) попадают на слизистую оболочку бронхиальной стенки. В условиях воспаления развивается гиперсекреция более вязкой слизи с повышенными адгезивными свойствами. В этой ситуации снижается функциональная активность реснитчатого эпителия, что приводит к нарушению мукоцилиарного транспорта и ослаблению основного местного защитного механизма — уменьшению продукции секреторного IgA, интерферона, лактоферрина и лизоцима. В результате нарушается дренажная функция дыхательных путей, создаются условия для бронхиальной обструкции, инвазии микроорганизмами. Кашель служит эффективным механизмом санации трахеобронхиального дерева [3, 6].
При кашле необходимо определить его интенсивность, тембр, периодичность, время появления, наличие и свойства мокроты и прочие клинические особенности, что может помочь в диагностике и определить тактику лечения. В начале ОРИ кашель, как правило, сухой и непродуктивный или малопродуктивный, в дальнейшем он приобретает влажный характер вследствие усиленного образования мокроты. У детей первых 4–5 лет жизни мокроту не всегда удается обнаружить, так как ребенок обычно проглатывает ее.
Подходы к терапии кашля при ОРИ по-прежнему неоднозначны [13, 23]. Как отмечено в обзоре, опубликованном в 2013 г. и посвященном изучению закономерностей течения кашля при ОРИ у детей, при естественном течении ОРИ у 10% пациентов продолжительность кашля достигает 4 недель, в 25% случаев кашель сохраняется более 2 недель и у 50% детей — до 10 дней; при этом кашель не только нарушает самочувствие ребенка, но и снижает качество жизни и сна ребенка и родителей [23].
Немедикаментозные средства
Традиционно в терапии кашля используют так называемые домашние средства. Показано, что уменьшению частоты и выраженности кашля по сравнению с таковыми при отсутствии лечения (но не в случае плацебо) способствует применение мазей и бальзамов, содержащих камфору, ментоловое и эвкалиптовое масла. Однако по сравнению с плацебо эти мази статистически значимо улучшают лишь качество сна больных детей и их родителей. При употреблении таких средств нередко развиваются нежелательные эффекты: раздражение кожного покрова, слизистой оболочки носа и глаз [15]. Необходимо учитывать также возрастные ограничения и возможность развития аллергических реакций, ухудшающих течение заболевания. На сегодняшний день нет убедительных доказательств эффективности паровых ингаляций, часто применяемых родителями при ОРИ у детей. В некоторых исследованиях паровые ингаляции облегчали кашель, в других случаях они не оказывали никакого влияния, при этом ни одно исследование не включало пациентов детского возраста [24].
Одним из наиболее древних домашних средств, применяемых при простуде, служит мед. По некоторым данным, мед предотвращает рост бактерий, вирусов и дрожжевых грибков, уменьшает воспаление. Как продемонстрировано в небольших рандомизированных контролируемых исследованиях, выполненных у детей и подростков (от 1 года до 18 лет), использование меда для облегчения кашля является лучшей тактикой, чем отсутствие лечения. Показано, что эффекты меда в отношении всех симптомов кашля не отличаются от эффектов декстрометорфана — противокашлевого средства центрального действия [21]. Необходимо помнить о риске аллергических реакций при употреблении меда, а также об ограничении его применения у детей до 1 года из-за недостаточного иммунитета против возбудителя ботулизма (Clostridium botulinum), который может присутствовать в меде [21, 23].
Положительный результат отмечен при использовании приемов дренажа и элементов лечебной физкультуры, причем чем младше ребенок, тем лучше он может откашляться при данных манипуляциях [3]. Однако для применения этого метода требуется помощь специалиста или предварительное обучение родителей, так как неадекватные действия могут причинить вред ребенку.
Лекарственные средства
Выбор лекарственных препаратов для лечения кашля — непростая задача в практике педиатра. Имеется широкий спектр средств, влияющих на кашель, но вопросы соотношения эффективности и безопасности их применения в педиатрии остаются открытыми.
Препараты, влияющие на продукцию и выведение мокроты, отличаются друг от друга по механизму действия, фармакологическим свойствам, показаниям к применению и широте использования. В большинстве случаев применение противокашлевых препаратов при воспалительных заболеваниях дыхательных путей не показано или ограничено, так как, подавляя кашлевой рефлекс и замедляя мукоцилиарный транспорт, они увеличивают вязкость бронхиального секрета и повышают риск развития бактериального воспаления.
Мукоактивные средства способствуют выведению мокроты из дыхательных путей при различных воспалительных заболеваниях. Несмотря на сходный конечный результат, механизм действия разных групп этих средств различен.
- Отхаркивающие средства рефлекторного действия (корень солодки, корень алтея, термопсис и другие растительные средства) рефлекторно стимулируют отхаркивание вследствие содержания алкалоидов и сапонинов, которые запускают каскад реакций: раздражающее воздействие на слизистую оболочку желудка вызывает раздражение кашлевого центра, его активность повышается, что приводит к усилению синтеза жидкого бронхиального секрета и выраженности кашлевого рефлекса. Кратковременность действия растительных препаратов определяет необходимость их частого приема, чем обусловлен такой побочный эффект, как сильная тошнота (возможна рвота). Использование растительных лекарственных средств для лечения и профилактики различных заболеваний (фитотерапия) имеет давнюю традицию и не утратило актуальности по сей день [20]. Зачастую растительные препараты считают безопасными, однако необходимо помнить, что «натуральность» их происхождения еще не означает безопасности: они могут вызывать побочные реакции (например, аллергию, гиперсекрецию, тошноту и рвоту), а также неблагоприятно взаимодействовать с другими лекарственными средствами [14]. Таким образом, к назначению отхаркивающих средств необходимо подходить крайне осторожно, предпочтение надо отдавать стандартизированным фитопрепаратам, производство которых отвечает требованиям стандарта «Надлежащая производственная практика» (Good Manufacturing Practice), а эффективность и безопасность подтверждены клиническими исследованиями в педиатрии.
- Муколитические средства (ацетилцистеин, карбоцистеин, амброксол и др.) разжижают мокроту, что способствует ее эффективному выведению из респираторного тракта.
Ацетилцистеин и карбоцистеин изменяют вязкость секрета, влияя на его физико-химические свойства, вследствие чего нормализуется мукоцилиарный транспорт. При этом они не увеличивают объем бронхиального секрета.
Основной механизм действия карбоцистеина — производного аминокислоты цистеина — заключается в нормализации соотношения сиаломуцинов и фукомуцинов посредством повышения активности сиалилтрансферазы, ингибирования нейраминидазы и ферментов, способствующих переносу углеводных остатков на белковую основу муцинов. Кроме того, под влиянием карбоцистеина уменьшается количество бокаловидных клеток слизистой оболочки и снижается выработка слизи.
Ацетилцистеин — также производное аминокислоты цистеина — обладает прямым муколитическим действием: разрушает дисульфидные связи мукополисахаридов мокроты, снижает вязкость слизи и облегчает ее выведение из дыхательных путей, не вызывая при этом значимого увеличения количества мокроты. В практике педиатра крайне важно, что благодаря такому механизму действия ацетилцистеин разжижает не только бронхиальный секрет, но и вязкий назальный секрет, поэтому его можно применять при заболеваниях как нижних, так и верхних дыхательных путей, например при риносинуситах.
Кроме того, широко известно антиоксидантное действие ацетилцистеина, реализуемое вследствие содержания нуклеотидной тиоловой (сульфгидрильной) группы, участвующей в процессах нейтрализации свободных радикалов, а также обусловленное процессами синтеза глутатиона. Благодаря антиоксидантному действию ацетилцистеин проявляет также противовоспалительный и антитоксический эффекты [3, 6]. В настоящее время оксидативный стресс, связанный с избыточным образованием свободных радикалов при воспалении, считают ключевым механизмом повреждения респираторной системы [9]. Влияние ацетилцистеина на антиоксидантные системы способствует защите клеток от свободнорадикального повреждения, что приводит к снижению выраженности воспаления слизистых оболочек дыхательных путей и ослаблению клинических проявлений. Антиоксидантные свойства ацетилцистеина, сопровождаемые противовоспалительным эффектом, безусловно, повышают его значение в лечении заболеваний дыхательной системы [3].
Весьма ценным свойством ацетилцистеина является способность уменьшать адгезию бактерий к эпителиальным клеткам слизистой оболочки дыхательных путей и тем самым снижать микробную колонизацию респираторного тракта. Его прием приводит к меньшему образованию биопленок грамположительными и грамотрицательными бактериями и грибками, а также к уменьшению продукции экстрацеллюлярного полисахаридного матрикса, что способствует разрушению зрелых биопленок [16, 17, 19].
Ацетилцистеин более активно действует на биопленки, чем другие муколитики. Например, способность снижать жизнеспособность биопленок золотистого стафилококка (через 5 и 48 часов) у ацетилцистеина в 5–6 раз выше, чем у амброксола и бромгексина [22].
Сочетанное применение ацетилцистеина с антибиотиками разных классов приводит к усилению бактерицидной активности последних [17, 19]. При необходимости назначения антибиотиков их комбинация с ацетилцистеином способствует статистически значимому сокращению длительности инфекционных заболеваний дыхательных путей у детей [4, 11]. В нескольких исследованиях показана целесообразность комбинации ацетилцистеина с антибиотиком при экссудативном среднем отите у детей — осложнении ОРИ, приводящем к тугоухости [8, 18].
Как показывают исследования и опыт, применение ацетилцистеина у детей безопасно. Проведены 20 контролируемых исследований использования ацетилцистеина у детей при ОРИ (общее число участников — 1080, возраст — от 2 месяцев до 13 лет, лечение получал 831 человек). Во всех исследованиях продемонстрирована клиническая эффективность ацетилцистеина: уменьшение количества эпизодов кашля к 6−7-м суткам, снижение частоты, интенсивности и продолжительности симптомов у детей с острыми заболеваниями как нижних, так и верхних дыхательных путей. Однако фактическая эффективность и в целом высокая безопасность ацетилцистеина продемонстрированы у детей в возрасте старше 2 лет. Оценка его безопасности у детей младше 2 лет затруднена вследствие недостаточного объема научных данных [11].
Ацетилцистеин выпускают в разнообразных лекарственных формах: для приема внутрь, ингаляций и инъекций, — что позволяет индивидуализировать его использование у детей разных возрастных групп, с различными заболеваниями. В амбулаторной практике чаще всего применяют сиропы, обладающие приятными органолептическими свойствами, для детей старше 2 лет можно рекомендовать АЦЦ® сироп (содержание ацетилцистеина — 20 мг/мл), не содержащий сахара, спирта и красителей.
Ацетилцистеин как муколитик предпочтителен при сочетанном поражении верхних и нижних дыхательных путей, симптомах риносинусита, поскольку он разжижает не только бронхиальный, но и вязкий назальный секрет, а также уменьшает воспаление благодаря антиоксидантному действию. Таким образом, один препарат позволяет педиатру решить сразу несколько задач [4, 11].
Препараты от кашля можно применять и с помощью небулайзеров, позволяющих доставить лекарственное средство непосредственно к месту воспаления. При этом необходимо помнить, что категорически не рекомендовано использовать в небулайзерах минеральную воду, масляные растворы и взвеси, в том числе отвары и настои трав.
ЗАКЛЮЧЕНИЕ
При выборе препаратов, влияющих на кашель при острой респираторной инфекции, необходимо учитывать не только патогенетические механизмы развития кашля и особенности детского организма в разные возрастные периоды, но и фармакологические свойства препаратов, показания к применению, данные клинических исследований. Назначение адекватной этиотропной, симптоматической и патогенетической терапии при респираторных инфекциях у детей способствует уменьшению выраженности симптомов, улучшению состояния пациентов и ускорению их выздоровления.
RU1702595015








