К аутоиммунным заболеваниям печени (АЗП) на сегодняшний день принято относить аутоиммунный гепатит (АИГ), первичный билиарный холангит (ПБХ) и первичный склерозирующий холангит. Этиология всех указанных заболеваний остается неизвестной.
ПБХ, ранее именовавшийся первичным билиарным циррозом, развивается преимущественно у женщин среднего возраста и представляет собой негнойный деструктивный холангит, сопровождающийся хроническим холестазом и портальным воспалением. При длительном течении ПБХ может приводить к цирротической трансформации печени и формированию печеночной недостаточности [1]. Среди женщин старше 40 лет заболеваемость ПБХ составляет 1 : 1000 [2].
Хронический вирусный гепатит B (ХГB) — опасное для жизни человека заболевание, вызываемое вирусом гепатита B (ВГB), которое без медицинского вмешательства может приводить к развитию цирроза и рака печени. ХГB является серьезной глобальной проблемой. По оценкам ВОЗ, на июль 2017 г. в мире насчитывалось не менее 257 млн человек, хронически инфицированных ВГB [3].
Хроническая ВГB-инфекция — динамичный процесс, в котором выделяют пять основных фаз (не всегда последовательно сменяющих одна другую): HBeAg-позитивная хроническая инфекция (I); HBeAg-позитивный хронический гепатит (II); HBeAg-негативная хроническая инфекция (III); HBeAg-негативный хронический гепатит (IV) и HBsAg-негативная фаза (V) [4].
HBsAg-негативную (V) фазу хронической ВГB-инфекции, которая характеризуется наличием в организме больного ДНК ВГB, выявляемой в сыворотке крови и/или ткани печени, при отсутствии в крови HBsAg, называют латентной ВГB-инфекцией (ЛВИ). Пациенты в этой фазе обычно имеют нормальные показатели АЛТ и очень низкую вирусную нагрузку в крови (как правило, не превышающую 200 МЕ/мл). ДНК вируса при ЛВИ чаще выявляется не в сыворотке крови, а в ткани печени.
Выделяют серопозитивный и серонегативный варианты ЛВИ. Серопозитивный вариант характеризуется наличием антител к HBcAg (anti-HBc), выявляемых одновременно с антителами к HBsAg (anti-HBs) или без них. При серонегативном варианте антитела к антигенам ВГB полностью отсутствуют.
Несмотря на то что ЛВИ впервые привлекла внимание специалистов более 40 лет назад (в связи со случаями реактивации гепатита В у больных, получавших химиотерапию) [5], на сегодняшний день представление о распространенности ЛВИ и ее клиническом значении у пациентов с АЗП можно получить лишь по единичным сообщениям. По имеющимся данным, в регионах, эндемичных по гепатиту В, ЛВИ может быть выявлена более чем у 12% пациентов с АЗП [6].
Учитывая тот факт, что пациенты с АЗП (особенно с АИГ) являются потенциальными кандидатами на получение иммуносупрессивной терапии, наличие у них ЛВИ может иметь важное клиническое значение в связи с риском реактивации гепатита В на фоне иммуносупрессии. При естественном течении ПБХ наличие ЛВИ, видимо, является неблагоприятным прогностическим признаком, ассоциирующимся с более агрессивным развитием заболевания и ускоренным прогрессированием фиброза [7].
Для иллюстрации клинического значения ЛВИ у пациентов с АЗП приведем собственное клиническое наблюдение, сделанное на базе Московского клинического научно-практического центра им. А. С. Логинова Департамента здравоохранения города Москвы (далее — ГБУЗ МКНЦ им. А. С. Логинова).
КЛИНИЧЕСКОЕ НАБЛЮДЕНИЕ
Описательная часть
Больная Н., 63 лет, в феврале 2018 г. повторно обратилась в отделение заболеваний печени МКНЦ им. А. С. Логинова с жалобами на выраженную общую слабость и дискомфорт в правом подреберье.
Из анамнеза известно, что в 1980 г. у пациентки в крови впервые обнаружили HBsAg, а затем — ДНК ВГB, которые в дальнейшем выявлялись до 2007 г. В указанный период по поводу диагностированного ХГB больная наблюдалась у инфекциониста по месту жительства (г. Тверь), противовирусной терапии не получала. В последующее десятилетие наблюдение прекратила, лабораторных исследований не выполняла.
В мае 2017 г. в связи с ухудшением самочувствия, появлением общей слабости и дискомфорта в правом подреберье пациентка обратилась за медицинской помощью. В клиническом анализе крови была отмечена легкая тромбоцитопения (52 × 109/л), при биохимическом исследовании — гипоальбуминемия (28 г/л), выявлено повышение уровней аминотрансфераз, щелочной фосфатазы и гамма-глутамилтранспептидазы. Маркеры вирусов гепатита В и С (HBsAg, ДНК ВГB, anti-HCV) не обнаружены. При эластометрии печени констатированы признаки цирроза печени (26 кПа, F4 по шкале METAVIR).
В августе 2017 г. пациентка была госпитализирована в отделение заболеваний печени МКНЦ им. А. С. Логинова, где (дополнительно к указанным изменениям) у нее в крови обнаружили антитела к антигенам мембраны митохондрий (АМА-М2 = 71 МЕ/мл); при УЗИ брюшной полости — спленомегалию и асцит 1-й степени; при эзофагогастродуоденоскопии (ЭГДС) — варикозное расширение вен пищевода 1-й степени (по N. Soehendra). HBsAg, anti-HCV не выявлены, тест на ДНК ВГB не проводился. На основании результатов обследования диагностирован цирроз печени в исходе первичного билиарного холангита (АМА-М2-позитивный). Рекомендован постоянный прием урсодезоксихолевой кислоты (УДХК) в дозе 1,5 г/сут.
В сентябре 2017 г. в клинической больнице № 122 г. Санкт-Петербурга пациентке была выполнена пункционная биопсия печени — обнаружены «гистологические признаки цирроза с холестазами», рекомендовано продолжить прием УДХК.
В октябре 2017 г. в одном из лечебных учреждений г. Твери изменения гистологической картины были расценены как синдром аутоиммунного перекреста (АИГ и ПБХ). Больной провели три сеанса плазмафереза, временно отменили УДХК, назначили глюкокортикостероиды (ГКС): преднизолон (90 мг/сут. — 7 дней, 60 мг/сут. — 2 дня), далее метилпреднизолон (20 мг/сут. с постепенным снижением дозы).
В декабре 2017 г. в связи с появлением фебрильной лихорадки, непродуктивного кашля и одышки пациентка была госпитализирована в городскую клиническую больницу № 6 г. Москвы, а затем переведена в пульмонологическое отделение МКНЦ им. А. С. Логинова, где в результате обследования диагностировали двустороннюю интерстициальную пневмонию. При проведении антибактериальной, муко- и бронхолитической терапии пневмония клинически и рентгенологически разрешилась.
В феврале 2018 г., учитывая возобновившиеся астенические проявления, пациентка была повторно госпитализирована в отделение заболеваний печени МКНЦ им. А. С. Логинова для уточнения диагноза и коррекции лечения.
Объективно (при поступлении): состояние удовлетворительное. Признаков печеночной энцефалопатии нет. Множественные сосудистые «звездочки» в зоне декольте, пальмарная эритема. Со стороны органов дыхания и сердечно-сосудистой системы — без значимых изменений. Живот обычных размеров, при пальпации мягкий, безболезненный. Симптомов раздражения брюшины нет. Перкуторно и методом зыбления признаков наличия свободной жидкости в брюшной полости не обнаружено. Печень на 3 см выступает из-под края реберной дуги, плотная, умеренно болезненная при пальпации. Селезенка не пальпируется. Поколачивание по поясничной области безболезненно с обеих сторон.
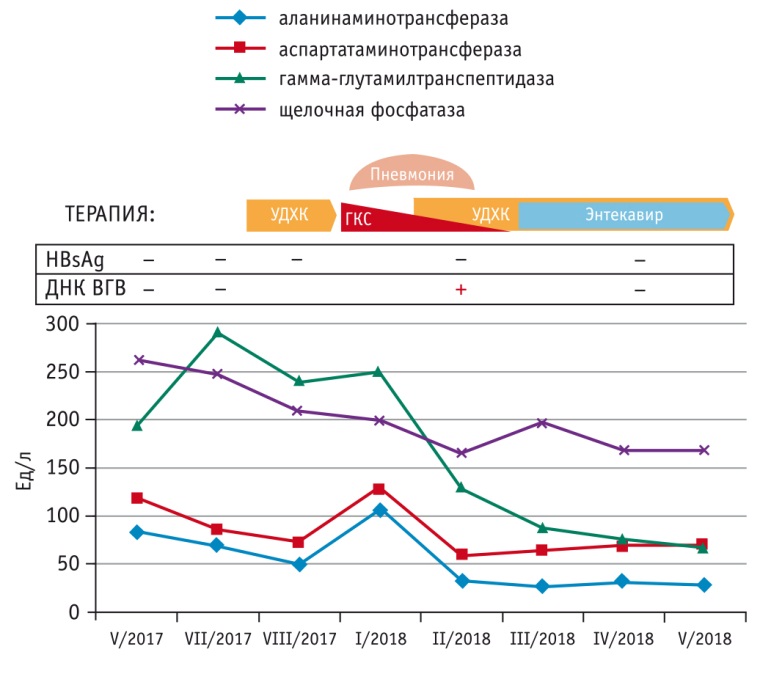
В результате лабораторно-инструментального обследования подтверждено наличие холестатического и цитолитического синдромов, гипоальбуминемии, тромбоцитопении, гепатоспленомегалии. Выявлено варикозное расширение вен пищевода и желудка 2-й степени. Несмотря на отрицательный результат повторного теста на HBsAg, в крови больной обнаружены anti-HBc и ДНК ВГB (< 150 МЕ/мл) (рис. 1).
Рис. 1. Динамика отдельных клинико-лабораторных показателей пациентки Н.
Примечание. ГКС — глюкокортикостероиды; УДХК — урсодезоксихолевая кислота
Проведена повторная оценка морфологической картины в биоптате печени пациентки Н. В препарате 4 столбика печеночной ткани длиной по 15 мм. Архитектоника печени нарушена. Широкие поля грубой волокнистой соединительной ткани разделяют группы гепатоцитов с формированием ложных долек. Среди пучков коллагеновых волокон расположены кровеносные и лимфатические сосуды различного калибра и гиперплазированные желчные протоки, окруженные скоплениями лимфоцитов. Деструкция мелких желчных протоков. Группы матово-стекловидных гепатоцитов, участки ацидофильной дистрофии гепатоцитов. Тельца Каунсильмена. Участки паренхиматозного холестаза. Выраженная гиперплазия клеток ретикулоэндотелиальной системы (рис. 2–4).
Рис. 2. Цирроз печени. Сформированные ложные дольки, разделенные фиброзными септами. Окраска гематоксилином и эозином, ув. × 400. Фото Филиппова С. А.
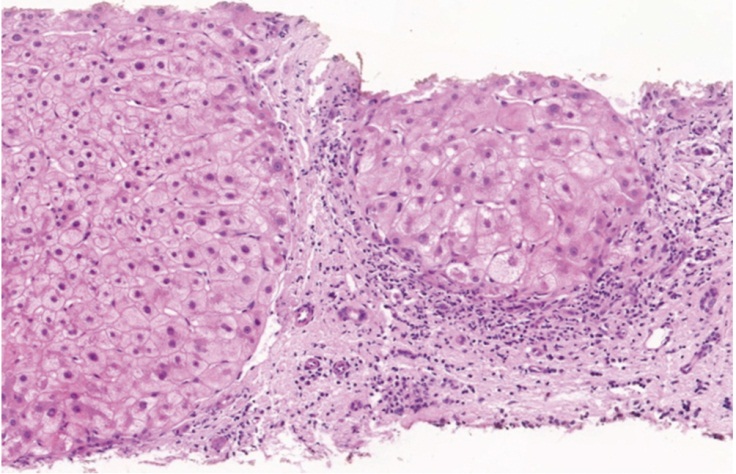
Рис. 3. Гиперплазированные желчные протоки, окруженные скоплениями лимфоцитов. Лимфоциты между эпителиоцитами протока. Окраска гематоксилином и эозином, ув. × 400. Фото Филиппова С. А.
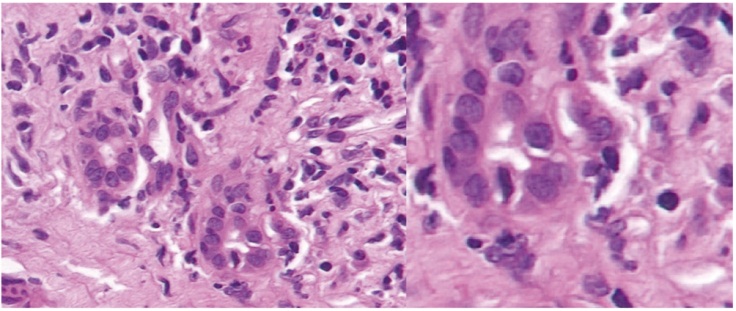
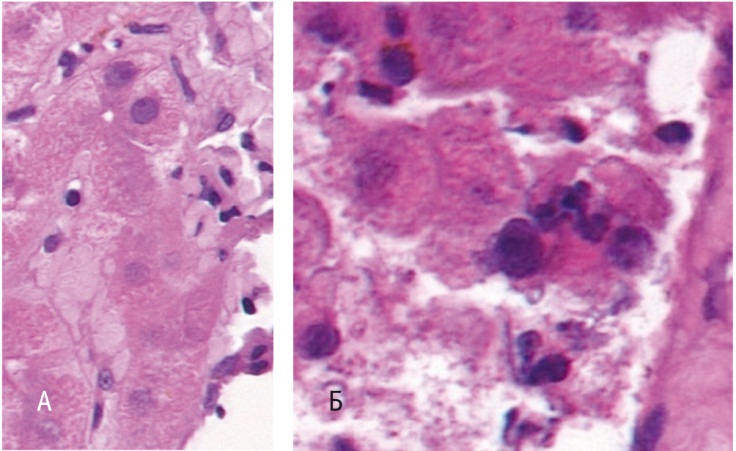
Рис. 4. Группы матово-стекловидных гепатоцитов (А), тельце Каунсильмена (Б). Окраска гематоксилином и эозином, ув. × 400. Фото Филиппова С. А.
Заключение: активный цирроз печени в исходе первичного билиарного холангита, протекающего на фоне хронического вирусного гепатита (вероятно, B-вирусной этиологии). Гистологических признаков аутоиммунного гепатита не обнаружено. METAVIR: A1, F4.
На основании результатов обследования выставлен окончательный диагноз. Цирроз печени смешанной этиологии (хронический вирусный гепатит В + первичный билиарный холангит), класс B (9 баллов) по Чайлду — Пью, 9 баллов по шкале MELD, с явлениями портальной гипертензии: варикозное расширение вен пищевода и желудка 2-й степени, спленомегалия, гиперспленизм (тромбоцитопения легкой степени).
Пациентке были отменены ГКС, в связи с реактивацией ВГB-инфекции назначена противовирусная терапия (энтекавир). В результате отмечено значительное улучшение самочувствия в виде уменьшения астенических проявлений, достигнуты авиремия, разрешение цитолитического синдрома, уменьшение холестаза.
Обсуждение
Характерными лабораторными признаками ПБХ считаются высокий уровень щелочной фосфатазы в сыворотке крови и наличие антител к антигенам мембраны митохондрий.
Из всех митохондриальных антигенов, распознаваемых антимитохондриальными антителами (АМА), наиболее специфичным является антиген М2. АМА к E2-субъединице пируватдегидрогеназного комплекса (АМА-М2) — высокочувствительный и специфичный маркер ПБХ, выявляемый более чем у 90% больных и менее чем у 1% здоровых взрослых людей. В АМА-серонегативных случаях диагностировать ПБХ помогает определение в крови ПБХ-специфичных антител (к антигенам gp210 и sp100) [8].
Визуализирующие исследования: УЗИ брюшной полости и магнитно-резонансная холангиопанкреатография (МРХПГ) — в диагностике ПБХ играют вспомогательную роль. УЗИ — первоочередное неинвазивное инструментальное исследование, выполняемое в основном для исключения механической обструкции желчных путей и дифференцирования внутри- и внепеченочного холестаза. МРХПГ проводят для четкой визуализации внутри- и внепеченочных желчных протоков.
При наличии типичной клинической картины, характерных лабораторных данных и отсутствии ультразвуковых признаков механической обструкции желчных путей ПБХ обычно диагностируется без проведения биопсии печени. Морфологическая верификация диагноза целесообразна при отрицательных результатах теста на АМА-М2, в случае необходимости уточнения стадии ПБХ и при наличии другой возможной причины хронического заболевания печени [9].
ЛВИ, характеризующаяся выявлением в сыворотке крови и/или ткани печени ДНК ВГB (при отсутствии в крови HBsAg), по некоторым данным, может быть обнаружена у 9% больных ПБХ [6]. Суррогатным маркером ЛВИ, позволяющим заподозрить наличие данной проблемы, являются anti-HBc (IgG).
В описанном нами клиническом случае пол и возраст пациентки, клинические проявления, данные лабораторно-инструментального обследования были достаточными основаниями для диагностирования цирроза печени в исходе ПБХ. Количество АМА-М2 (в 7 раз выше верхней границы нормы) в сочетании с выраженным повышением уровней щелочной фосфатазы и гамма-глутамилтранспептидазы (при отсутствии ультразвуковых данных, которые указывали бы на внутри- и внепеченочные объемные образования и заболевания желчного пузыря) позволяло с высокой вероятностью установить этиологию заболевания. На основании коэффициента де Ритиса, равного 1,5, наряду с гипоальбуминемией, тромбоцитопенией, высокой плотностью печени при эластометрии, признаками портальной гипертензии при ЭГДС и УЗИ возможно было адекватно оценить стадию процесса.
Несмотря на отсутствие в крови HBsAg и ДНК ВГB, сведения о ХГB в анамнезе позволяли предположить наличие у пациентки ЛВИ. Дополнительное основание для этого могло бы дать более раннее проведение тестирования с выявлением в крови anti-HBc.
Учитывая достаточность данных для установления верного диагноза, целесообразность выполнения биопсии печени, на наш взгляд, была сомнительной. К тому же неверная трактовка результатов гистологического исследования и пренебрежение отсутствием типичных для АИГ лабораторных признаков привели к выбору ошибочной лечебной тактики. Необоснованное назначение больной ГКС, очевидно, не только спровоцировало развитие у нее пневмонии, но и привело в реактивации ВГB-инфекции.
Средством выбора для лечения ПБХ в настоящее время считается УДХК, назначаемая в дозе 13–15 мг/кг/сут. пожизненно. При недостаточном ответе на УДХК для усиления терапевтического эффекта в дополнение к ней может быть назначена обетихолевая кислота. При непереносимости УДХК применение этого средства может служить альтернативным вариантом лечения. Убедительных данных, указывающих на целесообразность назначения иммуносупрессоров больным ПБХ, нет.
Хорошего эффекта от сочетания УДХК с иммуносупрессивной терапией можно ожидать в случае перекрестного синдрома АИГ-ПБХ, для диагностики которого рекомендуется использовать так называемые Парижские критерии. Отсутствие у больного ПБХ адекватного ответа на терапию УДХК может служить дополнительным аргументом в пользу наличия перекреста с АИГ [9].
Данные представленной нами пациентки не соответствовали критериям диагностики перекрестного синдрома АИГ-ПБХ. Незначительное повышение активности АЛТ, отсутствие аутоиммунных маркеров помимо АМА-М2, нормальный уровень IgG, доминирующие черты деструктивного холангита при морфологическом исследовании в сочетании с регрессом цитолиза и холестаза на фоне приема УДХК позволяли усомниться в наличии у больной перекреста с АИГ.
Вместе с тем данные анамнеза и характерные изменения гистологической картины (наличие матово-стекловидных гепатоцитов и телец Каунсильмена на фоне участков ацидофильной дистрофии гепатоцитов и выраженной гиперплазии клеток ретикулоэндотелиальной системы) должны были натолкнуть на мысль о присутствии ВГB (как компонента поражения печени) и о его роли в патогенезе заболевания.
Основной конечной точкой современных стратегий противовирусной терапии при ХГB является индукция долговременного подавления репликации ВГB. Показания к ней базируются на определении вирусной нагрузки (ДНК ВГB/мл), активности АЛТ и тяжести поражения печени (выраженности воспаления и фиброза) [4]. Противовирусная терапия больным ХГB обычно назначается во II или IV фазах инфекции, характеризующихся более активным течением заболевания с соответствующими изменениями лабораторных показателей и гистологической картины. Однако в «неактивные» III и V фазы также могут выявляться серьезные морфологические изменения («продвинутый» фиброз или цирроз печени), сформировавшиеся на предыдущих этапах заболевания, что в сочетании с выявляемой ДНК ВГB служит основанием для назначения противовирусных препаратов.
У больных, получающих иммуносупрессивную терапию, может происходить реактивация гепатита B вследствие потери контроля иммунной системы над инфекцией. Критерием реактивации у пациентов с ЛВИ является появление в крови HBsAg и/или ДНК ВГB. Реактивация может приводить к выраженному ухудшению течения хронического заболевания печени, резкому усилению гепатита вплоть до развития острой печеночной недостаточности и летального исхода [10].
Риск реактивации гепатита В у пациентов с ЛВИ, получающих иммуносупрессивную или химиотерапию, известен. HBsAg-негативные/anti-HBc-позитивные пациенты, получающие умеренные (10–20 мг/сут.) или высокие (> 20 мг/сут.) дозы преднизолона (или их эквивалент) 4 недели и более, относятся к группе умеренного риска. Частота реактивации у них составляет 1–10% [11].
Считается, что обычно нет необходимости в превентивном назначении противовирусной терапии таким пациентам. Во время и после иммуносупрессии целесообразно проводить активный лабораторный мониторинг (с определением HBsAg и/или ДНК ВГB в сыворотке крови каждые 1–3 месяца) и назначать аналоги нуклеоз(т)идов (энтекавир или тенофовир) в случае серореверсии по HBsAg или выявления ДНК ВГB (независимо от вирусной нагрузки и уровня АЛТ) [4, 12].
Своевременное выявление у больной реактивации ЛВИ на фоне приема ГКС (с появлением в крови ДНК вируса) и назначение ей противовирусной терапии, очевидно, играли значимую клиническую роль, поскольку предотвращенное таким образом обострение вирусного гепатита (на фоне имеющегося цирроза печени) могло иметь тяжелые последствия.
ЗАКЛЮЧЕНИЕ
Приведенный нами клинический случай наглядно демонстрирует, что латентная инфекция вирусом гепатита B (ВГB) у пациентов с аутоиммунным заболеванием печени (АЗП) может иметь важное клиническое значение. Роль латентной ВГB-инфекции (ЛВИ) в патогенезе АЗП в целом и первичного склерозирующего холангита в частности нуждается в дальнейшем изучении. Не исключено, что ВГB-инфекция, даже протекающая в скрытой (латентной) форме, может выступать фактором, провоцирующим развитие АЗП.
Больным АЗП целесообразно выполнять скринирование на наличие ЛВИ. При назначении иммуносупрессивной терапии пациентам с АЗП и наличием антител к HBcAg в крови следует проводить активный лабораторный мониторинг (ежемесячное определение HBsAg и/или ДНК ВГB в сыворотке крови), имея в виду вероятность реактивации гепатита В с возможным последующим ухудшением течения заболевания.







