Для диагностики фиброза при алкогольной болезни печени (АБП) используются инвазивные и неинвазивные методы исследования. В статье освещено современное состояние проблемы, проведен анализ литературы для оценки диагностической точности неинвазивных методов, представлены данные оригинального исследования корреляции показателей непрямой ультразвуковой эластографии с результатами пункционной биопсии печени (ПБП).
Во всем мире в 2016 г. употребление алкоголя явилось седьмым по значимости фактором как для риска смерти, так и для причин потери лет жизни (DALY — 13,6%), стандартизированная по возрасту смерть 2,2% женщин и 6,8% мужчин была связана с употреблением алкоголя. По данным на 2016 г., 32,5% населения Земли (2,4 млрд людей) хронически злоупотребляли алкоголем, во всем мире 2,8 млн смертей были связаны с употреблением алкоголя.
Среднестатистический показатель потребления стандартных доз алкогольных напитков (10 г чистого этилового спирта в день приняты за 1 единицу) в России составил для женщин 2,01-3, для мужчин 3,01-4 [1-4]. По данным ВОЗ, с 1990 по 2014 г. на территории РФ, Беларуси, Молдовы и Украины на 22% выросла смертность, ассоциированная с последствиями злоупотребления алкоголем. Официальная статистика РФ показывает, что алкоголь входит в число основных факторов риска смерти в российской популяции, его доля — 11,9%.
Стоит отметить, что причиной смерти от заболеваний органов пищеварения в 50-80% случаев послужил цирроз печени, преимущественно алкогольной и вирусной этиологии [5]. В Москве проведено скрининговое обследование на болезни печени среди случайно выбранных 5000 жителей, по результатам которого распространенность АБП в популяции составляет 6,9% [6]. По данным Национального института проблем злоупотребления алкоголем и алкоголизма США, в 44-48% случаев цирроз, приведший к смертельному исходу, обусловлен токсическим воздействием алкоголя [7].
ДИАГНОСТИКА АЛКОГОЛЬНОЙ БОЛЕЗНИ ПЕЧЕНИ
АБП — клинико-морфологическое понятие, включающее несколько вариантов повреждения паренхимы печени вследствие злоупотребления алкоголем — от стеатоза до алкогольного гепатита (стеатогепатита), приводящего к развитию последовательных стадий — фиброза, цирроза и гепатоцеллюлярной карциномы.
Гепатотоксичные дозы алкоголя: для мужчин — более 40-80 г/сут в пересчете на чистый этанол; для женщин — более 20 г этанола в сутки [5].
ПБП — инвазивный метод диагностики, в настоящее время он является «золотым стандартом» для оценки активности и стадии поражения ткани печени, эффективности проведенной терапии АБП. Однако до настоящего времени в России не разработаны нормативные документы, позволяющие регламентировать проведение данной манипуляции. К возможным осложнениям в результате биопсии печени можно отнести вазовагальные реакции с преходящей гипотонией, внутрипеченочные кровотечения, сообщалось также о случаях хилоперетонеума, перфорации кишечника, сепсисе [8]. Важно помнить, что результаты морфологической оценки биоптата печени зависят от опыта и квалификации морфолога, его способности объективно описать и дать количественную оценку морфологических признаков. Причинами ошибок могут стать и отсутствие преемственности в работе лечащего врача и морфолога, нарушение правил забора биоптата [9].
С учетом вышесказанного весьма актуальным остается вопрос об оценке стадии заболевания (выраженности фиброза) при АБП неинвазивными методами [10], которые включают определение уровней сывороточных маркеров и другие лабораторные тесты, а также методы визуализации. Сывороточные маркеры фиброза делятся на прямые и непрямые.
Прямые маркеры являются фрагментами компонентов печеночного матрикса, вырабатываемыми звездчатыми клетками печени в ходе фиброгенеза, и молекул, участвующих в регулировании прогресса и регресса фиброза.
-
Гиалуроновая кислота входит в состав гликозаминогликана экстрацеллюлярного матрикса (ЭЦМ). В ходе исследований для нее была показана наиболее высокая корреляция с гистологическими результатами фиброза печени [11, 12].
-
Карбокситерминальный пропептид проколлагена I типа и аминотерминальный пропептид проколлагена III типа (PIIINP), проколлаген VI типа. В процессе фиброгенеза содержание коллагена I типа увеличивается в несколько раз. PIIINP — важная составляющая соединительной ткани. Его относительная концентрация в базальной мембране выше при печеночном фиброгенезе, что, в свою очередь, сопровождается повышением его уровня в сыворотке крови [11, 13].
-
Металлопротеиназы (ММП) образуют семейство структурно связанных между собой протеолитических ферментов, которые участвуют в деградации ЭЦМ и базальной мембраны, увеличение их уровня наблюдается при различных заболеваниях печени. Тканевые ингибиторы ММП-1 (ТИМП-1) — это секретируемые белки, взаимодействующие с ММП и модулирующие их активацию и функционирование. ТИМП-1 контролирует активность большинства ММП, в то время как ТИМП-2 специфически ингибирует ММП-2. ТИМП-зависимое ингибирование деградации ЭЦМ может способствовать развитию фиброза печени. Повышение уровня ТИМП наблюдается при хронических заболеваниях печени [14].
Непрямые маркеры (тромбоциты, АСТ, МНО, γ-глутамилтрансфераза (ГГТ), билирубин, альбумин, холестерин) — показатели, которые отражают функциональное состояние печени, но не имеют прямой корреляции с уровнем отложения внеклеточного матрикса и косвенно позволяют судить о стадии фиброза.
У больных с хроническими заболеваниями печени и циррозом, независимо от его этиологии, имеется нарушение баланса в прокоагулянтной системе. Тромбоцитопения, характерная для пациентов с циррозом печени, обусловлена повышенной секвестрацией тромбоцитов в селезенке в результате спленомегалии, уменьшением уровней трех основных антикоагулянтов: протеина С, протеина S и антитромбина III. У таких больных часто снижено количество тромбоцитов в легкой (50-100 × 109 в мл) или умеренной (20-50 × 109 в мл) степени. Однако при этом на фоне «естественной гипокоагуляции» может возникать широкий спектр спонтанных (или неспровоцированных) венозных тромботических осложнений [15].
ГГТ отражает ферментативную активность печени, однако повышение ее уровня возможно при патологии билиарной системы, сердечной патологии, приеме некоторых лекарственных препаратов. Алкоголь стимулирует экспрессию гена ГГТ. Активность сывороточной ГГТ повышена примерно у 75% лиц, злоупотребляющих алкоголем (чувствительность — 60-90%, специфичность — 50-72%) [2].
АСТ и АЛТ — белковые вещества, участвующие в обменных процессах, в частности аминокислотных. Данные ферменты вырабатываются внутриклеточно, поэтому повышение их содержания в крови свидетельствует о разрушении клеточных структур. При многих формах острого и хронического поражения печени, при стеатозе АСТ/АЛТ меньше или равно 1, а при алкогольном гепатите это отношение часто превышает 2 [16].
Гипербилирубинемия может выступать показателем печеночной недостаточности. При нарастании тяжести АПБ часто отмечается уровень билирубина > 50 мкмоль/л [17].
Комбинации сывороточных тестов, используемых для диагностики фиброза печени, называются диагностическими индексами (панелями). Основные диагностические индексы, применяющиеся на практике (высокоинформативные для АБП):
-
FibroTest (α2-макроглобулин, гаптоглобин, ГГТ, аполинопротеин (АроА1), билирубин, пол, возраст);
-
FibroSpect (α2-макроглобулин, гиалуроновая кислота и ТИМП-1);
-
Hepascore (билирубин, ГГТ, гиалуроновая кислота, α2-макроглобулин, возраст, пол);
-
FibroMeter (количество тромбоцитов, протромбиновый индекс (ПИ), АСТ, гиалуроновая кислота, α2-макроглобулин, мочевина, возраст);
-
AshTest (ГГТ, АЛТ, общий билирубин, α2-макроглобулин, ApoА1, гаптоглобин с уровнем АСТ, возраст, пол);
-
индекс PGAA (ПИ, ГГТ, ApoA1 и α2-макроглобулин).
В ходе исследования показано, что при значениях FibroTest ниже 0,58 можно говорить о том, что прогрессирующего фиброза печени нет (стадия Клейнера ≥ F3) с диагностической точностью 94% [18]. FibroTest имеет высокую диагностическая ценность с площадью под ROC-кривой (AUROC), достигающей 0,94.
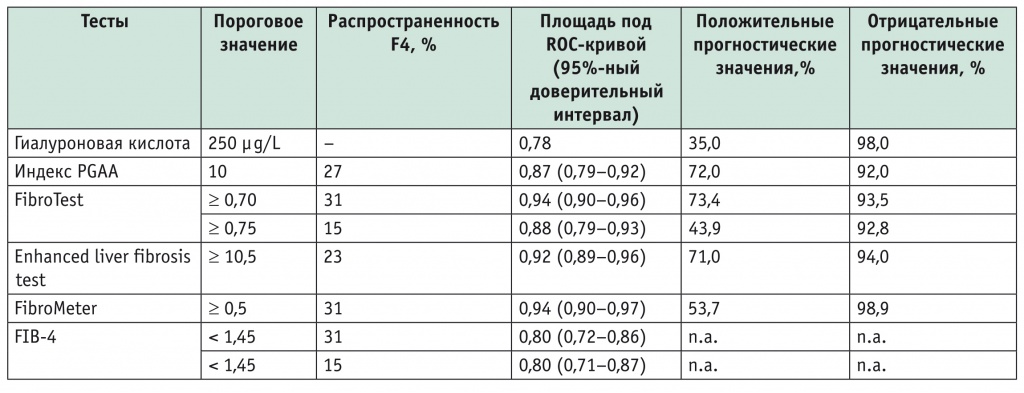
По данным исследований, при диагностике выраженного фиброза и цирроза диагностическая точность FibroTest, FibroMeterA и Hepascore в целом не отличалась при выраженном фиброзе (AUROC около 0,80) и циррозе (AUROC около 0,90), однако была выше, чем у APRI, Forns и FIB-4. Наиболее точным и прогностически значимым оказался FibroTest (табл. 1) [17, 18].
Таблица 1
Диагностическая эффективность некоторых неинвазивных тестов сывороточных маркеров фиброза для диагностики цирроза у пациентов с алкогольной болезнью печени [17]
МЕТОДЫ ВИЗУАЛИЗАЦИИ ПЕЧЕНИ
В клинической практике используются МРТ, КТ, УЗИ, непрямая ультразвуковая эластография печени. К плюсам данных методов можно отнести их высокую доступность, неинвазивность, возможность применения для скрининга на ранних этапах поражения печени. Эти методы позволяют количественно определить стеатоз, исключить другие причины поражения печени (например, первичный склерозирующий холангит), выявить признаки выраженного фиброза/цирроза и их осложнений. Ультразвуковая диагностика в качестве рутинного метода для оценки стадии фиброза обладает низкой чувствительностью и специфичностью, особенно на начальных стадиях фиброза, так же, как при степени стеатоза менее 20-30% объема ткани печени [17]. МРТ и МР-спектроскопия являются надежными инструментами для оценки количества стеатоза и могут обнаружить 5-10% стеатоза, но важно помнить, что методы стандартизации этих исследований еще не разработаны, а высокая стоимость и низкая доступность ограничивают их применение [19, 20].
Эластография
В 1991 г. J. Ophir и соавт. предложили использовать термин «эластография» (от лат. elasticus — упругий) для обозначения количественного метода визуализации биологических тканей [21]. Правильнее употреблять термин «эластометрия», так как в процессе исследования анализируется среднее значение показателей эластичности печени, а не визуальное изображение органа. Но в настоящее время за рубежом чаще используют термин «эластография», чем «эластометрия».
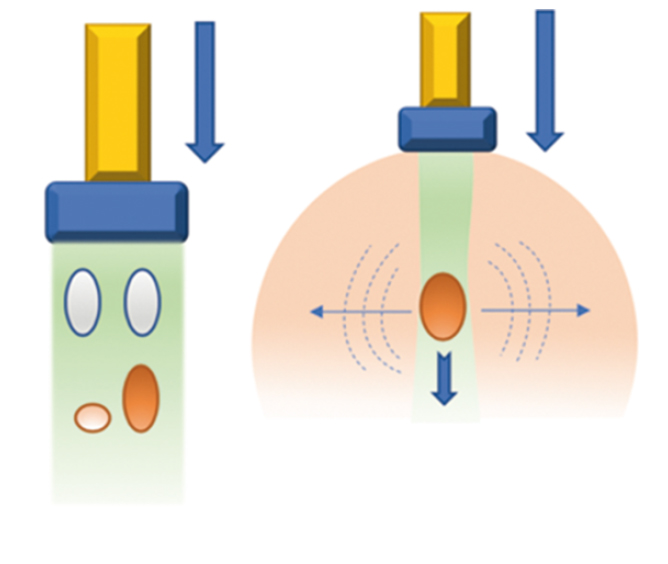
Компрессионная эластография оценивает деформацию тканей, соотношение величин деформации в разных участках области исследования. С помощью данного метода исследуют поверхностно расположенные органы. Компрессия производится линейным датчиком, что позволяет обеспечить деформацию тканей. Менее упругий, мягкий объект уменьшится в объеме сильнее, чем более упругий. На информативность метода влияет ряд условий (рис. 1):
-
«правило перпендикулярности» — плоскость сканирования находится под углом 90° к плоскости исследования;
-
«правило параллельности» — плоскость рабочей поверхности датчика параллельна плоскости исследования;
-
исследование выполняется на неподвижной твердой поверхности.
Рис. 1. Компрессионная эластография
Динамическая эластография основана на сдвиговых волнах — поперечных упругих волнах, которые распространяются в основном в твердых телах. В мягких биологических тканях при определенных условиях они также могут возникать в силу особых (резиноподобных) свойств биологических тканей, обусловленных вязкостью. Смещение частиц среды и сопутствующая этому деформация среды происходят в поперечном направлении относительно направления распространения волны. Если в направлении излучения ультразвукового датчика создать в узкой области давление определенного уровня, то в поперечном направлении возникает и начинает распространяться сдвиговая волна. Следовательно, скорость будет возрастать пропорционально упругости ткани. Существуют механический (аппарат Фиброскан, Echosens, Франция) и электронный (аппараты Aixplorer, SuperSonic Imagine, Франция, и Ultima, фирма «Радмир», Украина) способы генерации данных волн.
В ходе динамической эластографии применяются следующие виды давления:
-
механическое импульсное или вибрационное, с использованием сдвиговых волн, возникающих при этом (транзиентная эластография);
-
акустическое радиационное, создаваемое длинным ультразвуковым сигналом и оценкой получающихся продольных деформаций;
-
акустические радиационные импульсы, создаваемые ультразвуковыми сигналами, сфокусированными на разной глубине с использованием оценки скорости сдвиговых волн.
С помощью компрессионных методов получают только качественные (или сравнительные количественные) характеристики жесткости тканей, тогда как методы с применением сдвиговых волн позволяют оценить количественно модуль Юнга [22-24].
Непрямая ультразвуковая эластография печени (фиброэластометрия) — это пульс-Эхо-УЗ-методика оценки характера, скорости распространения колебаний для определения эластичности ткани печени.
К преимуществам данного метода можно отнести:
-
легкость выполнения исследования;
-
отсутствие ограничения трудоспособности пациентов;
-
минимальные временны́е и материальные затраты (в среднем занимает 5-7 мин, для его проведения не требуются дополнительные расходные материалы, кроме геля для УЗИ).
Ограничения метода непрямой ультразвуковой эластографии печени с использованием сдвиговых волн — аппарат-зависимые факторы, оказывающие влияние на качество и достоверность получаемых данных:
-
избыточная масса тела, слой подкожно-жировой клетчатки;
-
узкие межреберные промежутки;
-
наличие асцита, приводящее к невозможности распространения механической волны на ткань печени через слой жидкости;
-
повышение внутрибрюшного давления (метеоризм, напряжение пресса, тесная одежда на животе, гастростаз и обильный прием пищи);
-
быстрые смещения органа (близость некоторых участков печени к сердцу, аорте, диафрагме) [23].
Пороговые значения и корреляция показателей непрямой ультразвуковой эластографии с результатами пункционной биопсии печени
Ч.С. Павлов и соавт. провели метаанализ пяти ретроспективных и девяти проспективных когортных исследований с участием 834 пациентов, в которых применялись пороговые значения от 7,15 до 34,9 кПа. Чувствительность и специфичность непрямой ультразвуковой эластографии с пороговым значением около 7,5 кПа (от 7,00 до 7,8 кПа) составила 0,94 и 0,89 для выявления фиброза начиная со стадии F2. Значения от 9,5 кПа (диапазон от 8,0 до 11,0 кПа) с чувствительностью и специфичностью 0,92 и 0,70 позволяли предположить наличие тяжелого фиброза печени F3. О стадии фиброза F4 (цирроз печени) с чувствительностью 0,95 и специфичностью 0,71 свидетельствовали значения более 12,5 кПа [25].
На базе Клиники пропедевтики внутренних болезней, гастроэнтерологии и гепатологии им. В.Х. Василенко ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» и гастроэнтерологического отделения Мордовской Республиканской клинической больницы (г. Саранск) проведено когортное проспективное исследование, включавшее 90 пациентов (19 женщин и 71 мужчину).
Диагноз у всех участников ставился на основании анамнеза — злоупотребление алкоголем более 5 лет (в дозах более 24 г/сут для мужчин и более 16 г/сут для женщин). Подтверждение поражения печени основывалось на гистологических данных, полученных после проведения пункционной биопсии. ПБП была выполнена в кабинете биопсии клиники профессором Ч.С. Павловым и кандидатом медицинских наук Ш.А. Ондосом.
Выраженность фиброза печени в образцах печеночной ткани рассчитывалась с помощью системы МЕТАVIR: F0 — отсутствие рубцов, F1 — минимальное рубцевание, F2 — рубцевание имеет место и выходит за области печени, содержащие кровеносные сосуды, F3 — мостовидный распространяющийся фиброз, фиброзные участки соединяются между собой, F4 — цирроз или глубокое рубцевание печени.
Все морфологические исследования проведены доцентом кафедры патологической анатомии ФГАОУ ВО «Первый МГМУ им. И.М. Сеченова» Т.П. Некрасовой. Всем пациентам за день до биопсии проводилась фиброэластометрия на аппарате Фиброскан.
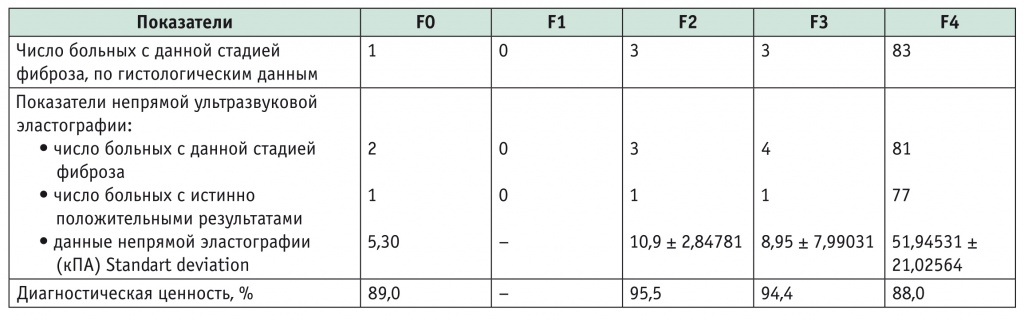
Слепым методом проведена сравнительная оценка диагностической точности фиброэластометрии в диагностике степени фиброза печени у пациентов с АБП. Сопоставляли данные, полученные при непрямой ультразвуковой эластографии (индекс-тест), и результаты гистологического исследования биоптатов печени (референс-стандарт) (табл. 2). Стадия фиброза F0 наблюдалась у 2, F2 — у 3, F3 — у 4, F4 — у 81 больного, F1 не выявлена. Для стадии F2 получена чувствительность 33%, специфичность — 97,7%, для стадии F3 чувствительность — 33%; специфичность — 96,5%, для стадии F4 чувствительность — 92,7%, специфичность — 42%.
Таблица 2
Сравнение результатов непрямой ультразвуковой эластографии и гистологического исследования биоптатов печени
Совпадение стадии фиброза, определенной по результатам непрямой ультразвуковой эластографии, с таковой по результатам морфологического исследования биоптата печени наблюдалось у 80 из 90 обследуемых.
ЗАКЛЮЧЕНИЕ
Сравнение результатов непрямой ультразвуковой эластографии с данными морфологического исследования — «золотого стандарта» оценки выраженности фиброза печени — показало, что высокой диагностической точностью она обладает при стадиях фиброза F3-F4.
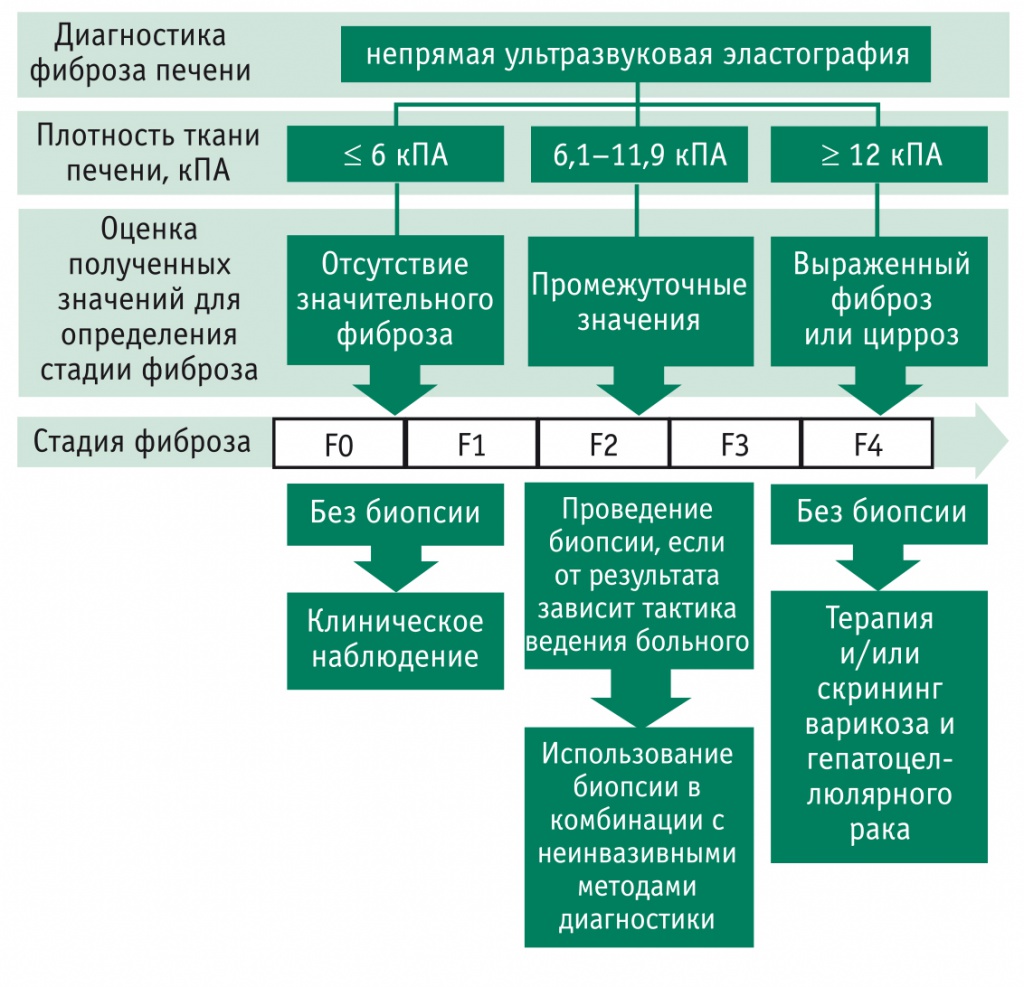
По результатам нашего исследования и с учетом мнения зарубежных экспертов мы предлагаем алгоритм использования непрямой ультразвуковой эластографии для оценки стадии фиброза у пациентов с алкогольной болезнью печени и выбора дальнейшей тактики лечения и ведения пациентов (рис. 2). У пациентов с плотностью печени до 6 кПА можно говорить о стадии фиброза F0-F1, которая требует дальнейшего клинического наблюдения без проведения биопсии. Полученные промежуточные значения (от 6,1 до 11,9 кПА) свидетельствуют о прогрессировании фиброза и диктуют необходимость пункционной биопсии печени в сочетании с использованием неинвазивных методов для определения тактики лечения. Плотность ткани более 12 кПА говорит о выраженном фиброзе или циррозе печени (стадия F4), в данном случае проведение биопсии нецелесообразно, однако требуется дополнительное обследование для исключения осложнений.
Рис. 2. Выбор метода диагностики стадии фиброза при алкогольной болезни печени