Проблема психического здоровья военнослужащих рассматривается как один из основных факторов национальной безопасности государства и боевой готовности вооруженных сил. Поэтому повышение качества комплектования войск, совершенствование системы психиатрической помощи и психопрофилактической работы относятся к числу важнейших общегосударственных задач. При этом ведущее значение приобретают мероприятия профилактической направленности, прежде всего в рамках систем отбора военнослужащих и мониторинга их психического здоровья. Вместе с тем существенным препятствием для их оптимизации являются особенности организации психодиагностической работы в воинской части, представляющей собой довольно сложный и запутанный алгоритм взаимодействия военных психиатров с различными должностными лицами. Это обусловлено отсутствием простых и надежных инструментов для выявления военнослужащих из групп риска, вследствие чего требуется преодоление низкой валидности существующих методик раннего обнаружения и прогнозирования психических нарушений за счет получения дополнительной информации от смежных специалистов: психологов, офицеров по работе с личным составом, командиров подразделений и т. п.
Так, прогностическая ценность результата при оценке риска развития психических расстройств на базе показателя нервно-психической устойчивости составляет всего 6,0%[1]. Наблюдаются значительные расхождения между частотой выявления склонности к девиантному поведению в ходе медицинского освидетельствования при призыве (0,96%) и по данным проспективных исследований (14,3%)[2]. В целом ретроспективная оценка использования различных тестов, шкал, опросников и т. п. в рамках психопрофилактических обследований показала, что, несмотря на высокий процент «отсеивания», их результативность была неудовлетворительной, а единственный пункт, обладающий достаточной прогностической ценностью, — это ответ на вопрос: «Имеете ли Вы психическое расстройство или обращались ли за психиатрической помощью в течение последних 6 месяцев?»[3].
Очевидно, что такие обескураживающие результаты, особенно в контексте широко известного эксперимента Розенхана[4], поддерживают сложившийся не только в общественном сознании, но и в медицинских кругах устойчивый стереотип предубежденного и настороженного отношения к психиатрии, в рамках которого широко распространено мнение, что «психиатрия и основной ее метод исследования — клинико-психопатологический — субъективны и ненаучны, получаемые результаты недостоверны, а диагностические заключения произвольны»[5].
В качестве узлового пункта данной проблемы В. П. Самохвалов[6] выделяет отсутствие наглядных, иконических знаков, доступных объективной регистрации, т. е. соответствующих «золотому стандарту» диагностики. Психопатологический метод не может претендовать на этот «стандарт», поскольку имеет концептуальные ограничения, связанные с проблемой двойного субъективизма: затруднения вербализации собственных переживаний у пациента в силу отсутствия специфических терминов в лексиконе и искажения смысла в ходе анализа врачом полученной от пациента информации[7] вследствие имманентной (в Кантовском понимании) полисемии. В связи с этим понятия, характеризующие диагностику, т. е. информативность, различительная способность, надежность и воспроизводимость, могут здесь восприниматься лишь в контексте грустной иронии. Вероятно, поэтому существенный сдвиг в сторону биологического редукционизма наблюдается в структуре анонсированного в 2013 г. проекта Research Domain criteria[8].
Возможно, в этом же русле следует вести поиск объективных маркеров психических расстройств, имеющих ключевое значение для оптимизации системы отбора военнослужащих и мониторинга их психического здоровья. С данной точки зрения особый интерес представляет этологическое изучение проявлений актуальных для военной психиатрии психических расстройств в невербальном поведении в рамках эволюционной парадигмы[6, 9, 10], уже доступных инструментальной регистрации с помощью технологии машинного зрения, а также определение биохимических, прежде всего с позиций моноаминовой гипотезы, психофизиологических (например, выявляемых с помощью пиктополиграфического метода[11]) и нейровизуализационных (в рамках концепции коннектопатий[12]) маркеров психических нарушений, анализ которых для объективизации различных психических расстройств и явился целью настоящей работы.
МАТЕРИАЛЫ И МЕТОДЫ
В этологической части исследования обследованы 85 мужчин и 38 женщин (средний возраст — 33,2 ± 11 года) с расстройствами шизофренического спектра (выборка 1). Произведена аудио- и видеофиксация стандартизированного психодиагностического интервью из 33 вопросов с помощью видеокамеры Canon XA30 с частотой кадров 30/мин. Контрольную группу составили 18 здоровых лиц. Покадровая разметка видеозаписей проводилась с помощью специализированного программного обеспечения для обработки изображения и распознавания мимики и жестов ООО НПП «Видеомикс» с выделением элементарных и простых комплексов поведения в соответствии с глоссариями В. П. Самохвалова[6] и Г. Е. Крейдлина[13], фонетический анализ — с помощью программы PRAAT[14].
В биохимической части исследования обследованы 20 больных (выборка 2) с депрессивным эпизодом (ДЭ) умеренной тяжести (F32.1), 20 с пролонгированной депрессивной реакцией (F43.21) и 25 с кратковременной смешанной тревожной и депрессивной реакцией (F43.22). Концентрацию серотонина тромбоцитов определяли методом иммуноферментного твердофазного анализа (ИФА) с помощью наборов реактивов Serotonin ELISA, кортизола — методом ИФА с использованием набора реагентов «СтероидИФА-кортизол».
Пиктополиграфический метод исследования основан на технологии автодокументирования действий испытуемого и обеспечивает проведение психодиагностического исследования на специальном графическом сенсорном планшете, позволяя получить профили смысло-эмоциональной значимости (СЭЗ) на основе анализа психомоторных показателей испытуемого при выполнении сценария исследования дополнительно к стандартным результатам тестирования. Материалом этой части работы стали результаты обследования 35 военнослужащих с расстройствами адаптации (РА) (F43.2), 18 с донозологическими формами психологических реакций (ДФПР) и 20 с умеренным ДЭ в соответствии с критериями МКБ-10 (выборка 3). Помимо клинико-психопатологического метода, использовались шкалы Гамильтона для оценки депрессии (Hamilton Rating Scale for Depression, HDRS) и тревоги (Hamilton Anxiety Rating Scale, HARS) и Госпитальная шкала тревоги и депрессии (Hospital Anxiety and Depression Scale, HADS). Пациентам с РА и умеренным ДЭ также предъявлялся психофизиологический стресс-тест на АПК «РЕАКОР» (НПКФ «Медиком МТД»). В качестве стресс-стимулов использовали валидизированные на здоровых военнослужащих видео- и аудиоматериалы.
Эталонным стресс-стимулом была электростимуляция тыльной поверхности предплечья. В период проведения процедуры измеряли частоту сердечных сокращений (ЧСС), кожно-гальваническую реакцию (КГР), фотоплетизмограмму, рекурсию дыхания.
Исследование морфофункциональных характеристик головного мозга проведено 302 пациентам с депрессивными расстройствами реактивного (F43), эндогенного (F20, F25, F31–33) и органического (F06.3) генеза (выборка 4), которым выполнялись позитронно-эмиссионная томография (ПЭТ) и МРТ в различных режимах структурной и функциональной нейровизуализации: воксельная морфометрия (VBM), диффузионно-тензорная визуализация (DTI), функциональная МРТ (фМРТ) и магнитно-резонансная спектроскопия. С помощью фМРТ обследовали также 20 человек с синдромом зависимости от опиоидов (в состоянии интоксикации опиоидами и в состоянии ремиссии до 1 месяца, средний возраст больных — 28,3 ± 3,7 года, стаж наркотизации — более 9 лет) и 18 здоровых лиц (контрольная группа). ПЭТ проводили на томографах Ecat Exact 47, Ecat Exact HR± и Biograph (Siemens, Германия), МРТ — на сканере Magnetom Symphony (Siemens, Германия) с индукцией магнитного поля 1.5 Tесла.
Статистическая обработка данных осуществлялась с помощью Statistical Parametric Mapping 12 в программной среде MATLAB и протокола FMRIB's Diffusion Toolbox. Результаты исследований сопоставлялись с данными клинической и психометрической (по HDRS) оценки состояния. Различия считали статистически значимыми при р < 0,05.
РЕЗУЛЬТАТЫ И ОБСУЖДЕНИЕ
Результаты этологической части исследования показали, что, несмотря на выраженные межиндивидуальные различия, даже простой сравнительный анализ выявляет значимые отличия в объеме поведенческих реакций у больных с расстройствами шизофренического спектра от здоровых лиц (табл.), прежде всего в частоте мимических движений и в характеристиках взгляда.
Таблица
Усредненные показатели интенсивности поведенческих реакций больных с расстройствами шизофренического спектра и здоровых лиц, кадры/мин (M ± σ)
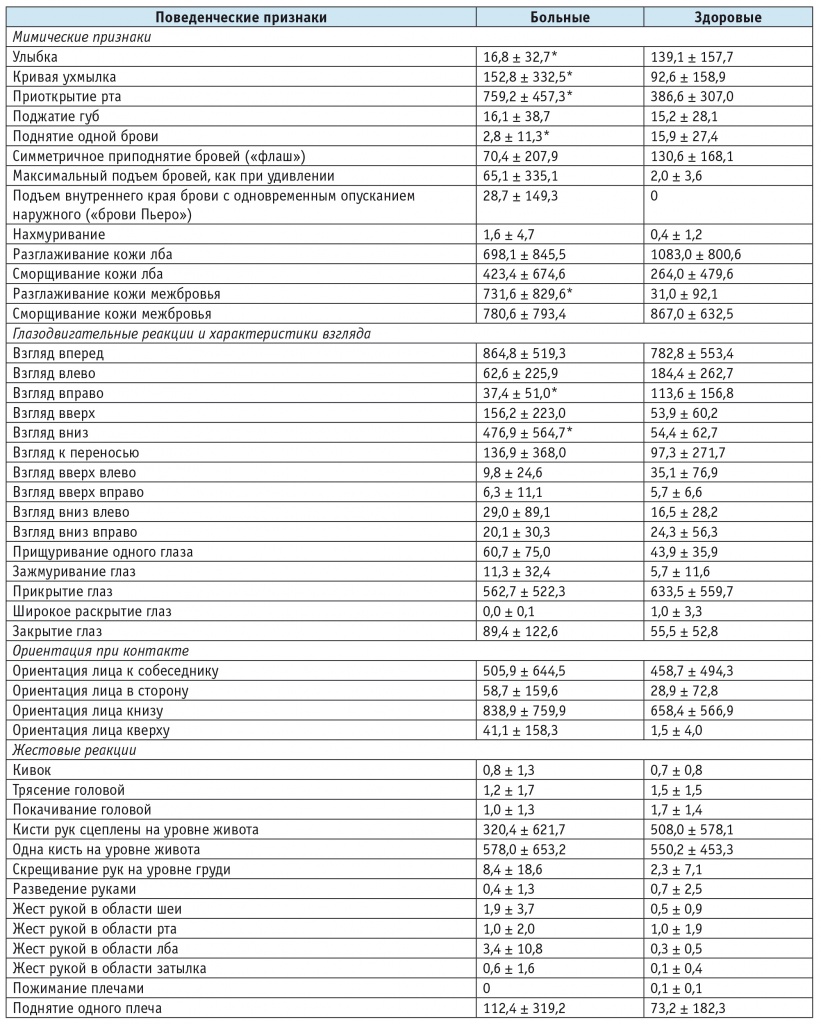
* Отличие от контрольной группы статистически значимо (p < 0,05).
Следует также указать, что использование поведенческих признаков в качестве переменных при расчете линейных дискриминантных функций позволило получить 100% точность решающих правил для здоровых и больных, при этом в уравнения вошли такие показатели, как разглаживание и сморщивание кожи межбровья, приоткрытие рта, направление взгляда вправо и вправо вниз, разведение руками, приподнятие бровей, покачивание головой, скрещивание рук на уровне груди.
Можно ожидать сходных различий в скоростных и амплитудных показателях поведенческих паттернов, в характере последовательности реакций, рассчитываемом на базе цепей Маркова, латентного семантического анализа и т. п., равно как и в объективных характеристиках устной речи (как фонетических, так и психолингвистических), однако эти показатели в силу их значительного объема заслуживают освещения в отдельной работе.
Очевидно, что характерный для больных шизофренией стиль поведения, отличный от прогнозируемого в норме, способен вызывать определенный дискомфорт у собеседника, поэтому подобный цифровой этологический портрет можно было бы рассматривать как объективный аналог предложенного Рюмке симптома чувства шизофрении (Praecox Gefühl).
Особого внимания заслуживает нейрофизиологическая объективизация психопатологических нарушений при мониторинге психического здоровья военнослужащих. Так, в ходе сравнения результатов субъективной (HADS) и объективной (психометрической экспертной по шкалам депрессии (рис. 1) и тревоги (рис. 2) Гамильтона) оценок выраженности аффективных нарушений установлено, что данные показатели были сопоставимыми в группах пациентов с РА и ДЭ. При этом они либо не отличались от аналогичных у лиц с ДФПР, как в случае субъективной оценки, либо обнаруживали статистически значимые различия на групповом уровне (при экспертной оценке), что затрудняет однозначную интерпретацию индивидуальных значений и не позволяет определить четкий диагностический порог для этих шкал.
Рис. 1. Результаты субъективной (Hospital Anxiety and Depression Scale, баллы), врачебной (Hamilton Rating Scale for Depression, баллы) и пиктополиграфической (ЭГОСКОП, относительные единицы) оценок выраженности депрессивных расстройств у обследованных.
* Отличия от лиц с донозологическими формами психологических реакций статистически значимы (p < 0,05)
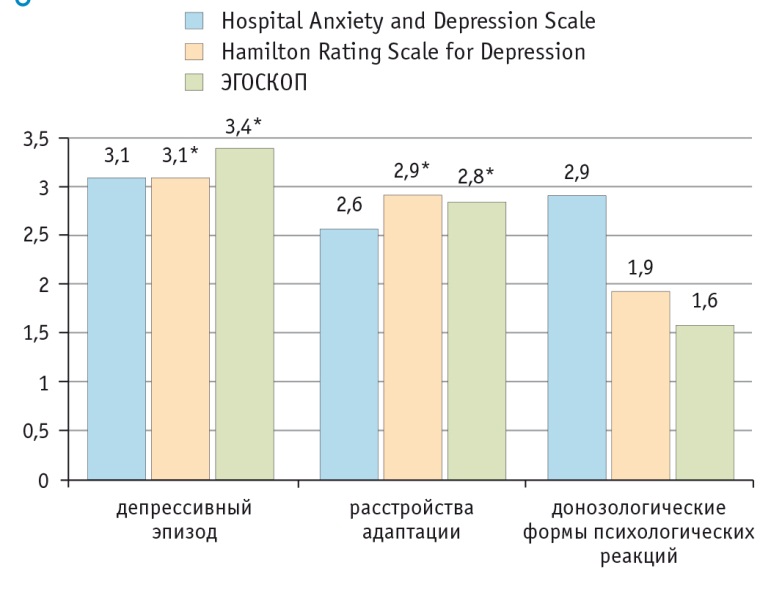
Рис. 2. Результаты субъективной (Hospital Anxiety and Depression Scale, баллы), врачебной (Hamilton Anxiety Rating Scale, баллы) и пиктополиграфической (ЭГОСКОП, относительные единицы) оценок тревожных расстройств у обследованных.
* Отличия от лиц с донозологическими формами психологических реакций статистически значимы (p < 0,05)
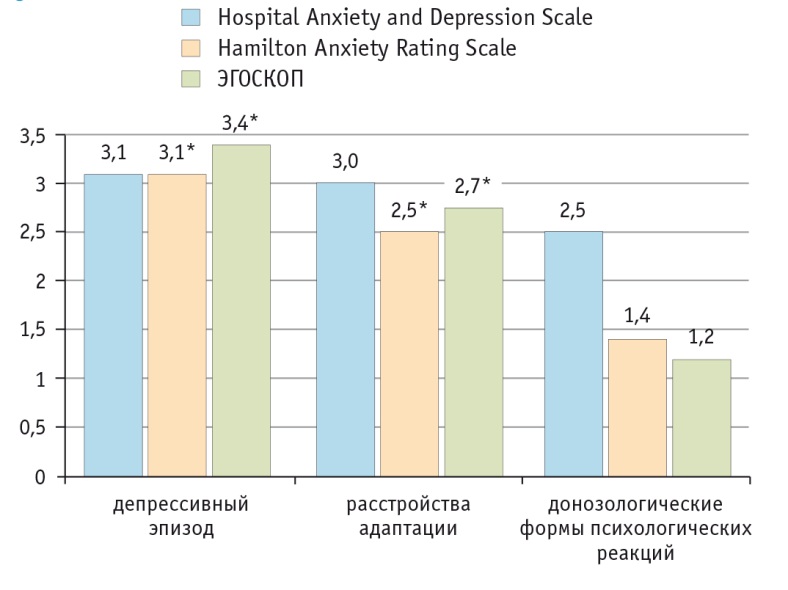
В то же время при пиктополиграфическом исследовании были выявлены наиболее отчетливые различия между значениями индекса СЭЗ у лиц с ДФПР, с одной стороны, и ДЭ и РА — с другой: у первых он практически не превышал 2 относительные единицы в связи с минимальной выраженностью у них симпатикотонических реакций, тогда как при ДЭ и РА, напротив, не встречались значения СЭЗ менее 2. Эти данные свидетельствуют о перспективности использования СЭЗ в качестве своеобразного когнитивного биомаркера аффективной патологии, верифицирующего субъективную значимость предъявляемых жалоб[15].
Биохимическая часть исследования включала в себя сопоставление психометрических и нейроэндокринных показателей. Так, обследование лиц 2-й выборки с помощью HADS не выявило значимых различий в уровнях тревоги и депрессии у пациентов трех групп (p > 0,05). Уровень кортизола у лиц с кратковременным РА оказался значимо ниже (p < 0,05) по сравнению с таковым у участников с ДЭ и пролонгированной депрессивной реакцией (258,6 ± 23,7 нмоль/л, 360,5 ± 42,7 нмоль/л и 401,9 ± 21,3 нмоль/л соответственно), между которыми значимых различий в концентрации кортизола не было.
Содержание тромбоцитарного серотонина у пациентов первой группы (324,7 ± 43,1 нг/млрд кл.) приближалось к нижнему диапазону референсных значений, у участников третьей группы располагалось в верхнем диапазоне (753,5 ± 63,3 нг/млрд кл.), а во второй группе — в среднем диапазоне референсных значений (539,7 ± 74,7 нг/млрд кл.).
Таким образом, использование данных нейроэндокринных маркеров[15] в диагностике депрессивных нарушений позволяет, с одной стороны, изучить каузальные механизмы психических расстройств с внешне сходной феноменологической картиной, а с другой — оценить патофизиологические последствия и выраженность психической патологии, что способствует лучшему пониманию патогенетических механизмов аффективных нарушений и прогнозированию прогрессирования психического расстройства, мониторингу его течения.
Данные стресс-тестирования больных с различным патогенезом депрессии показали, что у пациентов с эндогенной депрессией по сравнению с реактивной ответ на стресс-стимул был более выраженным, что проявлялось снижением ЧСС и КГР (КГР до и после стресс-стимула: 0,27 ± 0,13% и –0,14 ± 0,09% соответственно; ЧСС до и после стресс-стимула: 1,79 ± 0,68 мм рт. ст. и –0,93 ± 0,46 мм рт. ст.). Кроме того, у пациентов с эндогенной депрессией возвращение вышеперечисленных показателей к фоновым занимало больше времени (24,7 ± 4,3 с и 15,5 ± 6,1 с соответственно).
Результаты изучения нейровизуализационных маркеров[15] депрессивных расстройств в 4-й выборке показали, что при эндогенной депрессии при ПЭТ уровень метаболизма в головках хвостатых ядер был снижен на 20–40% от нормы при умеренной депрессии (до 25 баллов по HDRS) и более чем на 40% — при тяжелой (свыше 26 баллов по HDRS) (p < 0,05 по сравнению с контрольной группой), чего не наблюдалось при реактивной депрессии.
При фМРТ у пациентов с реактивной и органической депрессией функциональное «выключение» переднецингулярных отделов практически не отмечалось, в то время как у лиц с эндогенной депрессией, помимо менее выраженного, но все же имевшего место угнетения переднепоясных отделов и активации дорсолатеральной префронтальной коры, обнаруживалось отчетливое угнетение задне- и среднецингулярных отделов.
В VBM-режиме у всех пациентов с депрессивными расстройствами были выявлены изменения по сравнению с нормой в различных префронтальных корковых отделах и ряде подкорковых структур (Family-Wise (global) Error Probability, поправка на множественные сравнения достоверности «артефактных» активаций, р pfwe < 0,05). При этом у больных с реактивной и органической депрессией отмечалось качественное сходство топических изменений: в обеих группах были обнаружены снижение плотности серого вещества в орбитофронтальных, медиальных и дорсолатеральных префронтальных отделах с тенденцией к левосторонней локализации, а также изменения в инсулярных, верхнетеменных областях и миндалинах мозжечка. У пациентов с эндогенной депрессией снижение объема серого вещества в орбитофронтальных, перигенуальных и заднелобных отделах было менее обширным.
Кроме того, у всех больных с депрессивными расстройствами различного генеза выявлено угнетение активности миндалин. Данные DTI также показали качественное сходство между пациентами с реактивной и органической депрессией: в обоих случаях изменения определялись в трактах форникса и колена мозолистого тела, а также в трактах передне- и заднецингулярных областей, продольном и нижнем лобно-затылочном пучках. В количественном отношении по данным VBM и DTI при органической депрессии изменения были более выражены, чем при реактивной.
У больных с опиоидной наркоманией проводился анализ нейросети пассивного режима работы головного мозга Default Mode Network (DMN), при этом по сравнению с контрольной группой у них отмечалось ослабление функциональных связей всех структур DMN (False Discovery Rate, предел ложного обнаружения — вероятность ложноположительной связности между вокселями, pFDR < 0,05). Наиболее выраженные изменения имели место в медиальных лобных областях и предклинье в состоянии интоксикации, а в височных отделах — в состоянии ремиссии до 1 месяца. Оценка степени взаимосвязи корковых структур, отвечающих за систему «контроля поведения» (орбитофронтальная кора, префронтальная кора), с подкорковыми структурами, отвечающими за эмоции в лимбической системе, показала, что для больных с ранней ремиссией характерно ослабление функциональных связей между корковыми структурами и левым прилежащим ядром, миндалевидным телом с двух сторон, а в состоянии интоксикации в дополнение к этим изменениям была ослаблена функциональная связь между орбитофронтальной корой и скорлупой слева. Более того, в состоянии наркотического опьянения наблюдалось прерывание (p uncorr < 0,001) функциональных связей между зонами контроля и системой эмоционального подкрепления удовольствия (бледный шар, скорлупа, Nucleus accumbens и др.).
В целом ослабление функциональных связей в DMN с медиальными областями лобной коры у наркозависимых свидетельствует о нарушении процессов поведенческого контроля, мышления и принятия решения, что позволяет использовать эти данные в качестве объективизирующих критериев в диагностике болезней зависимости.
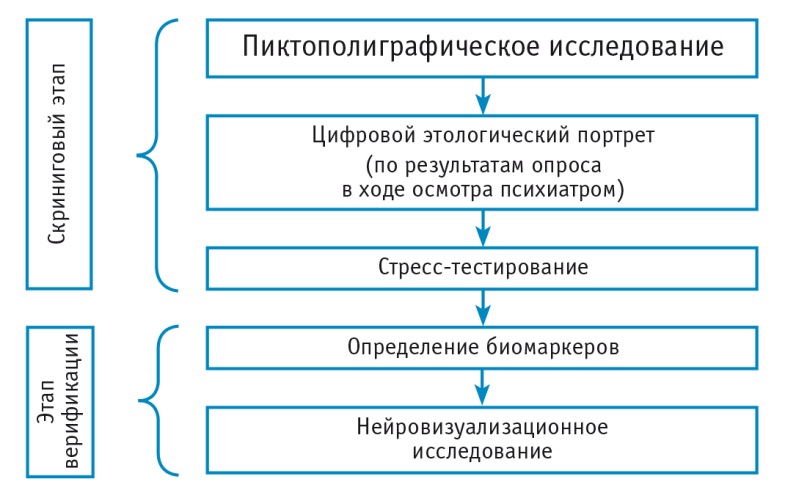
Приведенные данные свидетельствуют о возможности существенной модификации подходов к прогнозу и раннему выявлению психических расстройств у военнослужащих для их объективизации, что представляется особенно важным в свете сохраняющегося стигматизирующего эффекта психиатрических диагнозов, нередко определяющих социальный и трудовой прогноз бывших военнослужащих спустя десятилетия после увольнения даже при условии полной компенсации[16]. При этом выглядит уместной их интеграция в иерархическую диагностическую систему, где на скриниговом этапе (призывные пункты, войсковое звено) для анализа используются цифровой этологический портрет и/или результаты пиктополиграфии при заполнении психодиагностических тестов и стресс-тестирования после него, а на этапе верификации (в стационарных условиях) — результаты клинико-психопатологического, биохимического и нейровизуализационных исследований (рис. 3).
Рис. 3. Последовательность объективизации данных обследования при оценке прогноза и раннем выявлении психических расстройств у военнослужащих
Вместе с тем разработка объективных методов оценки и прогноза психического здоровья военнослужащих представляется трудноосуществимой без эффективной информационной поддержки[17] и формирования информационного поля военной психиатрии с использованием программно-технических средств для динамической оценки значимых изменений психического состояния на всех этапах прохождения военной службы. Ядром системы должен быть единый банк данных о психическом здоровье, а также о результатах военно-профессиональных и социально-психологических обследований прикрепленного контингента с авторизацией прав доступа для всех пользователей данного ресурса (офицеров медицинской службы, врачей из числа гражданского персонала МО РФ, специалистов психологической работы). Сведения о состоянии и результатах мониторинга психического здоровья должны храниться в виде персональных электронных медицинских записей пациентов, при необходимости переносимых на персонифицированные электронные носители медицинской информации (электронная медицинская карта, электронный жетон военнослужащего).
Основные сведения для первичного наполнения данных о психическом здоровье призывного контингента должны поступать на этапе комплектования ВС РФ, проводимого в военных комиссариатах и пунктах отбора на военную службу по контракту, при проведении профессионального психологического отбора и первичного медицинского освидетельствования граждан, поступающих на военную службу. Информация, полученная при мониторинге психического здоровья в рамках плановых обследований, должна передаваться в информационное поле из центров обработки данных, организованных при органах военного управления медицинской службы, с учетом прикрепления военнослужащего к месту несения военной службы.
ЗАКЛЮЧЕНИЕ
Практическая реализация описанных подходов позволит персонифицировать оказание медико-психологической помощи военнослужащим, повысить качество ранней диагностики психических расстройств, аддиктивного и суицидального поведения, а значит, эффективность всей психопрофилактической работы в войсках. Вместе с тем дальнейшие перспективы объективизации и прогноза психических расстройств у военнослужащих определяются междисциплинарными усилиями не только в перечисленных областях, но и в области нейрогенетических, нейробиологических (в широком смысле) и нейрофизиологических исследований по проблемам как боевой, так и небоевой патологии при непременном дальнейшем развитии информационных технологий, позволяющих в условиях лимита времени, сил и средств решать сугубо организационные и клинико-диагностические задачи.







