ВВЕДЕНИЕ
Ревматоидный артрит (РА) — системное аутоиммунное заболевание, характерные черты которого — синовиты мелких и крупных суставов и воспаление периартикулярных мягких тканей. Частота РА составляет от 3,1 до 100 случаев на 10 000 человек, что делает его самым распространенным воспалительным ревматологическим заболеванием[1]. У пациентов с РА заметно снижается качество жизни, они часто испытывают слабость и депрессию. Более того, РА является и социальным бременем, так как многие пациенты теряют работоспособность и способность к самообслуживанию[2].
Важный элемент клинической картины РА — мышечная слабость. В сравнении со значениями в здоровой популяции у пациентов с РА отмечается уменьшение мышечной силы на 25–70%, притом оно опережает потерю объема мышечной массы[3]. В связи с этим клинические методы диагностики саркопении будут обладать низкой специфичностью и приведут к гипердиагностике состояния. Используемые инструментальные методы диагностики, к которым относят биоимпендансный анализ и двухэнергетическую рентгеновскую абсорбциометрию (dual energy X-ray absorbtiometry, DEXA), имеют свои преимущества и недостатки. Так, к преимуществам биоимпендансного анализа можно отнести простоту выполнения процедуры, ее безопасность и большой объем референсных данных. Однако недостатки метода — зависимость результатов обследования от степени гидратации организма, ожирения и длины конечностей, интерпретация результатов осложняется отсутствием общепринятого референса.
Преимуществами DEXA принято считать воспроизводимость результата сканирования, безопасность исследования (степень лучевой нагрузки не превышает 0,6 мкЗв) и возможность оценки композитного состава отдельных зон. С помощью DEXA с программой Total Body определяются масса и процент содержания жировой, костной и тощей (мышцы и жидкие среды) тканей[4].
К недостаткам DEXA относят необходимость строгого соблюдения техники исследования, бо́льшую длительность процедуры, чем у биоимпендансного анализа, и отсутствие общепринятого референса. Для клинических исследований DEXA является предпочтительным методом изучения композитного состава тела.
Следует отметить, что несомненное преимущество инструментальных методов оценки композитного состава тела — возможность диагностировать ревматическую кахексию (РК) — осложнение РА, сопровождающееся снижением объема безжировой массы тканей при сохраненном или увеличенном объеме массы жировой ткани[5]. Это осложнение ассоциировано с повышением риска смерти от всех причин и в частности от сердечно-сосудистых заболеваний.
Несмотря на относительную простоту диагностики и широкую распространенность РК, по результатам клинических исследований, в реальной практике она диагностируется крайне редко в связи с низкой настороженностью практикующих врачей.
Несфатин 1 (НФ-1), также известный как нуклеобиндин 2 (NUCB2), — это нейроэндокринный пептид, участвующий в поддержании гомеостаза через регуляцию метаболизма, энергии гомеостаза и приема пищи[6]. В ряде работ продемонстрировано, что у лиц с ожирением, особенно с морбидным, сывороточный уровень НФ-1 выше, чем у людей без ожирения, и ассоциирован с сывороточным уровнем инсулина, индексом инсулинорезистентности Homeostasis Model Assessment of Insulin Resistance, абсолютной и относительной массой жировой ткани[7, 8]. Однако в международной литературе представлены и противоположные данные, когда в группе пациентов с ожирением сывороточный уровень НФ-1 был статистически значимо ниже, чем в группе без ожирения[9].
Особого внимания заслуживают исследования, которые указывают на связь сывороточного уровня НФ-1 с тревогой и депрессией, при этом у женщин корреляция между уровнем нейропептида и степенью тревоги положительная, а у мужчин — отрицательная[6]. В то же время в экспериментальной работе по моделированию геморрагического инсульта у мышей авторы показали, что интраперитонеальное введение НФ-1 приводило к меньшему повреждению центральной нервной системы, чем в группе без лечения и группе, в которой вводился солевой раствор в сопоставимом объеме[10].
Наш коллектив авторов изучал роль НФ-1 в воспалительном процессе на примере пациентов с РА. Установлено, что сывороточный уровень НФ-1 у больных РА значимо выше, чем у людей без воспалительных заболеваний суставов. Более высокая концентрация НФ-1 характерна для пациентов с РА с более высокой степенью его активности, серопозитивностью по ревматоидному фактору (РФ) и продолжительностью болезни более 10 лет. Высокий уровень НФ-1 положительно коррелировал с повышенными концентрацией С-реактивного белка и скоростью оседания эритроцитов[11].
В свете вышесказанного представляет интерес изучение ассоциации сывороточного уровня НФ-1 и показателей композитного состава тела у пациентов с РА.
Цель исследования: изучить ассоциацию сывороточного уровня НФ-1 с индексом массы тела (ИМТ), показателями композитного состава тела и РК.
МАТЕРИАЛЫ И МЕТОДЫ
В одномоментное сравнительное исследование включены 110 человек с РА, диагностированным на основании классификационных критериев American College of Rheumatology/European League against Rheumatism 2010, и 60 человек без хронических заболеваний, требующих постоянного приема лекарственных препаратов, наблюдавшихся амбулаторно в консультативно-диагностическом отделении ФГБНУ «НИИ КиЭР им. А.Б. Зборовского» (г. Волгоград) с 2017 по 2019 г. Письменное информированное согласие получено от всех участников.
Критерии включения в основную группу: верифицированный РА, возраст от 18 до 90 лет, подписанное добровольное информированное согласие на участие в исследовании. Критерии исключения: наличие злокачественных новообразований, хроническая болезнь почек С4 и С5 стадий, сахарный диабет 2 типа, беременность.
Проводилось стандартное клинико-лабораторное обследование всех участников. Дополнительно методом иммуноферментного анализа определялись сывороточные уровни НФ-1 (RayBio Nesfatin Enzyme Immunoassay Kit) и антител к циклическим цитруллинированным пептидам (АЦЦП) с использованием коммерческих тест-систем. Все участники прошли DEXA с программой Total Body на остеоденситометре LUNAR DPX Pro GE (США).
РК диагностировалась при уменьшении индекса безжировой массы ниже 10-перцентиля и увеличении индекса массы жировых тканей выше 25-го перцентиля. Референсные значения взяты из работы А. Coin и соавт., проведенной в итальянской популяции[12].
Исследование одобрено комитетом по биомедицинской этике ФГБОУ ВО «Волгоградский государственный медицинский университет» Министерства здравоохранения Российской Федерации (протокол № 2095-2016 от 13 января 2017 г.).
Статистический анализ осуществлялся с использованием пакета программ Statistica 10.0. Нормальность распределения количественных показателей проверялась методом Колмогорова — Смирнова и Лиллиефорса. Показатели, имеющие нормальное распределение, представлены в формате M ± SD [95% доверительный интервал (ДИ)], ненормальное распределение — Me [Q1–Q3]. Внутригрупповой анализ количественных показателей для нормально распределенных данных производился с помощью критерия Стьюдента (t), для ненормально распределенных — с применением U-критерия Манна — Уитни (в связи с тем, что число испытуемых превышало 30, использовалась Z-аппроксимация). Корреляционный анализ ненормально распределенных данных проводили при помощи критерия Спирмена (ρ). Результаты считали статистически значимыми при р ≤ 0,05.
РЕЗУЛЬТАТЫ
Пациенты с РА и условно здоровые лица были сопоставимы по возрасту (56,8 [47,4–62,6] против 52,0 [40,6–60,0] года соответственно, Z = 0,55; p = 0,585) и ИМТ (27,9 [23,2–32,0] против 25,7 [23,0–29,2] кг/м2 соответственно, Z = 0,29; p = 0,770). Средний уровень НФ-1 у пациентов с РА составил 50,49 ± 34,05 (95% ДИ: 44,05–56,9) нг/мл, что выше значений у условно здоровых людей — 31,61 ± 3,17 (95% ДИ: 30,8–32,4) нг/мл (t = 4,28; p < 0,0001). Клиническая характеристика больных с РА представлена в таблице 1.
Таблица 1. Клиническая характеристика пациентов с ревматоидным артритом (РА)

Большинство включенных в исследование пациентов были работоспособного возраста, преимущественно женщины с избыточной массой тела. Более двух третей больных имели агрессивный фенотип РА в связи с повышением уровней РФ и АЦЦП, умеренную степень активности заболевания с умеренным нарушением суставной функции. РК выявлена у 30 пациентов, что соотносится с данными, представленными в работах других авторов, в которых частота РК у больных РА составляла от 18 до 30%.
Нами проведен внутригрупповой анализ Краскела — Уоллиса для поиска зависимости медианы уровня НФ-1 от величины ИМТ в группах пациентов с РА и условно здоровых лиц. Данные представлены на рисунках 1 и 2.
Рис. 1. Внутригрупповой анализ различий медиан уровня несфатина 1 (НФ-1) в зависимости от индекса массы тела (ИМТ) у пациентов с ревматоидным артритом
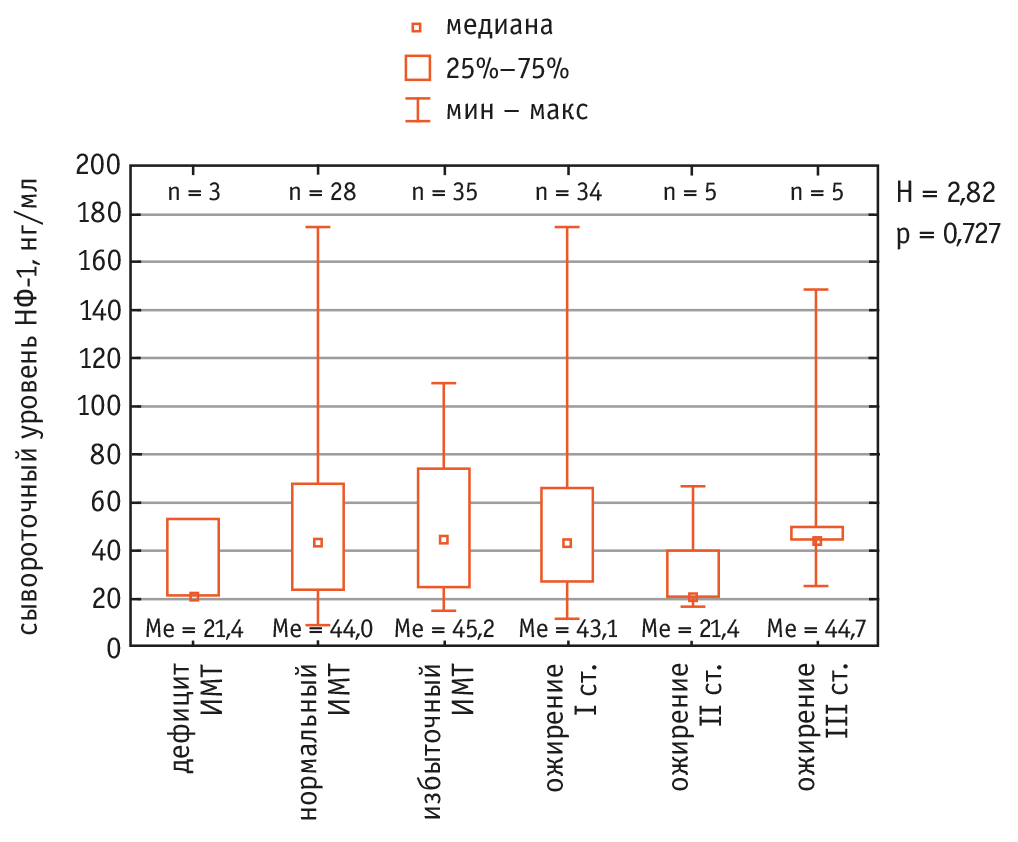
Рис. 2. Внутригрупповой анализ различий медиан уровня несфатина 1 (НФ-1) в зависимости от индекса массы тела (ИМТ) в группе условно здоровых лиц
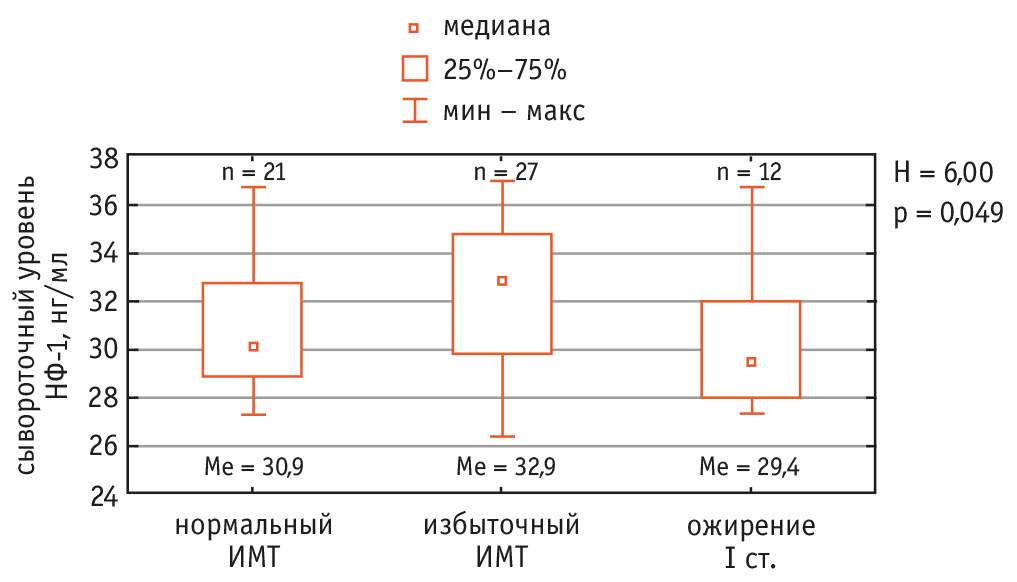
Несмотря на различие медиан содержания НФ-1 при разной величине ИМТ у пациентов с РА, статистически значимая взаимосвязь не выявлена. Этот результат отличается от данных международной литературы, которые продемонстрировали взаимосвязь уровня НФ-1 с ожирением[13]. Следует отметить, что в указанных работах не исследовалась ассоциация концентрации НФ-1 и ИМТ у пациентов с системными воспалительными заболеваниями. Таким образом, можно предположить, что наличие РА как основного заболевания могло повлиять на уровень исследуемого вещества и уменьшить взаимосвязь с ИМТ. Для проверки гипотезы нами произведен аналогичный анализ, но в группе условно здоровых лиц. Результат представлен на рисунке 2.
В группе здоровых людей медиана сывороточного уровня НФ-1 была больше у участников с избыточной массой тела, чем при нормальном ИМТ и ожирении I степени. В ряде работ показано, что НФ-1 стимулирует чувство голода и прием пищи[14, 15], что приводит к развитию метаболического синдрома и набору массы тела. Однако большое значение имеют и полиморфизмы нуклеотидной последовательности гена, кодирующего НФ-1, которые ассоциированы с ИМТ, массой тела и массой тощей ткани[16].
Таким образом, несмотря на подтверждение ассоциации сывороточного уровня НФ-1 с метаболическим синдромом, требуются дополнительные и более подробные исследования, уточняющие конкретный механизм этой взаимосвязи. Если будет определен механизм влияния НФ-1 на обмен веществ, то данный показатель может быть включен в клинические протоколы.
Нами проведен корреляционный анализ взаимосвязи сывороточного уровня НФ-1 с показателями композитного состава тела по отдельным зонам у больных РА. Результаты представлены в таблице 2.
Таблица 2. Корреляционный анализ взаимосвязи уровня несфатина 1 с показателями композитного состава тела по отдельным зонам у больных ревматоидным артритом
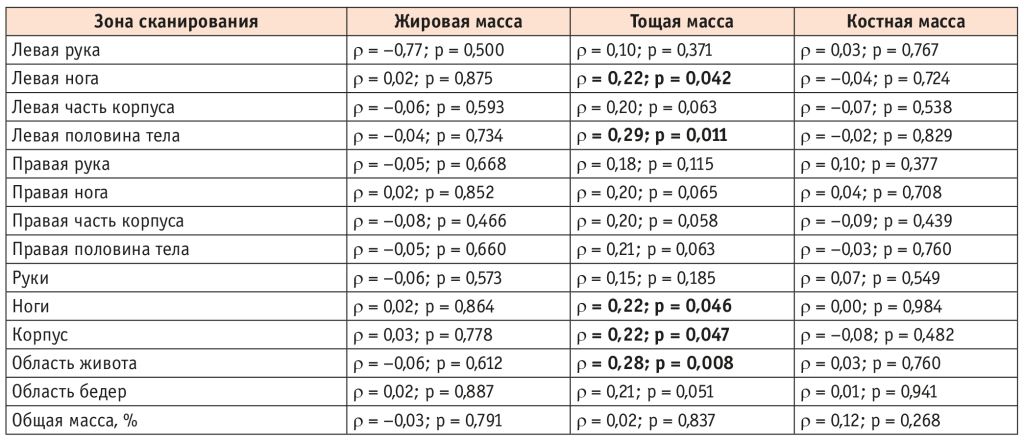
Сывороточный уровень НФ-1 у пациентов с РА статистически значимо коррелировал с массой тощей ткани в ногах (и отдельно в левой ноге), в левой половине тела, корпусе и брюшной зоне. Близкой к статистически значимой была корреляция с массой тощей ткани в области бедер. При этом сывороточный уровень НФ-1 не ассоциировался с общей массой тощей ткани. Следует отметить, что мы не обнаружили корреляцию содержания НФ-1 с массой костной и жировой тканей у пациентов с РА.
Известно, что наличие системного воспалительного процесса способствует снижению массы костной ткани и увеличению массы жировой. Кроме того, активно используемые в терапии РА препараты из группы глюкокортикоидов (88 пациентов принимали их ранее, 77 продолжали прием на момент исследования) способствуют активации костной резорбции, угнетению костного ремоделирования, развитию инсулинорезистентности с увеличением массы жировой ткани и стероид-индуцированной потере массы мышечной ткани[17, 18].
Проявляя антианорексигенный эффект, НФ-1 может способствовать достаточному потреблению нутриентов для поддержания гомеостаза тощей ткани, нарушение которого у пациентов с воспалительными заболеваниями играет важную роль в прогрессировании функциональных нарушений[19].
Отсутствие взаимосвязи уровня НФ-1 с массой тощей ткани в верхних конечностях можно объяснить болевым синдромом в кистях и плечах у пациентов с РА, который способствует ее ускоренной потере. В то же время мышцы туловища и ног постоянно напрягаются при ходьбе, что в совокупности с увеличенным приемом нутриентов больными с более высоким сывороточным уровнем НФ-1 будет сохранять массу этой ткани.
При проведении внутригруппового анализа Манна — Уитни мы установили, что медианы сывороточного уровня НФ-1 статистически значимо не различались у пациентов с РК и без нее. Данные представлены на рисунке 3.
Рис. 3. Внутригрупповой анализ взаимосвязи сывороточного уровня несфатина 1 (НФ-1) с ревматической кахексией (РК)
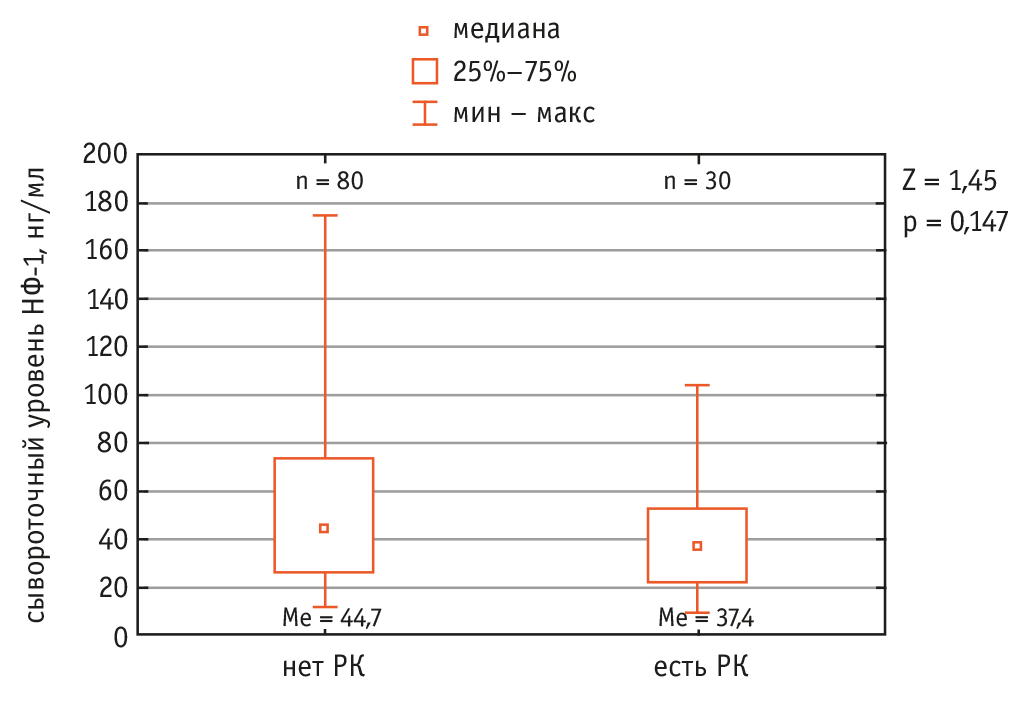
Несмотря на кажущееся различие медиан сывороточного уровня НФ-1 у пациентов с РК и без нее, статистической значимости оно не имеет. Можно предположить, что наличие РА, классической модели системного воспалительного процесса, оказывает выраженное влияние как на композитный состав тела, так и на сывороточный уровень НФ-1.
ЗАКЛЮЧЕНИЕ
Хотя нами обнаружена взаимосвязь между сывороточным уровнем НФ-1 и массой тощей ткани в отдельных зонах у больных РА, данный нейроэндокринный пептид не может использоваться как маркер диагностики РК. Необходимы дополнительные исследования, которые бы уточнили механизм ассоциации уровня НФ-1 с массой тощей ткани и, вероятно, способствовали бы разработке нового подхода к контролю этого показателя.
Поступила: 13.04.2023
Принята к публикации: 20.06.2023







