ВВЕДЕНИЕ
Амлодипин — дигидропиридиновый блокатор кальциевых каналов третьего поколения. Блокируя потенциал-зависимые кальциевые каналы L-типа, амлодипин снижает внеклеточный приток кальция внутрь клеток, что уменьшает внутриклеточную концентрацию данного иона в гладкомышечных клетках сосудов и вызывает расширение сосудов[1].
Амлодипин обладает выраженным антигипертензивным эффектом и является одним из основных препаратов для лечения артериальной гипертензии (АГ)[2], а также проявляет антиангинальные свойства и применяется для симптоматического лечения стенокардии напряжения[3] и вазоспастической стенокардии[4].
Амлодипин действует длительно. Сочетание большого объема распределения (1300–1600 л) и относительно низкого (по сравнению с другими блокаторами кальциевых каналов) клиренса (15–30 л/ч) приводит к тому, что период полувыведения амлодипина составляет 40–60 часов, что значительно больше, чем при применении других препаратов-антагонистов кальция (3–15 часов)[5]. С учетом данных особенностей фармакокинетики препарат применяется один раз в день.
Однако иногда его принимают 2 раза в день, или, наоборот, пациенты пропускают прием амлодипина. Эти отклонения от рекомендованной схемы могут привести к повышению плазменной/сывороточной концентрации амлодипина и риска развития относительной передозировки или к снижению эффективности проводимой терапии соответственно.
Амлодипин метаболизируется в печени с участием изоферментов семейства цитохромов P450 CYP3A[6].
Изменение активности данных ферментов в результате фармакокинетических межлекарственных взаимодействий или полиморфизмов в их генах могут также повлиять на плазменную концентрацию амлодипина[7], а значит, на эффективность и безопасность проводимой терапии.
Одним из возможных способов оптимизации терапии является контролирование фармакокинетики амлодипина и проведение терапевтического лекарственного мониторинга[8].
Данный подход позволяет связать фармакокинетику препарата с его эффективностью, когда забор крови сопровождается измерением артериального давления (АД)[9], и выявить истинную резистентную АГ, когда отсутствует контроль АД, несмотря на терапевтические концентрации препарата в плазме/сыворотке крови. Можно также установить фармакокинетические причины АГ, когда после приема лекарственного препарата вещество не достигает терапевтической концентрации в плазме/сыворотке крови, и объективно оценить приверженность пациентов к лечению[10]. В России подобные исследования практически не проводятся.
Цель исследования: оценить фармакокинетику амлодипина у пациентов с АГ.
МАТЕРИАЛЫ И МЕТОДЫ
Проведено клиническое одноэтапное контролируемое открытое когортное исследование на базе Рязанского областного клинического кардиологического диспансера, период исследования — февраль 2022 г. — февраль 2023 г. Оно одобрено локальным этическим комитетом при Рязанском государственном медицинском университете имени академика И.П. Павлова (протокол заседания № 11 от 04.03.2022 г.).
Критерии включения:
-
возраст старше 18 лет;
-
подписанная форма информированного согласия;
-
установленный диагноз АГ на основании клинических рекомендаций «Артериальная гипертензия у взрослых», утвержденных Научно-практическим советом Минздрава РФ, 2020 г.;
-
обязательное соблюдение пациентами рекомендаций по модификации образа жизни в соответствии с клиническими рекомендациями «Артериальная гипертензия у взрослых», утвержденными Научно-практическим советом Минздрава РФ, 2020 г.;
-
регулярный прием любых двух антигипертензивных препаратов (АГП) (лизиноприла, амлодипина, валсартана, метопролола) в сочетании с индапамидом в течение месяца, возможно, в фиксированных комбинациях, в стабильных дозировках;
-
фертильные пациентки женского пола должны были использовать надлежащие методы контрацепции на протяжении всего периода исследования.
Критерий исключения — беременность.
Проводилось плановое обследование всех пациентов, которое включало антропометрию, оценку АД, частоты сердечных сокращений, общий и биохимический анализы крови, анализ мочи, эхокардиографию, суточное мониторирование АД (СМАД).
Дополнительно, по результатам СМАД, все участники были разделены на две группы:
1) пациенты с контролируемой АГ, у которых среднесуточное систолическое АД (САД) < 135 мм рт. ст., среднесуточное диастолическое АД (ДАД) < 85 мм рт. ст., среднее ночное САД < 120 мм рт. ст., среднее ночное ДАД < 80 мм рт. ст.;
2) пациенты с неконтролируемой АГ, у которых, по данным СМАД, имелся хотя бы один из следующих маркеров плохого контроля АД: среднесуточное САД ≥ 135 мм рт. ст., среднесуточное ДАД ≥ 85 мм рт. ст., среднее ночное САД ≥ 120 мм рт. ст., среднее ночное ДАД ≥ 80 мм рт. ст.
Всего в исследование включены 183 пациента c АГ, их средний возраст — 63,4 ± 11,1 года, из них 79 (43,2%) мужчин, длительность АГ — 10 (7,5; 20) лет. В группу контролируемой АГ вошли 85 человек, средний возраст — 65,4 ± 10,8 года, из них 32 (37,6%) мужчины, длительность АГ — 10 (10; 20) лет. В группу неконтролируемой АГ включили 98 больных, средний возраст — 61,6 ± 11,1 года, из них 47 (47,9%) мужчин, длительность АГ — 10 (5; 20) лет.
По гендерному составу группы были сопоставимы, но пациенты с неконтролируемой АГ были статистически значимо моложе лиц с контролируемым заболеванием (p = 0,02).
После рандомизации утром перед приемом АГП и через 2 ч после приема амлодипина брали образцы венозной крови для оценки концентрации анализируемого вещества методом высокоэффективной жидкостной хроматографии с тандемной масс-спектрометрией с помощью хроматографа Ultimate 3000 и масс-спектрометра TSQ Fortis (Thermo Fisher Scientific). Применяли валидированную методику для аналитического диапазона 1–1000 нг/мл, описанную ранее[11].
Полученные результаты обрабатывали с использованием программ StatSoft Statistica 13.0 (США, номер лицензии JPZ811I521319AR25ACD-W) и Microsoft Excel for MAC ver. 16.24 (ID 02984-001-000001). Распределение полученных данных оценивали с помощью критерия Шапиро – Уилка. Если значение имело нормальное распределение, использовали t-критерий Стьюдента для оценки статистической значимости различий, в остальных случаях применялся тест Манна — Уитни. Значения частот сравнивались с помощью точного критерия Фишера.
Полученные результаты представлены в таблицах в виде среднего и стандартного отклонения (М ± SD) для данных с нормальным распределением или медианы (Me), верхних и нижних квартилей (Q1; Q2) для данных с ненормальным распределением.
РЕЗУЛЬТАТЫ
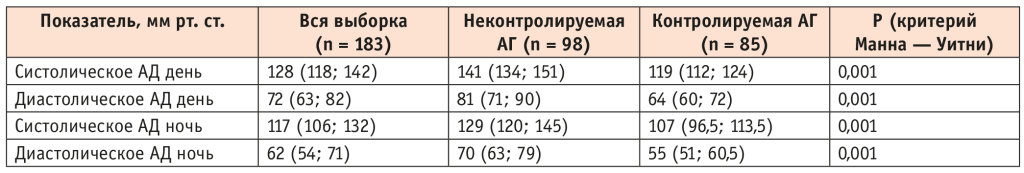
Значения дневного и ночного САД и ДАД, по данным СМАД, в группе неконтролируемой АГ статистически значимо превышали показатели участников группы с контролем АД (табл. 1).
Таблица 1. Данные суточного мониторирования артериального давления (АД), у пациентов с артериальной гипертензией (АГ), Me (Q1; Q2)
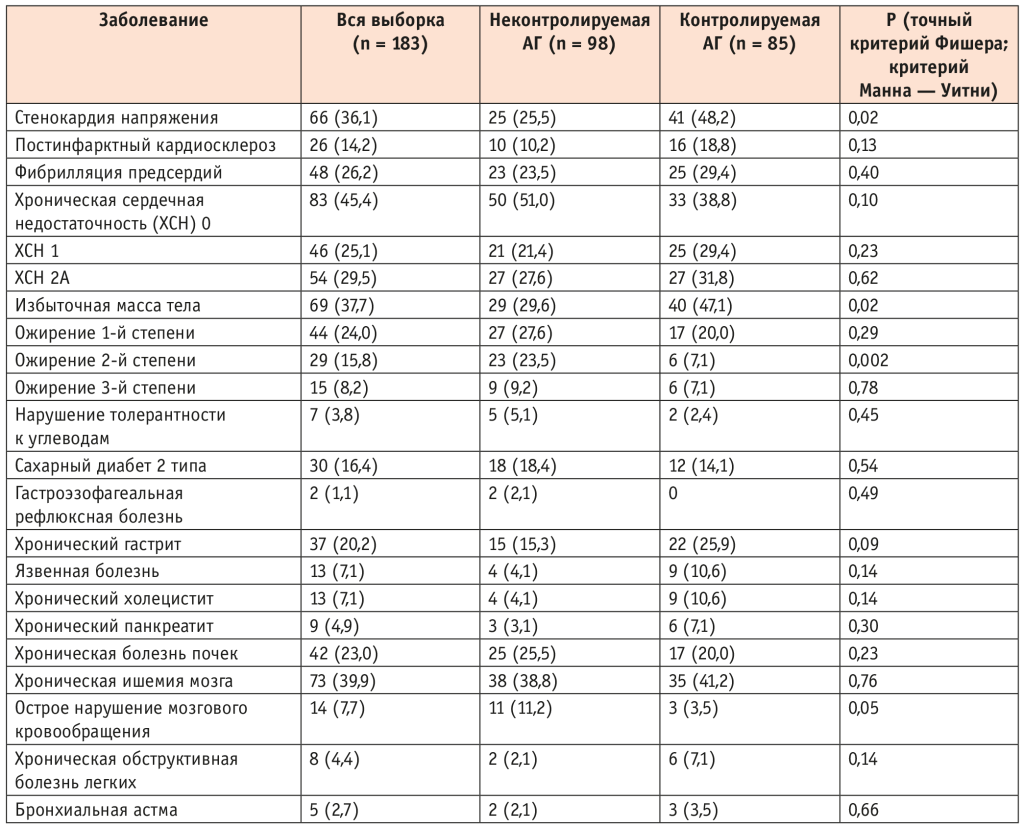
По основным сопутствующим заболеваниям пациенты двух групп были сопоставимыми. Статистически значимо чаще в группе с контролем давления встречались лишь стенокардия напряжения (p = 0,02) и избыточная масса тела (p = 0,02) и реже — ожирение 2-й степени (p = 0,002) и острое нарушение мозгового кровообращения (p = 0,05) (табл. 2). Распространенность заболеваний желудочно-кишечного тракта и почек, которые могли повлиять на фармакокинетику амлодипина, была сходной в обеих группах. Медиана функционального класса стенокардии в обеих группах и в общей выборке оказалась одинаковой — 2 (2; 3).
Таблица 2. Сопутствующие заболевания у пациентов с артериальной гипертензией (АГ), n (%)
В данной работе представлены результаты анализа концентраций амлодипина у пациентов с контролируемой и неконтролируемой АГ. Анализ концентраций других АГП будет представлен в последующих публикациях; 98,9% пациентов, включенных в исследование, принимали амлодипин.
Суточная доза амлодипина у больных c контролируемой АГ была значимо (на 13,9%) ниже (p = 0,03), чем у лиц с неконтролируемой АГ. При этом кратность (один или два раза в день) и время приема (утром, в обед или вечером) статистически значимо не различались в сравниваемых группах (табл. 3).
Таблица 3. Особенности приема амлодипина и его сывороточные концентрации у пациентов с артериальной гипертензией (АГ)
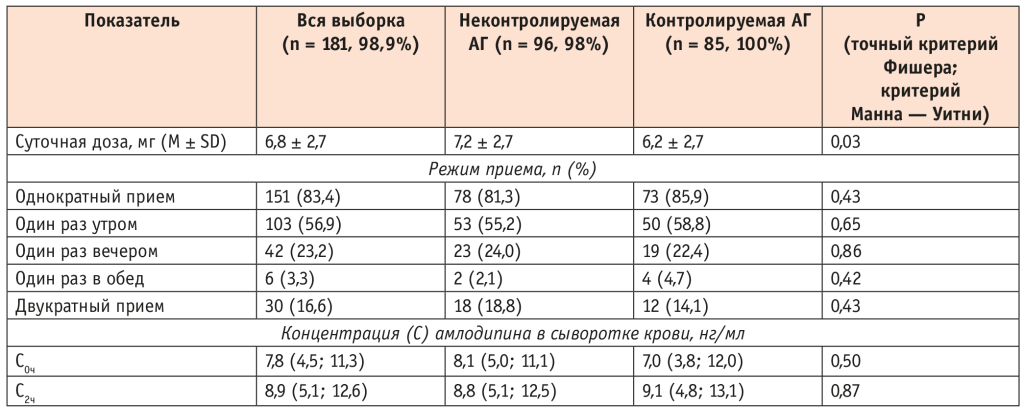
И равновесная концентрация амлодипина, и концентрация через 2 ч после приема у больных с неконтролируемой АГ статистически значимо не отличались от таковых у пациентов с контролируемой АГ (p > 0,05).
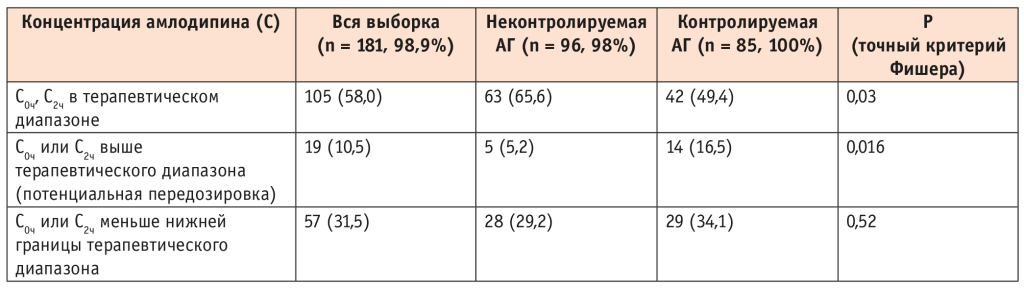
Согласно данным литературы, терапевтический диапазон концентраций амлодипина в сыворотке крови составляет 5–18 нг/мл[12]. У 65,6% пациентов с неконтролируемой и 49,4% с контролируемой АГ она находилась в пределах терапевтического диапазона (различия между группами были статистически значимыми, p = 0,03).
У 5,2% участников с неконтролируемой и у 16,5% с контролируемой АГ концентрация амлодипина оказалась выше терапевтического диапазона (p = 0,016), и это свидетельствует о том, что данные пациенты находятся в зоне риска развития относительной передозировки изучаемого лекарственного препарата, несмотря на прием в терапевтических дозах. С другой стороны, более высокие концентрации АГП у пациентов с контролируемым АД могут объяснить бо́льшую эффективность терапии, чем в группе неконтролируемого АД.
У 29,2% больных с неконтролируемой и 34,1% с контролируемой АГ концентрация амлодипина была ниже терапевтического диапазона (p > 0,05) (табл. 4).
Таблица 4. Соответствие концентрации амлодипина у пациентов с артериальной гипертензией (АГ) терапевтическому диапазону, n (%)
ОБСУЖДЕНИЕ
Анализ фармакокинетики лекарственных веществ (их концентрации в плазме/сыворотке крови) широко используется в клинической фармакологии для проведения терапевтического лекарственного мониторинга и повышения эффективности и безопасности лечения за счет поддержания концентрации лекарственного вещества в пределах терапевтического диапазона[8].
В кардиологии терапевтический лекарственный мониторинг разработан для отдельных препаратов. Например, показано, что высокая концентрация дигоксина в сыворотке крови у пациентов с застойной сердечной недостаточностью связана с повышением общего уровня смертности от всех причин (0,5–0,8 нг/мл — 29,9%; 0,9–1,1 нг/мл — 38,8% и ≥ 1,2 нг/мл — 48,0%, р = 0,006). Среди больных с концентрацией дигоксина от 0,5 до 0,8 нг/мл смертность была на 6,3% (95% доверительный интервал (ДИ): 2,1–10,5%) ниже, чем у лиц, получавших плацебо[13].
В последнее время все чаще определение концентрации лекарственных веществ используется для оценки приверженности пациентов к проводимому лечению[14].
Особенности фармакокинетики препарата важны и для правильного его приема, например в утреннее или вечернее время. В метаанализе девяти рандомизированных контролируемых исследований с участием 1215 человек показано, что время приема амлодипина не влияло на офисное АД (относительный риск (ОР) = –0,03, 95% ДИ: –0,93–0,88, р = 0,96), дневное АД (ОР = –0,30, 95% ДИ: –1,05–0,46, р = 0,44). Однако прием амлодипина вечером, когда его максимальная концентрация приходилась на ночное время, мог значительно снизить АД ночью (ОР = 2,04, 95% ДИ: 1,27–2,81, р < 0,00001), и его антигипертензивная эффективность была выше (ОР = 0,64, 95% ДИ: 0,55–0,74, р < 0,00001)[15].
В ходе настоящего исследования впервые в российской популяции оценена фармакокинетика амлодипина у пациентов с АГ. При этом пациенты были распределены на две группы: с контролируемым и неконтролируемым АД.
При анализе концентрации амлодипина в сыворотке крови пациентов выяснилось, что и равновесная концентрация, и концентрация амлодипина через 2 ч после приема у пациентов с неконтролируемой и контролируемой АГ статистически значимо не различались. В то же время в группе контролируемой АГ было статистически значимо больше больных с концентрацией амлодипина в сыворотке крови выше терапевтического диапазона. Полученные данные свидетельствуют о том, что для достижения целевых цифр АД требуется более высокая сывороточная концентрация изучаемого антигипертензивного препарата. Но, наравне с достижением нужного АД, сывороточная концентрация амлодипина выше терапевтического диапазона может предрасполагать к развитию нежелательных лекарственных реакций[16, 17].
С другой стороны, у 29,2% пациентов с неконтролируемой и 34,1% с контролируемой АГ концентрация амлодипина была ниже терапевтического диапазона: несмотря на прием антигипертензивного препарата, его концентрация в сыворотке крови не достигала терапевтических значений и, следовательно, не давала ожидаемого фармакологического эффекта. Таким образом, у 29,2% больных с неконтролируемой АГ одной из причин неэффективности фармакотерапии может являться фармакокинетика амлодипина, то есть недостижение терапевтических концентраций, а повышение дозы принимаемого препарата для достижения значений терапевтического диапазона способно помочь в контроле АД.
ЗАКЛЮЧЕНИЕ
Проведение терапевтического лекарственного мониторинга и оценка фармакокинетики амлодипина в клинической практике могут быть полезны для повышения эффективности и безопасности проводимой терапии.
Поступила: 24.11.2023
Принята к публикации: 15.01.2024







